Хинолиновая кислота
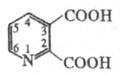
ХИНОЛИНОВАЯ КИСЛОТА (2,3-пиридиндикарбоновая к-та), мол. м. 167,12; бесцв. кристаллы, т. пл. 190-191 °С (с разл.). Раств. в воде, плохо раств. в этаноле, диэтиловом эфире и др. орг. р-рителях. При нагр. выше 190 °С или с СН3СООН декарбоксилируется с образованием никотиновой кислоты. С солями тяжелых металлов легко образует плохо р-римые в воде и орг. р-рителях соли, используемые для ее идентификации, напр. соль Сu(II) голубого цвета, соль Hg(II) коричневого цвета, Fе(III) - черно-коричневого, U(IV) - желто-зеленого цвета.
При нагр. с (СН3СО)2О или SOC12 хинолиновая кислота образует внутр. ангидрид, с NH3 в сухом бензоле - имид (т. пл. 230 °С), с СН3ОН в НС1 - диметиловый эфир (т. пл. 53-54 °С). При взаимод. с СН3ОН в конц. H2SO4 хинолиновая кислота превращается в 2-метоксикарбонилникотиновую к-ту. Восстановление хинолиновой кислоты Na в кипящем этаноле приводит к гексагидрохинолиновой к-те, в кипящем изоамиловом спирте - к гексагидроникотиновой к-те.
Получают хинолиновую кислоту окислением хинолина или 2,3-диметилпиридина щелочным р-ром КМnО4.
Лит.: Гетероциклические соединения, под ред. Р. Эльдерфилда, пер. с англ., т. 1, М., 1953, с. 446; Общая органическая химия, пер. с англ., т. 8, М., 1985, с. 228.
Л. Н. Яхонтов.

Дополнения к описанию хинолиновой кислоты:
Биологическая значимость: Является промежуточным метаболитом в метаболизме триптофана по кинурениновому пути. В нервной системе выступает как эндогенный нейротоксин, избыток которого связывают с нейродегенеративными заболеваниями, так как она является агонистом NMDA-рецепторов.
Механизм нейротоксичности: Избыточная активация NMDA-рецепторов хинолиновой кислотой приводит к эксайтотоксичности — гибели нейронов из-за перевозбуждения.
Практическое применение: Используется в научных исследованиях в качестве инструментального агента для изучения функций NMDA-рецепторов и моделирования нейродегенеративных процессов.