Окись этилена
Окись этилена получается при пропускании смеси этилена с воздухом (не более 3% этилена) при 300—400° С над катализаторами, содержащими мелко раздробленное серебро:
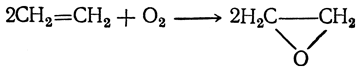
Она легко получается также действием концентрированных щелочей на этиленхлоргидрин:
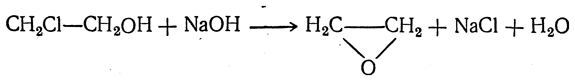
Окись этилена — жидкость, кипящая при +10,7° С; относительная плотность 0,897 (при 0°С). С водой она смешивается в любых соотношениях.
Являясь внутренним простым эфиром, окись этилена образует оксониевые соединения, подобно простым эфирам с открытой цепью:
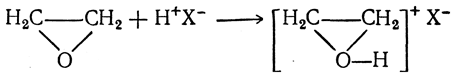
Многие реакции окиси этилена протекают с промежуточным образованием подобного соединения.
При нагревании до 400° С окись этилена превращается в изомерный ей уксусный альдегид. С водой она реагирует при нагревании, образуя этиленгликоль, причем в качестве промежуточных продуктов могут быть получены полиэтиленгликоли. Окись этилена легко присоединяет галоидоводороды (даже в водном растворе), образуя галоидгидрины гликоля, например:
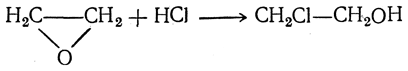
Благодаря этому окись этилена, не обладающая сколько-нибудь заметными основными свойствами, может осаждать слабые основания из водных растворов их галоидных солей. Связывая образующуюся кислоту, она смещает равновесие реакции гидролиза.
Окись этилена и ее гомологи могут присоединять аммиак и амины, давая соединения, относящиеся к аминоспиртам:
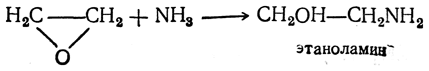
Окись этилена готовится в промышленном масштабе, и на ее основе производятся многочисленные и разнообразные синтезы.


