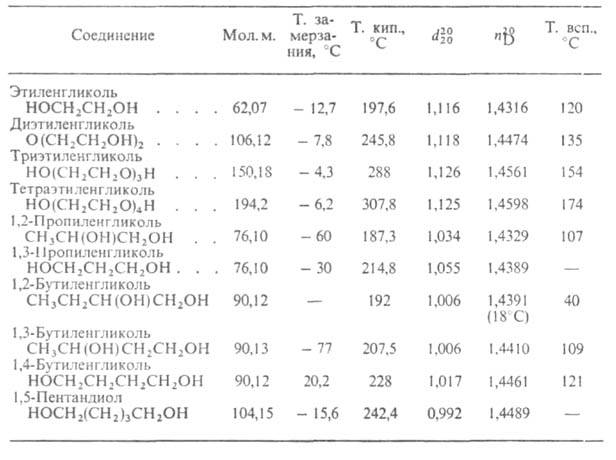
Гликоли
ГЛИКОЛИ (алкандиолы), двухатомные спирты жирного ряда общей ф-лы СnН2n(ОН)2. Группы ОН в молекулах могут находиться у одного атома С (геминальные гликоли), у соседних атомов (вицинальные) и т.д. Названия гликолей производят от названий соответствующих алканов или ал-кенов и соотв. суффиксов "диол" или "гликоль", напр. НОСН2СН2ОН-1,2-этандиол или этиленгликоль, НОСН2СН2СН2ОН-1,3-пропандиол или 1,3-пропиленгликоль (триметиленгликоль).
Наиб, практич. значение имеют этиленгликоль, пропиленгликоли, бутиленгликоли и нек-рые их производные, содержащие одну или более простых эфирных групп в молекуле (т.н. полигликоли, напр. диэтиленгликолъ), высокомолекулярные полиэтиленгликоли (см. Полиэтиленоксид).
Низшие гликоли - бесцв. прозрачные вязкие жидкости (см. табл.) без запаха, имеют сладковатый вкус, гигроскопичны. Наличие в молекуле двух групп ОН обусловливает более высокие плотность, вязкость и т-ру кипения гликолей, чем соответствующих одноатомных спиртов. Геминальные гликоли нестойки, напр. метиленгликоль существует только в водных р-рах.
Низшие гликоли (С2-С7) смешиваются с водой, спиртами, альдегидами, кетонами, к-тами, аминами во всех соотношениях. Гликоли, особенно полигликоли, хорошо растворяют синтетич. смолы, лаки, краски, эфирные масла, каучуки. Ароматич. углеводороды растворяются в гликолях ограниченно, предельные алифатич. углеводороды не растворяются. Благодаря водородным связям гликоли образуют ассоциаты с водой (гидраты), аминами и др. При образовании гидратов значительно понижается т-ра замерзания водных р-ров гликолей. На этом св-ве основано применение их как антифризов.
Гликоли обладают всеми хим. св-вами, характерными для спиртов. Гидроксильные группы гликолей реагируют независимо друг от друга или одновременно (поэтому иногда образуются соответствующие смеси продуктов). Со щелочными металлами и их гидроксидами гликоли образуют гликоляты (напр., NaOCH2CH2ONa), с одноосновными карбоновыми к-тами, их ангидридами или хлорангидридами - сложные моно- и диэфиры, с двухосновными к-тами и их производными-линейные сложные полиэфиры типа [—ORO—(O)CR'C(O)—]n, с низкомол. двухосновными к-тами или их эфирами-циклич. соединения, напр.:
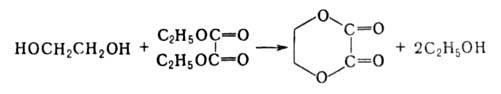
При действии галогеноводородов гликоли легко превращаются в галогенгидрины, напр. при нагр. с НС1 1,2-пропиленгликоля образуется смесь С1СН2СН(ОН)СН3 и НОСН2СН(С1)СН3; однако вторая группа ОН замещается на галоген труднее (лучше - действием РС15 или SOC12).
С альдегидами и кетонами (кат.-FеС13, Н3РО4) гликоли дают циклич. ацетали (1,2-гликоль-1,3-диоксоланы, 1,3-гликоль-1,3-диоксаны), напр.:
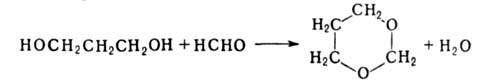
Под действием щелочных катализаторов гликоли реагируют с ацетиленом с образованием виниловых и дивиниловых эфиров: напр.: 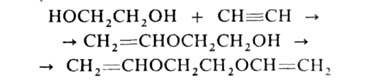
с акрилонитрилом - моно- или бис-цианэтиловых эфиров, напр.: 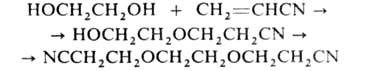
с эпоксидами при 140-180 °С - ди-, три- и полигликолей, напр.: 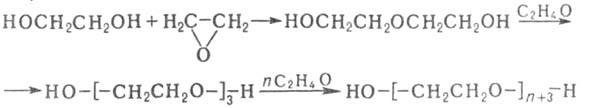
Характер продуктов, образующихся при дегидратации гликолей, определяется взаимным расположением групп ОН в молекуле и условиями р-ции. Так, под действием ZnCl2, разб. H2SO4 при слабом нагревании вициналопые гликоли превращаются в альдегиды или кетоны, напр.: НОСН2СН2ОН -> СН3СНО, 1,2-пропиленгликоль в присут. Н3РО4 на цеолите при 250°С- в осн. в СН3СН2СНО, пипакопы в результате пинаколиновой перегруппировки-в пинаколины. Гликоли (кроме вицинальных) превращаются в ненасыщ. спирты или диены, напр.:
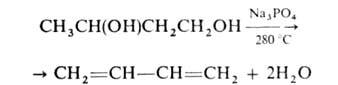
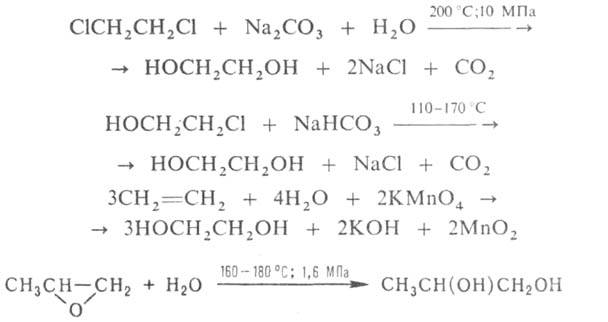
Кислородом гликоли окисляются до пероксидов, формальдегида, ацетона, муравьиной к-ты, сложных эфиров и др.; действием К2Сr2О7 или КМnО4-до СО2 и Н2О. Осн. методы синтеза гликолей:
Гликоли-р-рители, пластификаторы. Они применяются также для приготовления антифризов и гидравлич. жидкостей (этилен- и пропиленгликоли), для синтеза эфиров гликолей, полиэфирных смол, полиуретанов (1,2-пропиленгликоль, 1,4-бутиленгликоль), увлажнения разл. продуктов, напр. табака, казеина, желатины.
Токсичность гликолей убывает с увеличением мол. массы.
Литература
ДыментО.Н., Казанский К.С., Мирошников А. М., Гликоли и другие производные окисей этилена и пропилена, М., 1976; Kirk-Othmer encyclopedia, 2 ed., v. 10, N.Y., 1966. Б. Б. Чесноков.