Свойства
Галоидзамещенные кислоты вступают во все реакции, свойственные карбоновым кислотам. Они образуют соли, сложные эфиры, галоидангидриды, ангидриды, амиды и пр. Введение галоидов в молекулу кислоты увеличивает силу кислоты, как видно из приведенных ниже данных, причем это влияние падает от фтора к иоду:

Кроме того, галоид оказывает тем меньшее влияние на силу кислоты, чем дальше он отстоит от карбоксила в углеродной цепи:
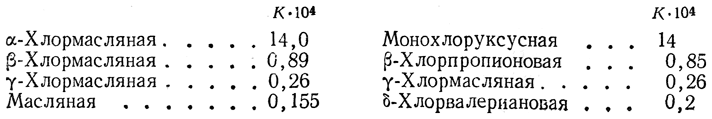
Ионизация карбоновых кислот заключается в обратимом удалении протона — ядра атома водорода — из карбоксильной группы кислоты под влиянием молекулы растворителя (воды):
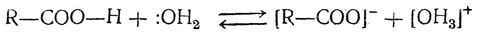
Степень ионизации кислоты будет тем больше, чем слабее связь между протоном и кислотным остатком.
Введение галоида, в частности хлора, в радикал карбоновой кислоты ослабляет связь протона с кислотным остатком, что объясняется полярным характером связи С—Сl в замещенном радикале кислоты. Благодаря этому, например, в хлоруксусной кислоте электронная пара, связывающая атом углерода группы CH2Cl с углеродным атомом карбонильной группы, несколько смещается по направлению к атому хлора. Такое смещение вызывает в свою очередь смещение электронов, связывающих этот атом углерода с кислородным атомом, в результате чего ослабляется связь протона с атомом кислорода:

Последовательное смещение электронной плотности в направлении к электроотрицательному заместителю (отрицательный индукционный эффект) приводит к увеличению силы галоидзамещенных кислот по сравнению с незамещенными.
При многократном замещении водорода галоидом индукционные эффекты не просто суммируются, а взаимно усиливают друг друга (это видно из сравнения констант диссоциации монохлор-, дихлор- и трихлоруксусной кислот).
Индукционное влияние довольно быстро ослабевает вдоль цепи простых связей между углеродными атомами и за пределами четвертого звена углеродной цепи (дальше 6 А) становится уже неощутимым.
Карбоксильная группа в свою очередь влияет на реакционную способность атома галоида, причем это влияние также зависит от положения галоида относительно карбоксила. Так, в α-галоидкислотах атом галоида чрезвычайно склонен к реакциям обмена:
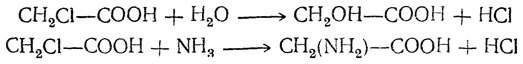
β-Галоидкислоты при кипячении со щелочами в большинстве случаев отщепляют молекулу галоидоводорода с образованием α,β-ненасыщенных кислот:
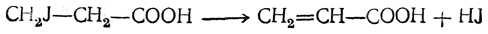
Под действием многих других реагентов от β-галоидкислот также в большинстве случаев отщепляется галоидоводород и лишь отчасти происходит замещение галоида на соответствующий радикал.
γ-Галоидкислоты при кипячении с водой или щелочью также легко отщепляют галоидоводород, но при этом образуются не непредельные кислоты, а циклические сложные эфиры, называемые лактонами:
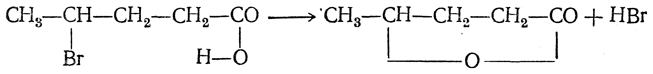
При многочисленных реакциях обмена атомов галоида на другие атомы и радикалы, а также при других реакциях, аналогичных реакциям простейших галоидпроизводных углеводородов, очень часто применяют не сами галоидкислоты, а их сложные эфиры.


