Двойной электрический слой
ДВОЙНОЙ ЭЛЕКТРИЧЕСКИЙ СЛОЙ, тонкий поверхностный слой из пространственно разделенных электрич. зарядов противоположного знака, образующийся на границе двух фаз. Поскольку пространств. разделение зарядов всегда сопровождается возникновением электрич. разности потенциалов, двойной электрический слой можно рассматривать как своеобразный микроконденсатор, расстояние между обкладками к-рого определяется молекулярными размерами. Образование двойного электрического слоя оказывает существенное влияние на скорость электродных процессов, адсорбцию ионов и нейтральных молекул, устойчивость дисперсных систем, смачиваемость, коэф. трения и др. св-ва межфазных границ. В биол. системах процессы образования и разрушения двойного электрического слоя на клеточных мембранах сопровождают распространение электрич. импульсов вдоль нервных и мышечных волокон. Наиб. детально строение двойного электрического слоя изучено на границе между металлич. электродом и р-ром электролита. При погружении металлич. электрода М в р-р электролита, содержащий ионы этого металла М+ (потенциалопределяющие ионы), устанавливается электрохим. равновесие, сопровождаемое выравниванием электрохим. потенциалов этих ионов в кристаллич. решетке металла и в р-ре. Если первоначально электрохим. потенциал ионов М+ в металле 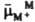 был больше электрохим. потенциала этих ионов в р-ре
был больше электрохим. потенциала этих ионов в р-ре 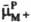 , то в процессе выравнивания этих величин нек-рое кол-во ионов М+ переходит из металла в р-р и пов-сть металла заряжается отрицательно. Притянутые к ней кулоновскими силами катионы из р-ра (не обязательно М+) образуют положит. обкладку двойного электрического слоя. Возникающая при этом электрич. разность потенциалов препятствует дальнейшему переходу ионов М+ из металла в р-р, что и приводит к установлению электрохим. равновесия. Если первоначально
, то в процессе выравнивания этих величин нек-рое кол-во ионов М+ переходит из металла в р-р и пов-сть металла заряжается отрицательно. Притянутые к ней кулоновскими силами катионы из р-ра (не обязательно М+) образуют положит. обкладку двойного электрического слоя. Возникающая при этом электрич. разность потенциалов препятствует дальнейшему переходу ионов М+ из металла в р-р, что и приводит к установлению электрохим. равновесия. Если первоначально 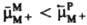 , то при установлении электрохим. равновесия часть ионов М+ из р-ра переходит на металл, заряжая его пов-сть положительно. Отрицат. обкладку двойного электрического слоя в этом случае составляют притянутые к пов-сти металла анионы р-ра. Путем подбора концентрации потенциалопределяющих ионов в р-ре можно добиться такой ситуации, что условие
, то при установлении электрохим. равновесия часть ионов М+ из р-ра переходит на металл, заряжая его пов-сть положительно. Отрицат. обкладку двойного электрического слоя в этом случае составляют притянутые к пов-сти металла анионы р-ра. Путем подбора концентрации потенциалопределяющих ионов в р-ре можно добиться такой ситуации, что условие 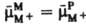 не требует перехода ионов М+ из металла в р-р или наоборот. В этом случае заряд пов-сти металла равен нулю, а его потенциал, измеренный относительно к.-л. электрода сравнения, наз. потенциалом нулевого заряда. Условия положительно заряженной, отрицательно заряженной и незаряженной пов-сти металла можно осуществить и в том случае, если в р-ре электролита нет потенциалопределяющих ионов.
не требует перехода ионов М+ из металла в р-р или наоборот. В этом случае заряд пов-сти металла равен нулю, а его потенциал, измеренный относительно к.-л. электрода сравнения, наз. потенциалом нулевого заряда. Условия положительно заряженной, отрицательно заряженной и незаряженной пов-сти металла можно осуществить и в том случае, если в р-ре электролита нет потенциалопределяющих ионов.
Методы изучения. Для исследования двойного электрического слоя используют в осн. три группы методов. Во-первых, адсорбц. методы, к-рые основаны на том, что образование двойного электрического слоя связано с адсорбцией разл. компонентов р-ра и вызывает изменение их концентрации. В частности, адсорбц. методы широко используют для изучения двойного электрического слоя, образованного на мелкодисперсных частицах в коллоидных системах. Во-вторых, методы, основанные на электрокапиллярных явлениях. Их сущность состоит в том, что образование двойного электрического слоя уменьшает работу, необходимую для создания новой пов-сти раздела фаз, и тем самым приводит к зависимости межфазного натяжения от потенциала электрода. Применение электрокапиллярных методов ограничено границами раздела между жидкими фазами, на к-рых возможно непосредственное измерение межфазного натяжения; для твердых электродов эти методы дают лишь качеств. информацию о строении двойного электрического слоя. В-третьих, методы, регистрирующие кол-во электричества, затраченного на создание определенного заряда электрода (заряжение двойного электрического слоя). Сюда относятся разл. гальваностатич. и потенциостатич. импульсные методы, а также метод измерения электрич. емкости двойного электрического слоя с помощью синусоидального переменного тока (см. Импедансный метод). Для успешного применения этих методов необходимо, чтобы все подведенное к электроду электричество затрачивалось только на заряжение двойного электрического слоя и не расходовалось на электрохим. р-ции. Электроды, удовлетворяющие этому требованию, наз. идеально поляризуемыми. Сведения о строении двойного электрического слоя на границе р-р|изолятор можно получить на основе изучения электрокинетических явлений. Двойной электрический слой изучают также с помощью оптич. методов (эллипсометрия, разл. варианты электроотражения света, комбинационное рассеяние в адсорбц. слое и др.). На основе указанных методов можно определить заряд пов-сти электрода q, его зависимость от потенциала электрода Е, потенциал нулевого заряда Eq = 0, электрич. емкость двойного электрического слоя, равную дq/дE, а также поверхностные избытки (адсорбции) разл. компонентов р-ра в зависимости от Е (или q)и их объемной концентрации.
Современная теория двойного электрического слоя, основной вклад в развитие к-рой внесли работы Г. Гелъмгольца (1879), Ж. Гуи (1910), Д. Чапмена (1913), О. Штерна (1924) и Д. Грэма (1947-58), базируется на след. модели ионной обкладки двойного электрического слоя. Благодаря тепловому движению ионы, адсорбировавшиеся на электроде только под действием кулоновских сил, распределяются у пов-сти подобно молекулам газа в земной атмосфере и образуют диффузную часть двойного электрического слоя. Границей диффузной части является т. наз. внеш. плоскость Гелъмгольца х2 (рис.), до к-рой могут дойти электрич. центры ионов, участвующих в тепловом движении. Между внеш. плоскостью Гельмголъца и пов-стью металла располагается плотная часть двойного электрического слоя, для к-рой характерна диэлектрич. проницаемость существенно меньшая, чем в объеме р-ра. В плотном слое локализуется дипольный двойной электрический слой, образованный ориентированными диполями р-рителя и орг. растворенного в-ва. Кроме того, в плотную часть двойного электрического слоя входят специфически адсорбирующиеся ионы; при этом их электрич. центры образуют т. наз. внутр. плоскость Гельмголъца х1.
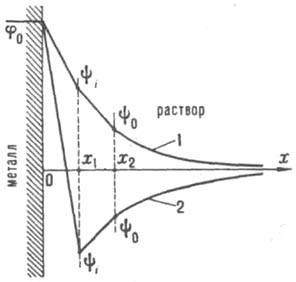
Схема распределения потенциала в двойном электрическом слое: 1 - при |q1| < |q|; 2 - при |q1| > |q|
В силу электронейтральности границы раздела плотность заряда q на электроде компенсируется зарядами специфически адсорбиров. ионов (q1) и ионов, находящихся в диффузной части двойного электрического слоя (q2): q= -q1-q2. Теория двойного электрического слоя позволяет связать величины q и q1, с электрич. разностями потенциала в плотной и диффузной частях двойного электрического слоя. Так, падение потенциала в плотной части двойного электрического слоя описывается ур-нием: yu = q/K02 + q1К12, где К02 и Kl2 - интегральные емкости соотв. всего плотного слоя и пространства между внутр. и внеш. плоскостями Гельмгольца. Падение потенциала в диффузном слое (потенциал внеш. плоскости Гельмгольца) в р-ре 1,1-валентного электролита с концентрацией с равно: 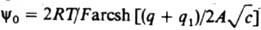 , где
, где 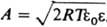 , e0 - диэлектрич. постоянная, e - диэлектрич. проницаемость р-рителя, a R, Т и F - соотв. газовая постоянная, т-ра и число Фарадея. Потенциал внутр. плоскости Гелъмгольца рассчитывают по ф-ле: yi = (q + lq1)/Kl2 + y0, где l [ 1 - коэф., характеризующий дискретность специфически адсорбиров. ионов. Если |q1| > |q|, то говорят, что произошла "перезарядка поверхности" специфически адсорбиров. ионами. В этом случае потенциалы y0 и yi, имеют знак, противоположный знаку общего скачка потенциала в ионном двойном электрическом слое j0 = yu + y0 (см. рис., кривая 2). Для развития теории дипольного двойного электрического слоя, связанного с адсорбцией молекул р-рителя, успешно используется зависимость емкости К02 от q. Теоретич. расчеты электронного двойного электрического слоя пока крайне противоречивы; с целью упрощения принято считать, что скачок потенциала в электронном двойном электрическом слое металла не зависит от q и потому не вносит вклада в наблюдаемые эффекты. Изучение св-в и строения двойного электрического слоя имеет большое значение для понимания и усовершенствования таких практически важных процессов, как электролиз, электроосаждение металлов, электрохим. р-ции в хим. источниках тока, коррозия металлов, коагуляция в коллоидных системах, флотация, ионный обмен и др.
, e0 - диэлектрич. постоянная, e - диэлектрич. проницаемость р-рителя, a R, Т и F - соотв. газовая постоянная, т-ра и число Фарадея. Потенциал внутр. плоскости Гелъмгольца рассчитывают по ф-ле: yi = (q + lq1)/Kl2 + y0, где l [ 1 - коэф., характеризующий дискретность специфически адсорбиров. ионов. Если |q1| > |q|, то говорят, что произошла "перезарядка поверхности" специфически адсорбиров. ионами. В этом случае потенциалы y0 и yi, имеют знак, противоположный знаку общего скачка потенциала в ионном двойном электрическом слое j0 = yu + y0 (см. рис., кривая 2). Для развития теории дипольного двойного электрического слоя, связанного с адсорбцией молекул р-рителя, успешно используется зависимость емкости К02 от q. Теоретич. расчеты электронного двойного электрического слоя пока крайне противоречивы; с целью упрощения принято считать, что скачок потенциала в электронном двойном электрическом слое металла не зависит от q и потому не вносит вклада в наблюдаемые эффекты. Изучение св-в и строения двойного электрического слоя имеет большое значение для понимания и усовершенствования таких практически важных процессов, как электролиз, электроосаждение металлов, электрохим. р-ции в хим. источниках тока, коррозия металлов, коагуляция в коллоидных системах, флотация, ионный обмен и др. Литература
