Аллены
АЛЛЕНЫ (1,2-диены), соединения общей ф-лы RR'C=C=CR"R'", где R, R', R", R'"-H, Alk, Аг, остаток гетероцикла или к.-л. функц. группа. Первый член ряда- аллен СН2=С=СН2: бесцв. газ; т.пл. -136,2°С, т.кип. -34,5°С; КПВ 1,7-10%. 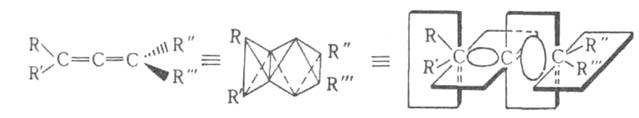
Структурные модели хирального аллена.
Квантовомех. модель кумулированных двойных связей в алленах предусматривает sp2-электронное состояние для обоих крайних атомов С. Центр. атом С имеет sp-гибридизацию. Поэтому вся исходящая от него система связей линейна; обе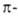 связи и концевые заместители расположены во взаимно перпендикулярных плоскостях (см. рис.). Вследствие этого взаимное влияние заместителей минимально, а при несимметричном замещении аллены существуют в виде энантиомеров. Это положение было предсказано еще Я. Вант-Гоффом; впоследствии оно было подтверждено расщеплением алленов на оптич. антиподы, синтезом оптически активных алленов с использованием хиральных реагентов или оптически активных исходных соединений, напр.:
связи и концевые заместители расположены во взаимно перпендикулярных плоскостях (см. рис.). Вследствие этого взаимное влияние заместителей минимально, а при несимметричном замещении аллены существуют в виде энантиомеров. Это положение было предсказано еще Я. Вант-Гоффом; впоследствии оно было подтверждено расщеплением алленов на оптич. антиподы, синтезом оптически активных алленов с использованием хиральных реагентов или оптически активных исходных соединений, напр.:
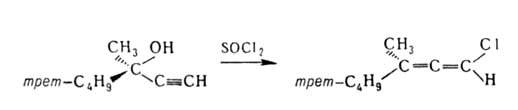
Электроф. и радикальное присоединения к алленам происходят легче, чем к олефинам, из-за наличия двух соседних связей С=С; при этом образуются винильные или аллильные структуры, напр.:
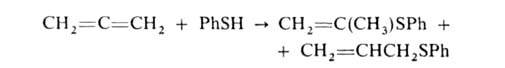
Под действием к-т или щелочей алленовая связь может перейти в ацетиленовую или 1,3-диеновую (прототропная изомеризация): 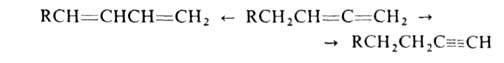
Аллены способны полимеризоваться с образованием смеси гомологов (от ди- до гексамеров); при димеризации получаются производные циклобутана. Аллены вступают в циклопри-соединение и с др. соед., имеющими кратные связи, напр.:
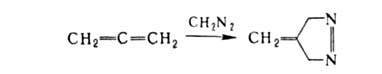
Алленовые группировки, сопряженные с электроноакцепторными группами, легко присоединяют по кратной связи нуклеофилы (YH): 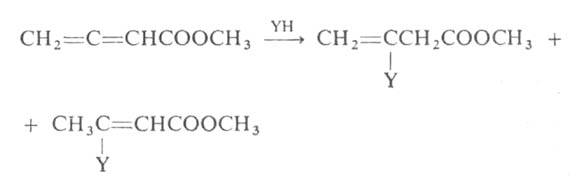
Важнейшие способы получения алленов:
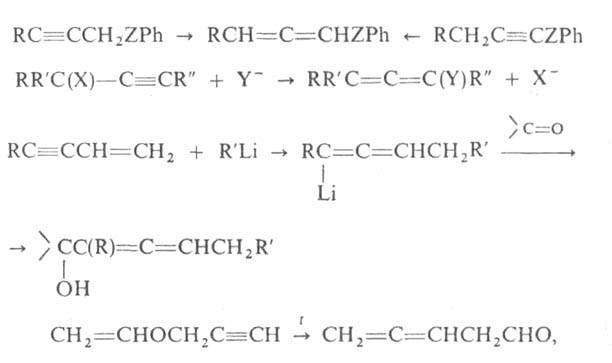
где X и Y-OH, Hal, OSO2R'"; Z = О, S, Se.
Кроме того, аллены можно синтезировать теми же способами, что и соединения с одной двойной связью: дегалогенированием, дегидрогалогенированием, дегидратацией, а также пиролизом енолфосфатов: 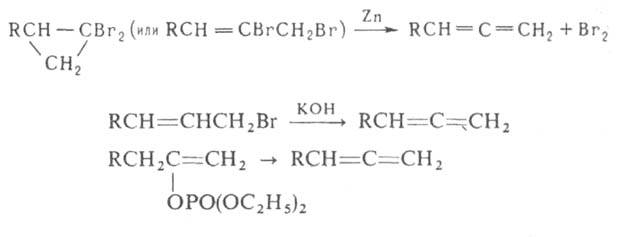
Аллены широко применяют в орг. синтезе. Они являются промежут. продуктами при получении простагландинов, феромонов, витаминов, лек. препаратов и др. Аллены обнаружены среди метаболитов низших грибов, высших растений, а также продуктов жизнедеятельности морских гидробионтов и насекомых.
Лит.. МавровМ. В., Кучеров В. Ф., в кн.. Реакции и методы исследования органических соединений, кн. 21, М., 1970, с. 90-316; Кучеров В. Ф., Мавров М.В., Держинский А. Р.. Природные полиацетиленовые соединения, М., 1972, гл. 5;Табер А. М., Калечиц И. В., Аллен, М., 1975; Мавров М. В., "Успехи химии", 1982, т. 51, в. 9, с. 1541-66: The chemistry of ketenes, allenes and related compounds, ed. S. Patai, v. 1-2, N. Y., 1980. М. В. Мавров.
