Эргоалкалоиды
ЭРГОАЛКАЛОИДЫ, индольные алкалоиды, выделенные из "ergot" - высушенной зрелой формы (склероции) гриба спорыньи (Claviceps purpurea) семейства Hypocreaceae. Спорынья паразитирует на ржи, др. злаках и ряде дикорастущих трав. Эргоалкалоиды обнаружены также в грибах родов Aspergillus, Penicillium и др., а также в растениях семейства вьюнковых (Соn volvulaceae). Из разных источников получают разл. типы эргоалкалоидов.
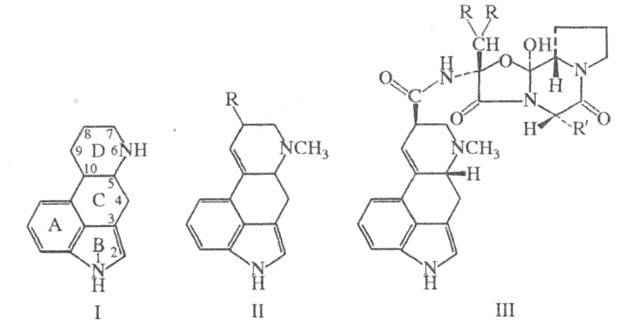
Эргоалкалоиды включают более 60 представителей. Большинство из них - производные эрголина (ф-ла I). Различают две осн. группы эргоалкалоидов. К первой относятся амиды лизергиновой к-ты (II; R = СООН), выделенные из грибов, паразитирующих на злаках. Эта группа включает растворимые в воде алкалоиды, в частности эргоновин [эргометрин; ф-ла II; R = C(O)NHCH(CH3)CH2OH], и т. наз. пептидные эргоалкалоиды, нерастворимые в воде. Примеры последних - эрготамин (III; R = Н, R' = СН2С6Н5), эргокристин (III; R = СН3, R' = СН2С6Н5), эргокорнин [III; R = CH3, R'= CH(CH3)2], эргокриптин [III; R = CH3, R' = СН2СН(СН3)2].
При выделении эргоалкалоидов первой группы из свежеприготовленного сырья в мягких условиях получают фармакологически высокоактивные производные лизергиновой к-ты, к-рые, как правило, левовращающие. Использование лежалого сырья или жестких условий выделения приводит к диастереомерам (по атому С-8), к-рые являются правовращающими и фармакологически малоактивны. Называют их, используя окончание "инин", напр. малоактивный изомер эргокристина - эргокристинин. В щелочной среде наблюдается взаимопревращение диастереомеров.
Вторая группа включает эргоалкалоиды клавинового типа, к-рые специфичны для грибов, паразитирующих на дикорастущих травах, реже - на ржи, а также высш. растениях. Клавиновые эргоалкалоиды- производные лизергола (II; R = СН2ОН) или лизергина (II; R = CH3). К ним относятся, в частности, элимоклавин (IV), пенниклавин (V), изофумигаклавин-А (VI), циклоклавин (VII), ханоклавин-I (VIII).
Нек-рые грибы продуцируют эргоалкалоиды необычного строения, к-рые не относятся ни к одной из названных групп. Так, из Penicillium concavo-rugulosum выделен (наряду с VIII) ругуловазин-А (IX), а из Penicillium rogueforti - рокефортин (X) в смеси с VI.
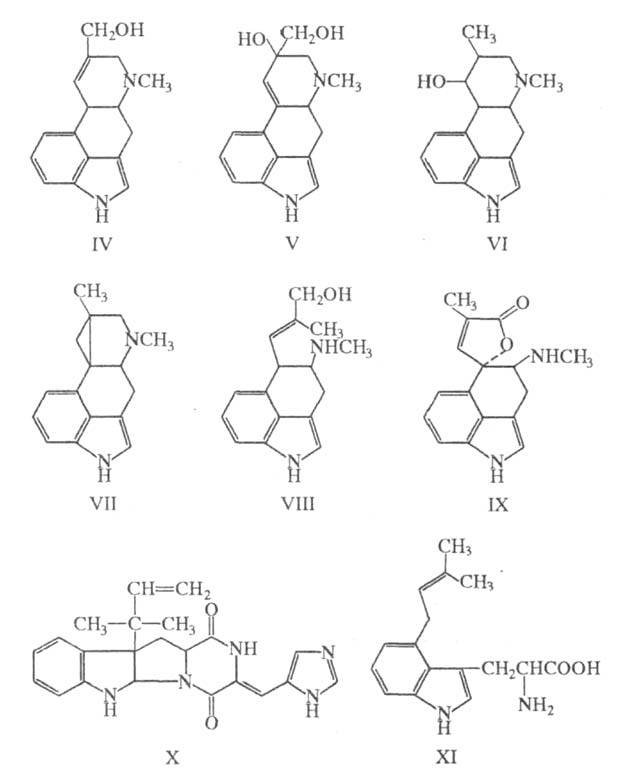
Строение эргоалкалоидов устанавливали по продуктам гидролиза и окисления, а также в результате их исследований методами спектрального и рентгеноструктурного анализа. Многие эргоалкалоиды синтезированы.
Биогенетич. предшественник эргоалкалоидов - триптофан. Из культуры Claviceps fusiformis выделено N-метильное производное образующегося в ходе биосинтеза 4-(3-метил-2-бутенил) триптофана (XI). Дальнейшие превращения последнего приводят к клавиновым алкалоидам и лизергиновой к-те, к-рая взаимод. с пептидами, одновременно образующимися из соответствующих аминокислот.
В пром-сти эргоалкалоиды получают из склероции спорыньи (содержащей до 0,3% алкалоидов) или синтетически. Для определения эргоалкалоидов используют р-ции, приводящие к образованию окрашенных соед., напр. с n-диметиламинобензальдегидом в сернокислом р-ре эргоалкалоиды дают характерное голубое окрашивание.
Массовые заболевания (эпилептич. конвульсии, гангрена конечностей), вызванные употреблением в пищу зараженного спорыньей зерна, были известны еще в средние века. Спектр фармакологич. действия эргоалкалоидов и их производных чрезвычайно широк. Среди них встречаются антагонисты адреналина, серотонина, ингибиторы пролактина. В медицине эргоалкалоиды применяются как маточные и успокаивающие средства, а также как средства против тахикардии, мигрени, аллергии, гипертонии. Эргоновин (в виде соли малеиновой к-ты) останавливает послеродовые кровотечения. Эрготоксин - смесь эргокристина, эргокорнина и эргокриптина - обладает сильным симпатолитич. действием. Дигидроэрготоксин - смесь соответствующих 9,10-дигидропроизводных - применяется при лечении сосудистых заболеваний. Лизергиновой кислоты диэтиламид - один из самых сильных галлюциногенов.
Лит.: Stо11 А., Ноfmann А., в кн.: The Alkaloids, ed. by R. H. F. Manske, v. 8.N.Y., 1965, p. 725-83; Stadler P. A., Stutz P., в кн.: The Alkaloids, ed. by R. H. F. Manske, v. 15, N. Y., 1975, p. 1-40).
A A. Ибрагимов.
