Способы получения более сложных циклопептидов
Сложные циклопептиды получаются значительно труднее, чем циклодипептиды. Наиболее распространенный способ их получения состоит в обработке циклизуемого пептида дициклогексилкарбодиимидом. При этом одновременно протекают две конкурирующие реакции — циклизация пептида
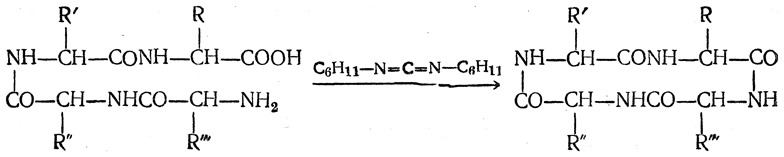
и образование смеси линейных пептидов за счет соединения нескольких молекул исходного пептида друг с другом. Чтобы подавить эту нежелательную реакцию, циклизацию ведут в очень разбавленных растворах, используя прием, разработанный для получения макроциклических соединений алифатического ряда.
Образование циклов может происходить не только за счет образования новой пептидной связи, но и другими способами, например путем образования дисульфидной связи:
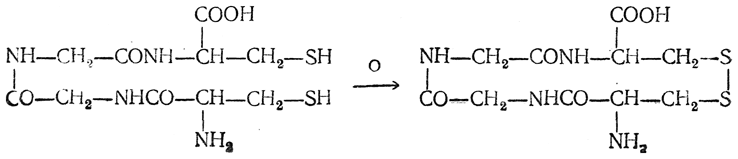
Структурные формулы сложных пептидов, как видно из приведенной схемы синтеза брадикинина, очень громоздки и неудобны. Поэтому принято пользоваться сокращенной записью формул, в которой аминокислотные остатки обозначаются несколькими буквами, происходящими от тривиальных названий аминокислот. Обозначения, принятые в советской химической литературе, приведены в табл. 33. В зарубежной литературе аминокислоты обозначают первыми тремя латинскими буквами их названия.
В сокращенных формулах принято, что аминокислота, записанная слева, ацилирует последующую аминокислоту, записанную справа, например фрагмент пептидной цепи
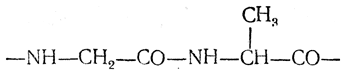
записывается следующим образом:
—глиц—ал—
Сокращенное наименование обозначает остаток аминокислоты, входящий в пептидную цепь, поэтому N-концевая аминокислота записывается Н—глиц-, а С-концевая — глиц—ОН. С-Концевая аминокислота в форме амида изображается сокращенно глиц-NН2, а для остатков амидов дикарбоновых аминокислот (например, глутамина, аспарагина) над или под сокращенным названием аминокислоты ставят символ NH2:

Остаток цистеина со свободной сульфгидрильной группой обозначают цис—SH, остаток цистина: цис—S—S—цис. Формула брадикинина в сокращенной записи имеет вид:
Н—арг—прол—прол—глиц—фал—сер—прол—фал—арг—ОН


