Енолы
Енолы, органические соединения, содержащие гидроксильную группу ОН при углерод-углеродной двойной связи. Простейший енол — виниловый спирт CH2 = CHOH, который, как и большинство енолов, неустойчив в свободном состоянии и превращается в изомерный ацетальдегид:
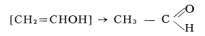
Неустойчивость енолов объясняется тем, что они находятся в таутомерном равновесии с соответствующими карбонильными соединениями:
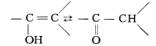
(см. Таутомерия). Поскольку карбонильная форма энергетически выгоднее енольной [на 54—71 кдж/моль (13—17 ккал/моль)], равновесие, как правило, смещено в сторону образования альдегидов и кетонов. Так, содержание енола в ацетоне 2,5-10-4%, в циклогексаноне 2,5-10-4%. Однако в отдельных случаях енольная форма становится устойчивой (например, у b-дикетонов, b-кетоальдегидов, циклических a-дикетонов и др.), т. к. разница в энергии компенсируется энергетическим выигрышем вследствие образования системы сопряжённых связей, а также водородной связи благодаря возникновению гидроксильной группы. Содержание енолов в равновесной смеси зависит также от растворителя, температуры и др. факторов.

Дополнения к описанию енолов:
Ключевые химические свойства:
Практическое применение:
Механизм таутомерии:
Стабильные енолы: