Таутомерия
Таутомерия (от греч. tautós — тот же самый и méros — доля, часть), быстрая обратимая структурная изомеризация; способные к таутомерии вещества при установившемся равновесии представляют собой смеси двух (или нескольких) взаимопревращающихся изомеров — таутомеров (см. Изомерия). Наиболее распространена прототропная триадная таутомерия (миграция протона между крайними атомами триады — системы трёх атомов, два из которых связаны двойной связью; миграция сопровождается перемещением двойной связи). К этому виду таутомерии относятся кето-енольная (а), имино-енаминная (б), амидная (в), в том числе лактим-лактамная (г), трёхуглеродная (д), кольчато-цепная (е) и некоторые др.:
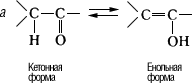
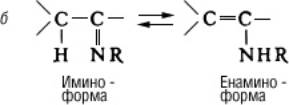
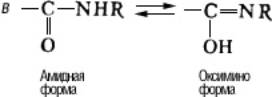
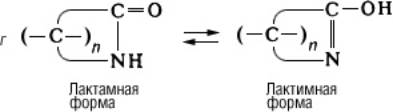
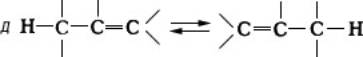
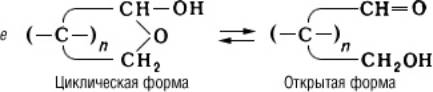
К диадной прототропной таутомерии (миграция протона в системе двух атомов) относят таутомерию синильной кислоты, кислот и тиокислот фосфора (этот тип таутомерии сопряжён с изменением валентности одного из атомов диады):
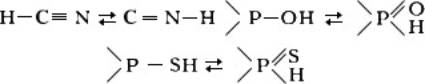
Анионотропная таутомерия (миграция отрицательно заряженного атома или группы атомов) наблюдается в ряду аллилгало-генидов, аллиловых спиртов и их производных:
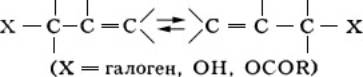
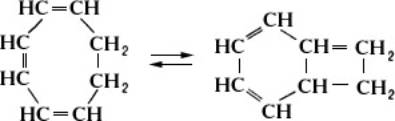
В таутомерных отношениях могут находиться также валентные изомеры, то есть изомеры, превращающиеся друг в друга путём перераспределения валентностей между атомами скелета молекулы, без миграции заместителей, например циклооктатриен существует в равновесии с бициклическим изомером:
В некоторых случаях таутомеры могут быть выделены в индивидуальном состоянии. В большинстве случаев (HCN и т. п.) наличие таутомеров доказывается спектральными методами.
Многие вещества образуют два ряда производных, соответствующих двум возможным таутомерным формам, что, однако, как правило, связано не с таутомерией, а с двойственной реакционной способностью (см. Мезомерия). Таутомерия предполагает реальное существование таутомеров, что в каждом случае требует доказательства.
Лит.: Ингольд К., Теоретические основы органической химии, пер. с англ., М., 1973, с. 658.
Б. Л. Дяткин.
