Гипофосфиты неорганические
ГИПОФОСФИТЫ НЕОРГАНИЧЕСКИЕ [диоксофосфаты(V)], соли фосфорноватистой к-ты Н3РО2. За исключением К2НРО2 имеют общую ф-лу М(Н2РО2)n, где n-степень окисления металла М. Гипофосфиты -кристаллы; при нагр. диспропорционируют с образованием Н2, красного Р, РН3, Р2Н6, фосфитов, дифосфитов и фосфатов. Гипофосфиты щелочных и щел.-зем. металлов хорошо раств. в воде (рН р-ров ок. 7), хуже - в этаноле. Гипофосфиты металлов в степени окисления + 3 малорастворимы в воде. Гипофосфиты образуют кристаллогидраты. Являются восстановителями. Получают их взаимод. Н3РО2 с гидроксидами или карбонатами металлов, гипофосфиты щелочных и щел.-зем. металле в - также р-цией красного Р с гидроксидами; К2НРО2 синтезируют взаимод. KNH2 с КН2РО2 в жидком NH3.
Наиб. практич. значение имеет НаН2РО2 - бесцв. кристаллы; разлагается выше 200 °С. Р-римость в воде 50% по массе; раств. в этаноле и этиленгликоле. Образует моногидрат (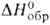 —842,6 кДж/моль). Получают взаимод. РН3 с NaCIO или Р с NaOH. Восстановитель при нанесении покрытий из Ni, Co, Sn на металлы и пластмассы; антиоксидант (предотвращает обесцвечивание алкидных смол при их получении); стабилизатор ПВХ и полиуретанов; реагент для фотометрич. определения As(III) и Sb(III).
—842,6 кДж/моль). Получают взаимод. РН3 с NaCIO или Р с NaOH. Восстановитель при нанесении покрытий из Ni, Co, Sn на металлы и пластмассы; антиоксидант (предотвращает обесцвечивание алкидных смол при их получении); стабилизатор ПВХ и полиуретанов; реагент для фотометрич. определения As(III) и Sb(III).
Литература
Comprehensive inorganic chemistry, ed. by A.F. Trotman-Dickenson, v. 2, Oxf.-[a.o.], 1975. , , П.П.Мельников.

Дополнения к описанию гипофосфитов неорганических: