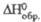Фосфиды
ФОСФИДЫ, соединения фосфора с более электроположит. элементами. По типу хим. связи фосфиды подразделяют на соед. с преим. ионной связью, металлоподобные и с преим. ковален-тной связью. К ионным относятся фосфиды щелочных и щел.-зем. элементов и металлов подгруппы цинка. Эти фосфиды легко гидролизуются водой, хорошо раств. в к-тах с выделением PH3, сгорают в токе O2 с образованием оксидов металлов и P, реагируют с галогенами. Нек-рые из них обладают полупроводниковыми св-вами из-за того, что в межатомной связи присутствует определенная доля ковалентной составляющей. Металлоподобные фосфиды образуют гл. обр. переходные металлы, в т. ч. РЗЭ. Их состав, как правило, не соответствует валентностям образующих их элементов. Эти фосфиды тугоплавки, устойчивы к действию воды и K-T. Их хим. стойкость растет с увеличением содержания P. Так, Ni3P, Cr3P, Fe3P, Ti3P легко разлагаются к-тами-окислителями (H2SO4, HNO3, HClO4), а также щелочами. В то же время фосфиды состава TiP, VP, TaP, CrP, FeP, MnP не взаимод. с конц. соляной к-той и к-тами-окислителями. Они раств. при нагр. в царской водке. Все металлоподобные фосфиды разлагаются смесью HF и HNO3 и при сплав-лении с щелочами и пероксидами металлов. Многие из них -полупроводники благодаря тому, что в хим. связь вносит определенный вклад ковалентная составляющая.
Ковалентные фосфиды образуются непереходными элементами III и IV гр. периодич. системы (кроме Tl). Они тугоплавки, их хим. стойкость к воде и др. агрессивным средам сильно зависит от чистоты образца. Особенно устойчивы высоко чистые в-ва. Все твердые ковалентные фосфиды- полупроводники, ширина запрещенной зоны к-рых тем больше, чем выше доля ионной связи в них. Типичные полупроводниковые фосфиды этой группы представляют собой координац. соед., в к-рых помимо простых ковалентных связей присутствуют донор-но-акцепторные связи. При этом атом P - донор, а атомы более электроположит. элемента - акцепторы электронной пары.
Фосфиды полуметаллов и неметаллов также гл. обр. ковалентные соед. Они м. б. газами (напр., PH3), твердыми в-вами; по электрофиз. св-вам - диэлектриками или полупроводниками. Типичный диэлектрик - BP. Он устойчив к действию к-т-окислителей и щелочей. Другие фосфиды этой группы, напр. AlP и SiP, не обладают большой стойкостью к действию хим. реагентов.
Св-ва нек-рых фосфидов представлены в табл. Фосфиды активных металлов - солеобразные в-ва, фосфиды металлов подгруппы Zn, у к-рых полностью заполнены (п — 1)d-орбитали,- полупроводники. В случае переходных металлов с незаполненными полностью (п— 1)d-орбиталями фосфиды могут быть как полупроводниками, так и металлоподобными. Для последних характерно относительно меньшее содержание P в формульной единице. При этом ферромагн. металлы могут образовывать и ферромагн. фосфиды, напр. Fe3P и CoP. Типичные полупроводники - фосфиды элементов групп Ша и IVa (GaP, InP, SiP, GeP).
| СВОЙСТВА НЕКОТОРЫХ ФОСФИДОВ | ||||||
| Соединение | Сингония | T. пл., 0C | кДж/моль | Ширина запрещенной зоны, эВ | ||
| K3Pа.. ...... | Гексагон. | Разлагается | — | — | ||
| Mg3Pа...... | Кубич. | Разлагается | -254,3 | — | ||
| Zi3P2б....... | Тетрагон. | 883 | -194,9 | 1,15 | ||
| Cd3P2б...... | " | 739 | -155,2 | 0,58 | ||
| Cu3Pв. | Гексагон. | 1022 | -150,6 | — | ||
| CuP2б....... | Моноклинная | 891 | -121,3 | 1,4 | ||
| BPг......... | Кубич. | 2250 | -395,7 | 4,5 | ||
| GaPб ....... | " | 1465 | -102,5 | 2,25 | ||
| InPб . | " | 1062 | -84,5 | 1,28 | ||
| SiPб. ........ | Ромбич. | 1170 | -79,1 | 2,4 | ||
| GePб........ | Моноклинная | 725 | -175,4 | 1,0 | ||
| TiPв. ........ | Гексагон. | 1990е | -282,8 | — | ||
| Cr3Pв. ....... | Тетрагон. | 1510 | — | — | ||
| CrPб........ | Ромбич. | 1600 | — | 0,8 | ||
| MnPб | " | 1147е | — | 1,1 | ||
| Mn3Pв. ...... | Тетрагон. | 1105 | — | — | ||
| FePб........ | Ромбич. | — | -121,3 | 1,0 | ||
| Fe3Pд ....... | Тетрагон. | 1166е | -164,0 | — | ||
| CoPд | Ромбич. | 1520 | -146,4 | — | ||
| Co2Pв....... | " | 1386 | -196,2 | — | ||
| Ni3Pв ....... | Тетрагон. | 1025 | -219,2 | — | ||
| Ni2Pв ....... | Гексагон. | 1106 | -184,1 | — | ||
| ZnGeP2 б ..... | Тетрагон. | 1250 | — | 2,2 | ||
| CdSiP2б..... | " | 1200 | — | 1,8 | ||
а Солеобразен. б Полупроводник. в Металлоподобен.г Диэлектрик. д Ферромагнетик. е С разложением.
Осн. метод получения фосфидов- синтез из простых в-в в вакууме, атмосфере инертного газа или под давлением паров P. Можно также получать фосфиды взаимод. PH3 с металлами или их оксидами, карботермич. восстановлением фосфатов, обменной фосфи-дизацией (р-ция металла или его хлорида с др. фосфидом) и т. д. Наиб. практич. применение нашли галлия фосфид и индия фосфид как полупроводниковые и оптоэлектронные материалы. SiP используют для легирования монокристаллов Si. Перспективные полупроводниковые материалы - тройные фосфиды, напр. ZnSiP2, CdGeP2. Соед. Cu3P применяют как раскислитель в произ-ве бронз, для пайки латуни вместо серебряного припоя.
Zn3P2 и Cu3P - полупроводниковые материалы, Zn3P2 - также зооцид. Фосфиды железа и Ni употребляют для создания износостойких покрытий на деталях машин. Благодаря самопроизвольному выделению горючих фосфинов во влажном воздухе Mg3P2 и Ca3P2 являются компонентами спец. сигнальных устройств и пиротехн. составов. Фосфиды токсичны из-за выделения PH3.
ПДК для Cu3P 0,5 мг/м3, для Zn3P2 0,1 мг/м3.
Лит.: Самсонов Г.В., Верейкина Л.Л., Фосфиды, К., 1961; Кри-сталлохимические, физико-химические и физические свойства полупроводниковых веществ. Справочник, M., 1973; Угай Я. А., Введение в химию полупроводников, 2 изд., M., 1975; Гончаров E. Г., Полупроводниковые фосфиды и арсениды кремния и германия, Воронеж, 1989. Я. А. Угай.