§4. Подгруппа цинка
По распространенности в природе цинк и его аналоги стоят далеко позади соответствующих элементов подгруппы кальция. Содержание цинка в земной коре оценивается в 0,001%, кадмия 8·10–6 % и ртути – 6·10–7 %.
Все три элемента встречаются преимущественно в виде сернистых соединений типа ЭS. Важнейшими рудами цинка и ртути являются минералы цинковая обманка (ZnS) и киноварь (HgS). Аналогичный им природный сульфид кадмия – минерал гринокит (CdS)–самостоятельно встречается крайне редко. Напротив, небольшие количества CdS почти всегда содержатся в цинковой обманке. Важной рудой цинка является также минерал галмей (ZnСО3 ). Минералы цинка очень часто встречаются совместно со свинцовыми и серебряными. В состав большинства подобных полиметаллических (содержащих несколько металлов) руд входит также и кадмий.
Процесс получения элементарного цинка из руд проводится в две стадии. Сначала обжигом на воздухе переводят сульфид в окись, а затем восстанавливают ее углем:
2ZnS + ЗО2 = 2SO2 + 2ZnO
и
ZnO + С = СО + Zn
Образующиеся по второй реакции пары цинка увлекаются током СО и сгущаются в конденсаторах. Однако часть их уносится далее и оседает затем в виде тонкого порошка. Основная масса последнего подвергается повторной переработке, частично же он поступает в продажу под названием цинковой пыли.
Для выделения цинка часто пользуются также электролизом. В этом случае полученную путем окислительного обжига руды ZnO обрабатывают серной кислотой. Образующийся раствор ZnSO4 и служит электролитом, из которого затем осаждают цинк.
Вследствие большей летучести кадмия по сравнению с цинком он накапливается в цинковой пыли. Последнюю растворяют в H2 SO4 и на раствор действуют металлическим цинком. При этом по схеме
Cd2+ + Zn = Zn2+ Cd
происходит выделение кадмия.
Ввиду нестойкости HgO при высоких температурах получение металлическей ртути сводится к одной реакции:
HgS + O2 = SO2 + Hg
Выделяющиеся пары ртути улавливают в специальных приемниках, где они и сжижаются.
Элементы подгруппы цинка представляют собой белые металлы с синеватым (Zn) или серебристым (Cg, Hd) оттенком. На влажном воздухе они покрываются пленками окислов и теряют свой блеск. Все три металла (особенно ртуть) легкоплавки. Их важнейшие константы сопоставлены в приводимой таблице.
В противоположность ковкому и тягучему кадмию цинк при обычных условиях довольно хрупок. Все три элемента легко образуют сплавы друг с другом и– многими другими металлами. Не сколько особое место среди них занимают сплавы ртути (т. н. амальгамы), многие из которых жидки или тестообразны.

1) Ежегодное мировое производство цинка составляет около 2,5 млн. т. Большая часть добываемого металла используется для оцинковывания железа (т. е. покрытия его тонким слоем цинка) с целью предохранения от ржавления.
Основное потребление кадмия связано с производством так называемых щелочных аккумуляторов. Его ежегодная мировая выработка составляет около 7 тыс. т.
Ртуть находит применение в очень многих самых разнообразных областях, Ее ежегодная мировая добыча составляет около 6 тыс. г.
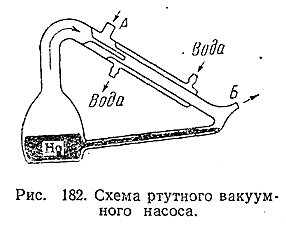
2) Важное использование ртути связано с получением высокого вакуума. Для этого обычно служит изготовляемый из стекла или металла ртутный вакуумный насос, схематически показанный на рис. 182. Нагреванием до кипения заполняющей нижнюю часть сосуда ртути соз дается непрерывная струя ее пара, котораясквозь узкую трубку с большой скоростью поступает в охлаждаемое снаружи водой пространство, присоединенное к откачиваемому сосуду через А. Быстро летящие атомы ртути своими ударами гонят молекулы откачиваемого газа к отводу Б, где эти молекулы попадают под действие более грубого насоса («фор–вакуумного»), дающего всей системе предварительное разрежение порядка О,1 –0,01 мм рт. ст. Сами ртутные пары конденсируются в охлаждаемом пространстве, и жидкая ртуть вновь поступает в нагреваемый сосуд. Установка работает непрерывно и способна создать вакуум с давлением до стомиллионных Долей миллиметра ртутного столба.
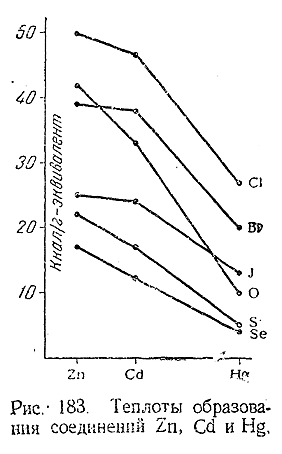
В соприкосновении с сухим воздухом Zn, Cd и Hg при обычной температуре не изменяются. Будучи достаточно нагреты, Zn и Cd сгорают до окислов ЭО, тогда как ртуть окисляется лишь медленно. Взаимодействие Zn и Cd с серой протекает также весьма энергично, но для начала реакции требуется нагревание. Напротив, ртуть соединяется с мелко раздробленной серой (при растирании обоих элементов в ступке) уже на холоду. Аналогичные различия наблюдаются и в отношении этих металлов к галоидам, с которыми при обычных условиях ртуть реагирует легче, чем Zn и Cd. Эта повышенная химическая активность ртути обусловлена ее жидким агрегатным состоянием, сильно облегчающим протекание реакций. По существу же металлические свойства элементов в ряду Zn–Cd–Hg заметно ослабляются. Это видно, частности, из приведенного на рис. 183 сопоставления теплот образования аналогичных соединений рассматриваемых элементов: при переходе от Zn к Hg они во всех случаях уменьшаются.
В ряду напряжений цинк расположен левее железа, кадмий – несколько правее его, а ртуть – значительно–правее водорода. Несмотря на то, что Zn и Cd более металличны, чем водород, они практически не вытесняют его из воды, так как поверхность металлов быстро покрывается защитной окисной пленкой. В разбавленных НСl и H2 SO4 цинк растворяется легко, кадмий медленно, а ртуть нерастворима. В азотной кислоте все три элемента легко растворяются. Например, реакция с ртутью идет па уравнению:
3Hg.+ 8HNO3 = 3Hg(NO3 )3 + 2NO + 4Н2 О
От своих аналогов цинк отличается растворимостью также в крепких растворах щелочей:
Zn + 2NaOH = Na2 ZnO2 + Н2
Цинк и кадмий образуют только один ряд соединений, отвечающий двухвалентным элементам. Для ртути, кроме того, характерны производные, в которых она электрохимически одновалентна. Соединения этого типа будут отдельно рассмотрены в конце параграфа. В противоположность не очень ядовитым производным Zn и Cd и сама ртуть и ее соединения чрезвычайно ядовиты.
Окиси цинка и его аналогов (ЭО) могут быть получены путем непосредственного соединения элементов с кислородом при нагревании. В противоположность белой ZnO аналогичные окислы Cd и Hg имеют коричневый (CdO) или ярко–красный (HgO) цвет. При очень тонком измельчении окиси ртути цвет ее становится желтым. В воде окиси Zn, Cd и Hg почти нерастворимы, но в кислотах легко растворяются, образуя соответствующие соли.
Отвечающие окислам ЭО гидроокиси [Э(ОН)2 ] цинка и кадмия выделяются в виде белых студенистых осадков при действии сильных щелочей на растворы солей Zn и Cd. Гидроокись цинка является амфотерным соединением (с преобладанием основных свойств над кислотными) и поэтому растворяется в избытке сильной щелочи с образованием цинкатов (например, Na2 ZnO2 ). У гидроокиси кадмия отчетливо выражены лишь основные свойства. В кислотах обе гидроокиси легко растворяются.
Аналогичная им гидроокись ртути [Hg(OH)2] отщепляет воду уже в момент образования. Поэтому при действии сильных щелочей на соли ртути, например, по реакции
2NaOH + Hg(NO3 )2 = 2NaNO3 + HgO + H2 O
выделяется желтая окись ртути. В избытке щелочи она нерастворима, а с кислотами легко образует соли.
Подобно самим катионам Zn2+, Cd2+и Hg2+, бесцветно и большинство их солей. Нитраты и сульфаты цинка и его аналогов хорошо растворимы в воде. По ряду Zn–Cd–Hg растворимость фторидов увеличивается, а других галоидных (и большинства остальных) солей уменьшается. Производные слабых неорганических кислот (Н2 СО3 , H2 S и т. п.), как правило, малорастворимы в воде. Очень разбавленный раствор HgCl2 (хлорной ртути, или «сулемы») является одним из употребительных дезинфицирующих веществ.
Некоторые соли Cd2+и Hg2+(а отчасти и Zn2+) в растворах значительно менее диссоциированы, чем то обычно для типа МХ2 . В частности, это относится к галоидным солям Cd и Hg (за исключением фтористых), причем по ряду Cl– – Br– – J–степень диссоциации уменьшается. Особенно мало диссоциирован цианид ртути [Hg(CN)2 ], раствор которого почти не проводит электрического тока. Напротив, нитраты и сульфаты Cd2+и Hg2+диссоциированы нормально.
Нормально диссоциированные соли Zn и его аналогов подвержены в растворе значительному гидролизу, который по ряду Zn–Cd–Hg усиливается. Некоторые соли Zn, Cd и Hg легко образуют комплексные соединения. Среди них преобладают типы М[ЭХ3 ] и М2 [ЭХ4 ]. Примером может служить хорошо растворимый в воде бесцветный ртутноиодистый калий – K2 [HgJ4 ].
3) Взаимодействие ионов Zn2+и Cd2+с аммиаком сопровождается ком–плексообразованием по схеме Э2+ + 4NН3 = [Э(NН3 )4 ]2+. Для Hg2+гораздо типичнее замещение водорода в NH3 . Так, в растворе HgCl2 по реакции HgCl2 + 2NH3 = NH2 HgCl + NH4 Cl выпадает белый осадок амидного соединения NH2 HgCl. Весьма характерны для ртути также различные соли амидного основания, отвечающего формуле HN(HgOH)2 . Наиболее известна из них коричневая йодистая соль, выпадающая в осадок при взаимодействии аммиака (или солей аммония) с щелочным раствором K2 [HgJ4 ]. Образование ее идет по уравнению: NH3 + 2K2 [HgJ4 ] + 3КОН = HOHgNHHgJ + 7KJ + 2H2 O. Реакция эта используется для открытия аммиака.
В отличие от обоих других элементов рассматриваемой подгруппы, для ртути известны производные, в которых она электрохимически одновалентна. На самом деле во всех таких произволных содержится группировка атомов –Hg2 –, причем оба атома ртути в ней двухвалентны, но одна валентность каждого из ник утрачивается на образование неполярной связи с другим по схеме: –Hg–Hg–. Так как при электролитической диссоциации группировка эта не разрушается, в растворах содержится сложный ион Hg2+.
Вещества, содержащие в своем составе группировку –Hg2 – носят название соединений закиси ртути. Ион Hg2 2+бесцветен. Большинство производящихся от него солей малорастворимо в воде. Немногие хорошо растворимые сильно диссоциированы и заметно тидролизованы. Примером производных этого типа может служить легкорастворимая в воде азотнокислая закись ртути [Нg2 (NО3 )2 ], образующаяся при взаимодействии HNO3 с избытком ртути:
6Hg + 8HNO3 = 3Hg2 (NO3 )2 + 2NO + 4H2 O
Практически важна почти нерастворимая в воде хлористая ртуть (Hg2 Cl2 ), используемая в медицине под названием «каломели».
Под действием окислителей соединения закиси ртути довольно легко переходят в производные окиси, например:
Hg2 Cl2 + Cl2 = 2HgCl2
Наоборот, восстановители легко переводят соединения окиси ртути в производные закиси, например, по реакции:
2HgCl2 + SO2 + 2H2 O = H2 SO4 + Hg2 Cl2 + 2HCl
При избытке восстановителя процесс часто идет до выделения металлической ртути:
Hg2 Cl2 + SO2 + 2H2 O = H2 SO4 + Hg + 2HCl
4) Для многих солей Hg2 2+характерен распад на соответствующую соль Hg2+и металлическую ртуть по схеме: Hg2 X2 = HgX2 + Hg. В некоторых случаях (например, Hg2 Cl2 , Hg2 SO4 ) он идет под действием света или нагревания и крайне медленно, в других случаях [например, Hg2 (CN)2 , Hg2 S] настолько быстро протекает уже в момент образования соли Hg2 2+, что последняя вовсе не может быть выделена. Например, при взаимодействии Hg2 (NO3 )2 с KCN реакция/идет по уравнению:
Hg2 (NO3 )2 + 4KCN = 2KNO3 + K2 [Hg(CN)4 ] + Hg
Сопоставляя Zn, Cd и Hg с основными элементами вторсуи группы– бериллием и магнием, –можно отметить, что некоторые свойства в ряду Be–Hg изменяются весьма закономерно. Примером могут служить температуры плавления и кипения элементов, последовательно уменьшающиеся при переходе от Be к Hg.
Однако подобная закономерность в изменении многих других свойств для ряда Be– Ra характерна еще более. В этом ряду мы имеем, например, строго последовательное возрастание атомных и ионных радиусов, отчетливое усиление основного характера гидроокисей и увеличение их растворимости в воде, повышение термической устойчивости солей и т. д.
Суммарно оба сопоставления показывают, что с точки зрения закономерности характера изменения свойств самих элементов Be и Mg могут быть включены как первые члены в обе подгруппы, а с точки зрения свойств соединений – только в подгруппу кальция.


