Бериллий
БЕРИЛЛИЙ (от греч. beryllion - уменьшит. от beryllos - берилл; лат. Beryllium) Be, хим. элемент II гр. периодич. системы, ат. н. 4, ат. м. 9,01218. В природе встречается только один стабильный изотоп 9Ве. Поперечное сечение захвата тепловых нейтронов 0,90*10-30 м2, поперечное сечение рассеяния нейтронов 7,54*10-28 м2. Конфигурация внеш. электронной оболочки 2s2; степени окисления +2, + 1 (крайне неустойчива); энергия ионизации Ве° -> Be1+ ->Ве2+ соотв. 9,3227 и 18,2112 эВ; электроотрицательность по Полингу 1,5; атомный радиус 0,113 нм; ионный радиус Be2+ 0,030 нм (координац. число 3).
Содержание бериллия в земной коре 6*10-4% по массе, в воде морей и океанов 6*10-7 мг/л. Известно 54 собственно бериллисвых минерала, важнейшие из них - берилл (и его разновидности - изумруд, аквамарин, гелиодор, воробьевит, ростерит, бандит) 3ВеО*А12О3*6SiO2 (14,0% ВеО), фенакит 2BeO*SiO2 (45,5% ВеО), бертрандит 4ВеО*2SiO2*Н2О (36,5% ВеО), гельвин (Mn,Fe,Zn)4[BeSiO4]3S (11,0-14,2% ВеО). Общие запасы бериллия в рудах (в виде берилла и бертрандита) - 380 тыс. т (1980).
Свойства. Бериллий - хрупкий твердый металл светло-серого цвета с металлич. блеском. Имеет две кристаллич. модификации: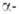 Be - решетка гексагональная типа Mg(a = 0,22866 нм, с = 0,35833 нм, z = 2, пространств. группа Р63/mmc);
Be - решетка гексагональная типа Mg(a = 0,22866 нм, с = 0,35833 нм, z = 2, пространств. группа Р63/mmc);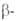 Be - решетка кубическая типа
Be - решетка кубическая типа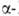 Fe (a = 0,25515 нм, пространств. группа /mЗm); т-ра перехода
Fe (a = 0,25515 нм, пространств. группа /mЗm); т-ра перехода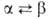 1277°С,
1277°С,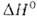 перехода 2,1 кДж/моль. Т. пл. 1287°С, т. кип. 2471 °С; плотн. 1,816 г/см3, жидкого 1,690 г/см3 (1287°С); для
перехода 2,1 кДж/моль. Т. пл. 1287°С, т. кип. 2471 °С; плотн. 1,816 г/см3, жидкого 1,690 г/см3 (1287°С); для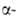 Be СР° 16,44 Дж/(моль*К), для
Be СР° 16,44 Дж/(моль*К), для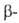 Be 30,0 Дж/(моль*К) (1555 К);
Be 30,0 Дж/(моль*К) (1555 К);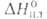 12,6 кДж/моль,
12,6 кДж/моль,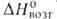 324 кДж/моль (298,15 К),
324 кДж/моль (298,15 К),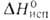 309,9 кДж/моль (2744 К); S°298 9,50 Дж/(моль*К). Ур-ния температурных зависимостей давления пара соотв. над твердым и жидким бериллием: lg p(Па) = 7,22364 - 16498,359/Т - 0,00047200T + 1,52356 lg T; lg pПа) = 16,68444 - 17051,58/T+ 0,00002400T - 1,60643 lg Т Температурный коэф. линейного расширения для бериллия 99,9%-ной чистоты при 300-500 К 12*10-6 К-1 (параллельно оси с кристаллич. решетки), 9*10-6 К-1 (перпендикулярно оси с), для бериллия с примесями [1,264% (А1 + Ме)1 13,9*10-6 - 19,6*10-6 К-1 (293-1373 К); температурный коэф. объемного расширения 33,24*10-6 К-1 (273-323 К); теплопроводность для бериллия 99,9%-ной чистоты 2930-1464 Вт/(м*К) (20-95 К), для бериллия с примесями [1,264% (Al + Mg)] 194-81 Вт/(м*К) (273-1273 К);
309,9 кДж/моль (2744 К); S°298 9,50 Дж/(моль*К). Ур-ния температурных зависимостей давления пара соотв. над твердым и жидким бериллием: lg p(Па) = 7,22364 - 16498,359/Т - 0,00047200T + 1,52356 lg T; lg pПа) = 16,68444 - 17051,58/T+ 0,00002400T - 1,60643 lg Т Температурный коэф. линейного расширения для бериллия 99,9%-ной чистоты при 300-500 К 12*10-6 К-1 (параллельно оси с кристаллич. решетки), 9*10-6 К-1 (перпендикулярно оси с), для бериллия с примесями [1,264% (А1 + Ме)1 13,9*10-6 - 19,6*10-6 К-1 (293-1373 К); температурный коэф. объемного расширения 33,24*10-6 К-1 (273-323 К); теплопроводность для бериллия 99,9%-ной чистоты 2930-1464 Вт/(м*К) (20-95 К), для бериллия с примесями [1,264% (Al + Mg)] 194-81 Вт/(м*К) (273-1273 К);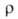 (в Ом*м] 4,0*10-8 (30К), 6,6*10-8 (293 К), 16*10-8 (600 К), 32*10-8 (1000 К); температурный коэфф.
(в Ом*м] 4,0*10-8 (30К), 6,6*10-8 (293 К), 16*10-8 (600 К), 32*10-8 (1000 К); температурный коэфф.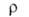 6,6*10-3 К-1 (273-373 К); т-ра перехода в сверхпроводящее состояние для компактного металла 0,026 К, для тонких пленок, полученных осаждением из газовой фазы, 5,0-8,2 К; диамагнитен, магн. восприимчивость -1*10-9 (293 К); стандартный электродный потенциал (Be/Be2+ ) —1,7 В;
6,6*10-3 К-1 (273-373 К); т-ра перехода в сверхпроводящее состояние для компактного металла 0,026 К, для тонких пленок, полученных осаждением из газовой фазы, 5,0-8,2 К; диамагнитен, магн. восприимчивость -1*10-9 (293 К); стандартный электродный потенциал (Be/Be2+ ) —1,7 В;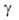 жидкого 1,444 Дж/м2 (1560 К).
жидкого 1,444 Дж/м2 (1560 К).
Мех. св-ва бериллия в значительной степени зависят от его чистоты и способа термич. обработки;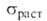 229-573 МПа, предел текучести при растяжении 213-277 МПа, относительное удлинение 0,36-15,8%, модуль упругости 0,290-0,311 МПа, твердость по Бринеллю 1060-1320 МПа. Для получения заготовок и изделий из бериллия в осн. используют методы порошковой металлургии.
229-573 МПа, предел текучести при растяжении 213-277 МПа, относительное удлинение 0,36-15,8%, модуль упругости 0,290-0,311 МПа, твердость по Бринеллю 1060-1320 МПа. Для получения заготовок и изделий из бериллия в осн. используют методы порошковой металлургии.
Бериллий в жидком состоянии раств. во мн. металлах, напр. в А1, Си, Fe, Co, Ni, Zn, не раств. в Mg. Твердые р-ры образует лишь с нек-рыми металлами; наиб, растворим бериллий в сплавах с Си (2,75% по массе), N1 (2,7%), Сг (1,7%), р-римость сильно уменьшается с понижением т-ры, в результате чего сплавы, содержащие бериллий, способны к дисперсионному твердению.
Компактный бериллий устойчив на воздухе и не взаимод. с горячей и холодной водой благодаря образованию на его пов-сти пленки бериллия оксида ВеО; выше 800°С заметно окисляется. Взаимод. с разб. и конц. соляной к-той и H2SO4, при нагревании-с HNO3. С р-рами щелочей (с концентрированными-на холоду, с разбавленными-при нагревании) образует соли - берилла ты М2[Ве(ОН)4], с расплавами щелочей - бериллаты М2ВеО2. При взаимод. с N2 или NH3 при 500-900°С получается нитрид Be3N2, с С при 1700-2100°С - карбид Ве2С, с галогенами - галогениды ВеНа12, с Р выше 750°С-фосфид Ве3Р2. В вакууме выше 700°С бериллий восстанавливает КОН, при 270°С - ВаО, при 1075°C - MgO, при 1400°С - ТiO2 до соответствующих металлов и при 270°C - SiCl4 до Si. С Н2 до 1300°С не взаимодействует. Ниже приводятся св-ва нек-рых соед. бериллия.
Гидроксид Ве(ОН)2 получают осаждением из водных р-ров солей бериллия аммиаком или NaOH; в зависимости от условий осаждения гидроксид может существовать в разл. формах, отличающихся структурой и р-римостью в воде. Он амфотерен; свежеосажденный реагирует с к-тами, с р-рами щелочей образует М2[Ве(ОН)4].
Из галогенидов бериллия наиб, важен бериллия фторид BeF2. Для ВеС12 т. пл. 416°С, т. кип. 550°С; раств. в воде (42,2% по массе при 20°С), спирте, эфире, CS2; получают действием С12 на смесь ВеО и С при 650-1000 °С; компонент расплавов при электролитич. получении бериллия. Для ВеВr2 т. пл. 488 °С, для Ве12 510°С.
Сульфат BeSO4 и нитрат Be(NO3)2 при обычных условиях существуют в виде тетрагидратов. Сульфат раств. в воде (29,7% BeSO4 при 25°С); мало гигроскопичен: при 400°С обезвоживается, при 547-600°С разлагается на ВеО и SO3. Нитрат раств. в воде [51,2% Be(NO3)2 при 20 С]; сильно гигроскопичен; при 60-100°С образует гидроксопитрат переменного состава, выше 200°С или при 130-300°С в вакууме разлагается до ВеО; безводную соль получают разложением Be(NO3)2*2N2O4 в вакууме при 50 oС.
Гидроксокарбонат - соед. переменного состава, образуется при взаимод. водных р-ров солей бериллия с Na2CO3 или (NH4)2CO3; с др. карбонатами дает комплексные соединения.
Действием карбоновых к-т на Ве(ОН)2 или гидроксокарбонат бериллия получают оксисоли типа Be4O(OOCR)6, представляющие собой молекулярные соединения. Наиб. важен оксиацетат Ве4О(ООССН3)6 - кристаллы; т.пл. 284°С, т. кип. 331°С, т. возг. 200°С (в вакууме), т. разл. 600-700°С; не раств. в воде, хорошо раств. в орг. р-рителях; промежут. продукт при очистке бериллия от др. элементов перегонкой, а также при получении ВеО высокой чистоты. Для формиата Ве4О(ООСН)6 т. возг. 247-257°С (в вакууме). В водных р-рах соли бериллия гидролизуются.
Получение. Бериллий извлекают из рудного концентрата (берилла) сульфатным или фторидным способом. В первом случае концентрат сплавляют (750°С) с Na2CO3 или СаСО3, сплав обрабатывают конц. горячей H2SO4. Из образовавшегося р-ра сульфатов Be, A1 и др. действием (NH4)2SO4 отделяют А1 в виде алюмо-аммониевых квасцов, оставшийся р-р обрабатывают избытком NaOH; при этом образуется р-р Na2[Be(OH)4] и алюминатов Na. При кипячении р-ра в результате разложения бериллата осаждается Ве(ОН)2; алюминат остается в р-ре; Ве(ОН)2 очищают от примесей экстракцией трибутилфосфатом.
По фторидному способу концентрат спекают с Na2[SiF6] и Na2CO3. Ок. 750°С образуется фторобериллат Na:
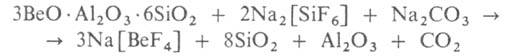
Фторобериллат Na2[BeF4] выщелачивают водой и из полученного р-ра действием NaOH осаждают Ве(ОН)2, при прокаливании к-рого образуется ВеО. Иногда Ве(ОН)2 дополнительно очищают, растворяя его в H2SO4 в присут. комплексонов и затем осаждая аммиаком. К оставшемуся после действия NaOH р-ру, содержащему NaF, для утилизации последнего добавляют Fe2(SO4)3, при этом осаждается Na3[FeF6], к-рый также используется для разложения берилла, частично заменяя Na2[SiF6].
Сульфатный способ используют также для извлечения бериллия из бертрандита. При этом сернокислый р-р экстрагируют керосином, содержащим ди(2-этилгексил) фосфорную к-ту. Орг. фракцию обрабатывают водным р-ром (NH4)2CO3, при этом осаждаются гидроксиды и гидроксокарбонаты Fe и А1, а бериллий остается в р-ре в виде (NH4)2[Be(CO3)2], к-рый при нагревании р-ра до 95°С количественно разлагается, образуя осадок 2ВеСО3*Ве(ОН)2; при прокаливании последнего при 165°С получают Ве(ОН)2.
Для получения металлич. бериллия ВеО или Ве(ОН)2 переводят в ВеС12 или BeF2. Фторид восстанавливают Mg при 925-1325°С. Расплав смеси ВеС12 с NaCl подвергают электролизу. Очищают бериллий до 99,98%-ной чистоты вакуумной дистилляцией. Пластичный бериллий, содержащий не более 10~4% примесей, получают зонной плавкой.
Определение. Для обнаружения бериллия используют эмиссионные дуговой и искровой спектральные методы (особенно широко - при анализе прир. и биол. объектов), колориметрич. (с хинализарином, бериллоном II или арсеназо I), флуорометрич. (с морином, 8-гидроксихинолином, 8-гидроксихинальдином) и радиоактивационные методы. Важное значение имеет фотонейтронный метод, не требующий отделения сопутствующих элементов; кол-во нейтронов, возникающих при р-ции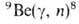 Be, пропорционально содержанию бериллия в пробе. Для определения бериллия в биол. объектах и воде океанов практич. значение имеет метод изотопного разбавления с использованием искусственного радиоактивного изотопа 7Ве(Т1/2 53,01 сут). Гравиметрич. методом бериллий определяют: в виде ВеО, получаемого после осаждения Ве(ОН)2 аммиаком при рН 9,6 в присут. комплексона III и прокаливания при 1000°С; в виде Ве2Р2О7, образующегося после осаждения и прокаливания при 800°С NH4BePO4; в виде [Co(NH3)6]2[Be4O(CO3)6]*хН2О (х = 10,8 - 11,3), осаждающегося при действии [Co(NH3)6]Cl2 на р-р (NH4)2[Be(CO3)2].
Be, пропорционально содержанию бериллия в пробе. Для определения бериллия в биол. объектах и воде океанов практич. значение имеет метод изотопного разбавления с использованием искусственного радиоактивного изотопа 7Ве(Т1/2 53,01 сут). Гравиметрич. методом бериллий определяют: в виде ВеО, получаемого после осаждения Ве(ОН)2 аммиаком при рН 9,6 в присут. комплексона III и прокаливания при 1000°С; в виде Ве2Р2О7, образующегося после осаждения и прокаливания при 800°С NH4BePO4; в виде [Co(NH3)6]2[Be4O(CO3)6]*хН2О (х = 10,8 - 11,3), осаждающегося при действии [Co(NH3)6]Cl2 на р-р (NH4)2[Be(CO3)2].
Применение. Бериллий-легирующая добавка в медных [бериллиевые бронзы; в США - ок. 80% производимого бериллия (1980)], никелевых, железных, магниевых и др. сплавах, приобретающих благодаря бериллию высокую прочность и твердость, хорошую электрич. проводимость, теплопроводность и коррозионную стойкость. Насыщение пов-сти стальных деталей бериллием (бериллизация) повышает их коррозионную стойкость. Ок. 20% производимого бериллия (США, 1980) используется в авиастроении, ракетной (детали сверхзвуковых самолетов. оболочки ракет и др.) и ядерной технике (отражатели, замедлители нейтронов); ок. 40%-в электротехнике, ок. 15%-в электронике (напр., приборы акустоэлектроники). Из бериллия изготовляют окошки рентгеновских трубок, т. к. он проницаем для рентгеновских лучей. Изотоп 7Ве - радиоактивный индикатор. Бериллий в смеси с препаратами Ra служит источником нейтронов (т.к. испускает нейтроны при действии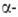 частиц,
частиц,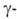 излучения) и дейтронов в результате ядерных р-ций:
излучения) и дейтронов в результате ядерных р-ций: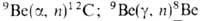 ; 9Be(d, n)10Be.
; 9Be(d, n)10Be.
Летучие и р-римые соед. бериллия, пыль, содержащая бериллий и его соед., очень токсичны, обладают аллергич. и канцерогенным действием, раздражают кожу и слизистые оболочки, вызывают дерматозы, конъюнктивиты, назофарингит и др. заболевания кожи и слизистых, заболевания легких и бронхов - трахеобронхит, пневмонию и опухоли легких. Заболевания могут возникнуть через 10-15 лет после прекращения контакта с бериллием. Для бериллия и его соед. (в пересчете на бериллий) ПДК 0,001 мг/м3, в питьевой воде 0,0002 мг/л.
Мировая добыча бериллиевых руд 1350 т/год (1979), самого бериллия-ок. 350 т/год (1980). Бериллий открыт Л. Вокленом в 1798. Металлич. бериллий получен Ф. Вёлером и независимо от него А. Бюсси в 1828.
Литература
Бериллий, под ред. Д.Уайта, Д. Берка, пер. с англ., М., 1960; Дарвин Дж., БаддериДж., Бериллий, пер. с англ., М., 1962; Кьелл грен Б. Р., Бериллий, в кн.: Справочник по редким металлам, пер. с англ., М., 1965, с. 47-80; Новоселова А. В., Бацанова Л. Р., Аналитическая химия бериллия, М., 1966; Эверест Д. А., Химия бериллия, пер. с англ., М., 1968; Котан Б. И., Капустинская К. А., Топунова Г. А., Бериллий, М., 1975: Бериллий. Справочник, под ред. А. И. Бурназяна, М., 1980; Beryllium science and technology, ed. by D. Webster, G.J.London, v. 1-2, N.Y.-L.. 1979. A.B. Новоселова.
