Глиоксаль
обыкновенно получают осторожным окислением азотной кислотой этилового спирта или уксусного альдегида (паральдегида). При этом образуется полимер глиоксаля, легко растворяющийся в воде и обладающий в растворе многими реакциями мономолекулярного глиоксаля. При выпаривании раствора полимер получается в виде бесцветной аморфной массы.
В промышленном масштабе глиоксаль получается путем каталитической дегидрогенизации этиленгликоля:

Глиоксаль является одним из простейших представителей органических веществ, обладающих окраской. При перегонке полимерного глиоксаля с фосфорным ангидридом получается мономерный глиоксаль СНО—СНО в виде паров, обладающих ярким изумрудно-зеленым цветом и острым запахом, похожим на запах формалина. При сильном охлаждении паров получаются красивые желтые кристаллы, которые при еще более сильном охлаждении делаются бесцветными. Кристаллы плавятся при 15° С, превращаясь в желтую жидкость, кипящую при 51° С. Окрашенность глиоксаля связана с присутствием в молекуле двух рядом расположенных карбонильных групп.
Жидкий глиоксаль крайне неустойчив; в присутствии даже ничтожных следов влаги он быстро превращается в твердый полимер, только в виде которого глиоксаль и был известен в течение долгого времени.
Глиоксаль дает все качественные реакции альдегидов (окраска с фуксинсернистой кислотой, образование серебряного зеркала и др.). Как диальдегид он образует соединение с двумя молекулами бисульфита натрия, с гидроксиламином дает диоксим HON=CH—СН=NOH, называемый глиоксимом, присоединяет две молекулы синильной кислоты:
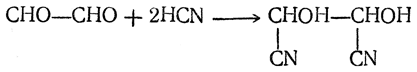
Окислением глиоксаля могут быть получены глиоксиловая кислота СНО—СООН и щавелевая кислота НООС—СООН.
При действии растворов едкого кали глиоксаль превращается в гликолевую кислоту. Реакция состоит в том, что одна альдегидная группа окисляется, а другая восстанавливается:
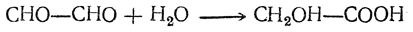
Янтарный альдегид СНО—СН2—CH2—СНО был получен действием озона на диаллил СН2=СН—СН2—СН2—СН=СН2 с промежуточным образованием диозонида:
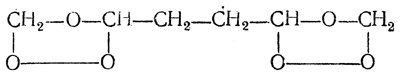
Диоксим янтарного альдегида получается из пиррола действием гидроксиламина:
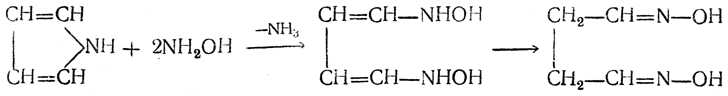
Янтарный альдегид — бесцветная, остро пахнущая жидкость с т. кип. 56,6° С при 8,5 мм. pm. cm.


