Калориметр
Калориметр (от лат. calor — тепло и ...метр), прибор для измерения количества теплоты, выделяющейся или поглощающейся в каком-либо физическом, химическом или биологическом процессе. Термин «калориметр» был предложен А. Лавуазье и П. Лапласом (1780).
Современные калориметры работают в диапазоне температур от 0,1 до 3500 К и позволяют измерять количество теплоты с точностью до 10-2%. Устройство калориметров весьма разнообразно и определяется характером и продолжительностью изучаемого процесса, областью температур, при которых производятся измерения, количеством измеряемой теплоты и требуемой точностью.
Калориметр, предназначенный для измерения суммарного количества теплоты Q, выделяющейся в процессе от его начала до завершения, называют калориметром-интегратором; калориметр для измерения тепловой мощности L и её изменения на разных стадиях процесса — измерителем мощности или калориметром-осциллографом. По конструкции калориметрической системы и методу измерения различают жидкостные и массивные калориметры, одинарные и двойные (дифференциальные).
Жидкостный калориметр-интегратор переменной температуры (рис. 1) с изотермической оболочкой применяют для измерений теплот растворения и теплот химических реакций. Он состоит из сосуда с жидкостью (обычно водой), в котором находятся: камера для проведения исследуемого процесса («калориметрическая бомба»), мешалка, нагреватель и термометр. Теплота, выделившаяся в камере, распределяется затем между камерой, жидкостью и др. частями калориметра, совокупность которых называют калориметрической системой прибора. Изменение состояния (например, температуры) калориметрической системы позволяет измерить количество теплоты, введённое в калориметр. Нагрев калориметрической системы фиксируется термометром. Перед проведением измерений калориметр градуируют — определяют изменение температуры калориметрической системы при сообщении ей известного количества теплоты (нагревателем калориметра или в результате проведения в камере химической реакции с известным количеством стандартного вещества). В результате градуировки получают тепловое значение калориметра, т. е. коэффициент, на который следует умножить измеренное термометром изменение температуры калориметра для определения количества введённой в него теплоты. Тепловое значение такого калориметра представляет собой теплоёмкость (с) калориметрической системы. Определение неизвестной теплоты сгорания или др. химической реакции Q сводится к измерению изменения температуры Dt калориметрической системы, вызванного исследуемым процессом: Q = c×Dt. Обычно значение Q относят к массе вещества, находящегося в камере калориметра.
Калориметрические измерения позволяют непосредственно определить лишь сумму теплот исследуемого процесса и различных побочных процессов, таких как перемешивание, испарение воды, разбивание ампулы с веществом и т.п. Теплота побочных процессов должна быть определена опытным путём или расчётом и исключена из окончательного результата. Одним из неизбежных побочных процессов является теплообмен калориметра с окружающей средой посредством излучения и теплопроводности. В целях учёта побочных процессов и прежде всего теплообмена калориметрическую систему окружают оболочкой, температуру которой регулируют.
У жидкостных калориметров температуру оболочки поддерживают постоянной. При определении теплоты химической реакции наибольшие затруднения часто связаны не с учётом побочных процессов, а с определением полноты протекания реакции и с необходимостью учитывать несколько реакций.
В калориметре-интеграторе другого вида — изотермическом (постоянной температуры) введённая теплота не изменяет температуры калориметрической системы, а вызывает изменение агрегатного состояния тела, составляющего часть этой системы (например, таяние льда в ледяном калориметре Бунзена). Количество введённой теплоты рассчитывается в этом случае по массе вещества, изменившего агрегатное состояние (например, массе растаявшего льда, которую можно измерить по изменению объёма смеси льда и воды), и теплоте фазового перехода.
Массивный калориметр-интегратор чаще всего применяют для определения энтальпии веществ при высоких температурах (до 2500 °С). Калориметрическая система у калориметров этого типа представляет собой блок из металла (обычно из меди или алюминия) с выемками для сосуда, в котором происходит реакция, для термометра и нагревателя. Энтальпию вещества рассчитывают как произведение теплового значения калориметра на разность подъёмов температуры блока, измеряемых после сбрасывания в его гнездо ампулы с определённым количеством вещества, а затем пустой ампулы, нагретой до той же температуры.
Теплоёмкость газов, а иногда и жидкостей, определяют в т. н. проточных лабиринтных калориметрах — по разности температур на входе и выходе стационарного потока жидкости или газа, мощности этого потока и джоулевой теплоте, выделенной электрическим нагревателем калориметра.
Калориметр, работающий как измеритель мощности, в противоположность калориметру-интегратору должен обладать значительным теплообменом, чтобы вводимые в него количества теплоты быстро удалялись и состояние калориметра определялось мгновенным значением мощности теплового процесса. Тепловая мощность процесса находится из теплообмена калориметра с оболочкой. Такие калориметры (рис. 2), разработанные французским физиком Э. Кальве (Е. Calvet, 1895—1966), представляют собой металлический блок с каналами, в которые помещают цилиндрические ячейки. В ячейке проводится исследуемый процесс; металлический блок играет роль оболочки (температура его поддерживается постоянной с точностью до 10-5—10-6 К). Разность температур ячейки и блока измеряется термобатареей, имеющей до 1000 спаев. Теплообмен ячейки и эдс термобатареи пропорциональны малой разности температур, возникающей между блоком и ячейкой, когда в ней выделяется или поглощается теплота. В блок помещают чаще всего две ячейки, работающие как дифференциальный калориметр: термобатареи каждой ячейки имеют одинаковое число спаев и поэтому разность их эдс позволяет непосредственно определить разность мощности потоков теплоты, поступающей в ячейки. Этот метод измерений позволяет исключить искажения измеряемой величины случайными колебаниями температуры блока. На каждой ячейке монтируют обычно две термобатареи: одна позволяет скомпенсировать тепловую мощность исследуемого процесса на основе Пельтье эффекта, а другая (индикаторная) служит для измерения нескомпенсированной части теплового потока. В этом случае прибор работает как дифференциальный компенсационный калориметр. При комнатной температуре такими калориметрами измеряют тепловую мощность процессов с точностью до 1 мквт.
Обычные названия калориметров — «для химической реакции», «бомбовый», «изотермический», «ледяной», «низкотемпературный» — имеют историческое происхождение и указывают главным образом на способ и область использования калориметра, не являясь ни полной, ни сравнительной их характеристикой.
Общую классификацию калориметров можно построить на основе рассмотрения трёх главных переменных, определяющих методику измерений: температуры калориметрической системы Tc; температуры оболочки To, окружающей калориметрическую систему количества теплоты L, выделяемой в калориметре в единицу времени (тепловой мощности).
Калориметр с постоянными Tc и To называют изотермическим; с Tc = To — адиабатическим; калориметр, работающий при постоянной разности температур Tc — To, называют калориметром с постоянным теплообменом; у изопериболического калориметра (его ещё называют калориметром с изотермической оболочкой) постоянна To, а Tc является функцией тепловой мощности L.
Важным фактором, влияющим на окончательный результат измерений, является надёжная работа автоматических регуляторов температуры изотермических или адиабатических оболочек. В адиабатическом калориметре температура оболочки регулируется так, чтобы она была всегда близка к меняющейся температуре калориметрической системы. Адиабатическая оболочка — лёгкая металлическая ширма, снабженная нагревателем, — уменьшает теплообмен настолько, что температура калориметра меняется лишь на несколько десятитысячных град/мин. Часто это позволяет снизить теплообмен за время калориметрического опыта до незначительной величины, которой можно пренебречь. В случае необходимости в результаты непосредственных измерений вводится поправка на теплообмен, метод расчёта которой основан на законе теплообмена Ньютона — пропорциональности теплового потока между калориметром и оболочкой разности их температур, если эта разность невелика (до 3—4 °С).
Для калориметра с изотермической оболочкой теплоты химической реакции могут быть определены с погрешностью до 0,01%. Если размеры калориметра малы, температура его изменяется более чем на 2—3 °С и исследуемый процесс продолжителен, то при изотермической оболочке поправка на теплообмен может составить 15—20% от измеряемой величины и существенно ограничить точность измерений. В этих случаях целесообразнее применять адиабатическую оболочку.
При помощи адиабатического калориметра определяют теплоёмкость твёрдых и жидких веществ в области от 0,1 до 1000 К. При комнатных и более низких температурах адиабатический калориметр, защищенный вакуумной рубашкой, погружают в Дьюара сосуд, заполненный жидким гелием, водородом или азотом (рис. 3). При повышенных температурах (выше 100 °С) калориметр помещают в термостатированную электрическую печь.
Лит.: Попов М. М., Термометрия и калориметрия, 2 изд., М., 1954; Скуратов С. М., Колосов В. П., Воробьев А. Ф., Термохимия, ч. 1—2, М., 1964—66; Кальве Э., Прат А., Микро-калориметрия, пер. с франц., М., 1963; Experimental thermochemistry, v. 1—2 N. Y. — L., 1956-62.
В. А. Соколов.
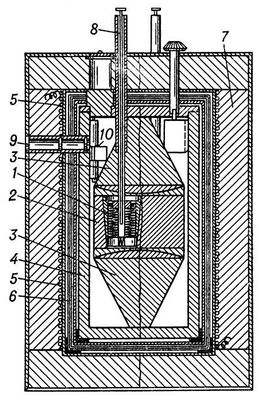
Рис. 2. Калориметр Э. Кальве для измерения тепловой мощности процессов (схема): 1 — калориметрическая ячейка с термопарами; 2 — блок калориметра; 3 — металлические конусы для создания однородного поля температур в блоке; 4 — оболочка; 5 — нагреватель для термостатирования прибора; 6 — тепловые экраны; 7 — тепловая изоляция; 8 — трубка для введения вещества в калориметр; 9 — окно для отсчётов показаний гальванометра 10.
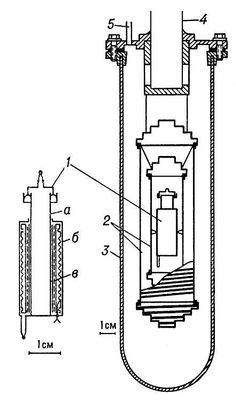
Рис. 3. Адиабатический калориметр для определения теплоёмкости при низких температурах (схема): 1 — калориметр (а — сосуд для вещества, б — термометр сопротивления, в — нагреватель); 2 — адиабатические оболочки (ширмы); 3 — вакуумная рубашка; 4 — труба для откачки; 5 — трубка для электрических проводов.
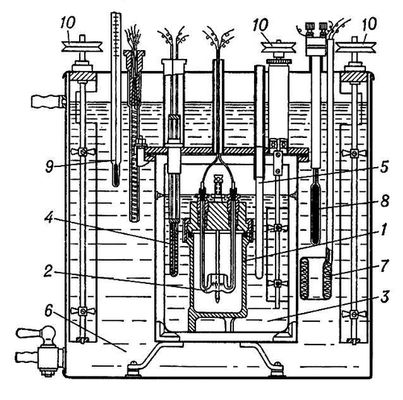
Рис. 1. Жидкостный калориметр-интегратор с изотермической оболочкой (схема): 1 — «калориметрическая бомба»; 2 — нагреватель для возбуждения реакции; 3 — собственно калориметр (сосуд, заполненный водой); 4 — термометр сопротивления; 5 — холодильник (трубка, через которую можно пропускать холодный воздух); 6 — изотермическая оболочка калориметра, заполненная водой; 7 — нагреватель оболочки; 8 — контактный термометр для регулировки температуры оболочки; 9 — контрольный термометр; 10 — мешалки с приводом.
