Гиббса-Дюгема уравнение
ГИББСА-ДЮГЕМА УРАВНЕНИЕ, связывает изменения т-ры Т, давления р и хим. потенциалов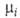 компонентов равновесных термодинамич. систем. В общем виде записывается в форме:
компонентов равновесных термодинамич. систем. В общем виде записывается в форме: 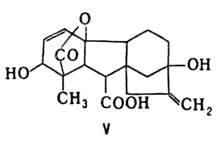
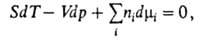
где 5 и К-энтропия и объем системы соотв., ni-число молей i-того компонента. Для процессов, происходящих при постоянных Т и р, Гиббса - Дюгема уравнение устанавливает связь между изменениями хим. потенциалов компонентов и Наиб. широко используется в термодинамике р-ров. Для р-ров неэлектролитов употребительны след. формы ур-ния: 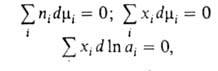
где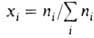 -молярная доля i-того компонента, аi-его активность, связанная с
-молярная доля i-того компонента, аi-его активность, связанная с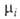 соотношением:
соотношением: 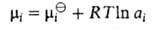
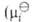 -хим. потенциал компонента в стандартном состоянии, R-газовая постоянная). Форма записи Гиббса - Дюгема уравнения для коэффициентов активности
-хим. потенциал компонента в стандартном состоянии, R-газовая постоянная). Форма записи Гиббса - Дюгема уравнения для коэффициентов активности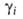 зависит от способа выражения концентрации (в молярных долях, молярности или моляльности). При выражении концентрации в молярных долях для р-ров неэлектролитов
зависит от способа выражения концентрации (в молярных долях, молярности или моляльности). При выражении концентрации в молярных долях для р-ров неэлектролитов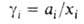 и Гиббса - Дюгема уравнение имеет вид: Для р-ров электролитов разработаны спец. формы
и Гиббса - Дюгема уравнение имеет вид: Для р-ров электролитов разработаны спец. формы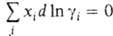 записи Гиббса - Дюгема уравнения.
записи Гиббса - Дюгема уравнения.
Гиббса - Дюгема уравнение позволяет определять зависимость от состава хим. потенциала, активности или коэф. активности одного из компонентов бинарного р-ра, если подобная зависимость известна для др. компонента (в случае многокомпонентных р-ров-для всех остальных компонентов). Гиббса - Дюгема уравнение применяют также для определения активности компонентов бинарного р-ра по данным о равновесном общем давлении пара над р-ром при данной Т.; с его помощью проверяют термодинамич. согласованность экспериментально определенных значений активности в-в (см. Активность термодинамическая).
Ур-ние предложено Дж. Гиббсом в 1876; его приложения впервые рассмотрены П. Дюгемом (Дюэмом) в 1886.
Лит. см. при статьях Активность, Растворы электролитов, Растворы неэлектролитов. В. А. Михайлов.
