Ультрафиолетовая спектроскопия
УЛЬТРАФИОЛЕТОВАЯ СПЕКТРОСКОПИЯ (УФ спектроскопия, УФС), раздел оптич. спектроскопии, включающий получение, исследование и применение спектров испускания, поглощения и отражения в ультрафиолетовой области, т. е. в диапазоне длин волн 10-400 нм (волновых чисел 2,5 · 104 - 106 см-1). УФС при длине волны меньше 185 нм наз. вакуумной, т. к. в этой области УФ излучение настолько сильно поглощается воздухом (гл. обр. кислородом), что необходимо применять вакуумные или наполненные непоглощающим газом спектральные приборы.
Техника измерения УФ спектров в осн. такая же, как спектров в видимой области (см. Спектрофотометрия). Спектральные приборы для УФС отличаются тем, что вместо стеклянных оптич. деталей применяют аналогичные кварцевые (реже флюоритовые или сапфировые), к-рые не поглощают УФ излучение. Для отражения УФ излучения используют алюминиевые покрытия. Приемниками служат обычные или маложелатиновые фотоматериалы, а также фотоэлектрич. приборы, гл. обр. фотоэлектронные умножители, счетчики фотонов, фотодиоды, ионизационные камеры. Для увеличения чувствительности при использовании фотоматериалов иногда регистрируют флуоресценцию, вызванную исследуемым УФ излучением.
Для возбуждения УФ спектров испускания атомов и молекул служат пламя (см. Фотометрия пламени эмиссионная), дуга постоянного или переменного тока, низко- и высоковольтные искры, ВЧ и СВЧ разряд (в т.ч. безэлектродный), плазмотроны, разряд в полом катоде, лазерное излучение и др. (см. Спектральный анализ). УФ спектры поглощения и отражения получают в осн. с использованием таких источников излучения, как дейтериевые (водородные), ртутные, ксеноновые и др. газоразрядные лампы. Используют также нагретые до ок. 3000 К твердые тела, напр. разл. вольфрамовые лампы (с ленточным излучателем или со сферич. анодом, разогреваемым дуговым разрядом, и др.). Источниками линейчатых спектров служат спектральные лампы разл. конструкций (напр., с полым катодом). Применяют также лазеры, излучающие в УФ области (водородный лазер).
Как правило, при облучении УФ излучением B-BO не разрушается и не изменяется, что позволяет получать данные о его хим. составе и структуре. В УФ области проявляются электронные спектры, т. е. положение полос и линий определяется разностью энергий разл. электронных состояний атомов и молекул. Здесь лежат резонансные линии нейтральных, одно- и двукратно ионизованных атомов, а также спектральные линии, испускаемые многократно ионизованными атомами в возбужденном состоянии. В ближней УФ области сосредоточены полосы поглощения большинства полупроводников, возникающие при прямых переходах электронов из валентной зоны в зону проводимости.
В УФ области находятся также электронно-колебат. полосы молекул (колебат. структура проявляется только при низких т-рах; в обычных условиях она приводит к диффузным, т. е. размытым, спектрам), что широко используют в хим. анализе и исследованиях. Появление этих полос связано с переходами электронов между связывающими 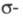 и
и 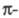 , несвязывающими п- и разрыхляющими
, несвязывающими п- и разрыхляющими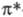 - и
- и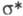 -орбиталями (см. Молекулярные спектры). Это позволяет использовать УФС для изучения электронного строения молекул, влияния заместителей на хим. св-ва ароматич. соединений, для установления типа хим. связей, определения параметров пов-стей потенц. энергии возбужденных состояний молекул и т. п. В основе этих исследований лежит отнесение полос поглощения УФ спектров к определенным электронным переходам. При этом необходимо учитывать положение и интенсивность полос. Обычно под термином "УФ спектроскопия" понимают именно эту область спектроскопии.
-орбиталями (см. Молекулярные спектры). Это позволяет использовать УФС для изучения электронного строения молекул, влияния заместителей на хим. св-ва ароматич. соединений, для установления типа хим. связей, определения параметров пов-стей потенц. энергии возбужденных состояний молекул и т. п. В основе этих исследований лежит отнесение полос поглощения УФ спектров к определенным электронным переходам. При этом необходимо учитывать положение и интенсивность полос. Обычно под термином "УФ спектроскопия" понимают именно эту область спектроскопии.
Для насыщ. углеводородов возможны только 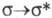 -переходы, требующие больших энергий, и соответствующие им полосы лежат в области вакуумного УФ, напр. в случае метана и этана - при 125 и 135 нм соответственно. Для ненасыщ. соединений характерны
-переходы, требующие больших энергий, и соответствующие им полосы лежат в области вакуумного УФ, напр. в случае метана и этана - при 125 и 135 нм соответственно. Для ненасыщ. соединений характерны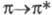 -переходы, проявляющиеся при длинах волн 165-200 нм. Наличие сопряжения, алкильных или др. заместителей (в т. ч. содержащих гетероатомы) приводит к смещению полос в длинноволновую область (бато-хромный сдвиг), напр. бутадиен поглощает уже при 217 нм. У карбонильных (как и у тиокарбонильных) соед. в наиб. длинноволновой области находится малоинтенсивная полоса, вызванная
-переходы, проявляющиеся при длинах волн 165-200 нм. Наличие сопряжения, алкильных или др. заместителей (в т. ч. содержащих гетероатомы) приводит к смещению полос в длинноволновую область (бато-хромный сдвиг), напр. бутадиен поглощает уже при 217 нм. У карбонильных (как и у тиокарбонильных) соед. в наиб. длинноволновой области находится малоинтенсивная полоса, вызванная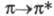 -переходом, запрещенным по симметрии. В более коротковолновой области проявляются полосы высокой интенсивности
-переходом, запрещенным по симметрии. В более коротковолновой области проявляются полосы высокой интенсивности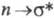 - и
- и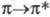 -переходов. Так, в спектре формальдегида имеются максимумы поглощения при 295 (слабый), 185 и 155 нм.
-переходов. Так, в спектре формальдегида имеются максимумы поглощения при 295 (слабый), 185 и 155 нм.
Полосы поглощения сложных эфиров, амидов, галогенан-гидридов смещены в коротковолновую область, а полосы тиокарбонильных соед.- в длинноволновую область по сравнению с полосами поглощения соответствующих карбонильных соед., напр.: максимумы поглощения CH3C(O)H, CH3C(O)NH2 и CH3C(S)NH2 наблюдаются при 290, 214 и 358 нм соответственно. Вследствие гибридизации неподеленной пары электронов азота в соед., содержащих группу C = N, интенсивность полосы 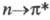 -перехода у них выше, чем у карбонильных соединений. В спектрах нитросоед. положение и интенсивность полосы
-перехода у них выше, чем у карбонильных соединений. В спектрах нитросоед. положение и интенсивность полосы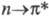 -перехода зависят от природы соседнего с нитрогруппой атома. Так, у О-нитросоед. эта малоинтенсивная полоса расположена в более коротковолновой области, чем у С-нитросоединений. В спектре нитрами-нов (N-NO2) полоса
-перехода зависят от природы соседнего с нитрогруппой атома. Так, у О-нитросоед. эта малоинтенсивная полоса расположена в более коротковолновой области, чем у С-нитросоединений. В спектре нитрами-нов (N-NO2) полоса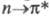 -перехода наиб. интенсивная.
-перехода наиб. интенсивная.
Для азо- и нитрозосоединений также характерны 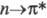 -переходы. Полосы УФ спектра N- и О-нитрозосоединений смещены в коротковолновую область по сравнению с полосами С-нитрозосоединений. Сопряжение кратных связей с такими азотсодержащими хромофорными группами, как NO2, NO, N = N, N3, вызывает батохромный сдвиг всех полос поглощения и возрастание их интенсивности.
-переходы. Полосы УФ спектра N- и О-нитрозосоединений смещены в коротковолновую область по сравнению с полосами С-нитрозосоединений. Сопряжение кратных связей с такими азотсодержащими хромофорными группами, как NO2, NO, N = N, N3, вызывает батохромный сдвиг всех полос поглощения и возрастание их интенсивности.
Характер спектра поглощения зависит от взаимного расположения хромофоров. Если хромофорные группы соединены непосредственно, то в спектре наблюдаются сильные изменения по сравнению со спектрами соед. с изолированными хромофорными группами. Относит. расположение хромофоров у кратных связей позволяет различать цис- и транс-изомеры.
Полосы в спектрах ароматич. соед. связаны с переходами 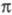 -электронов ароматич. системы. На вид спектра влияют заместители: такие как алкил, галогены - незначительно, группы с неподеленными парами электронов (ОН, OR, NH2, NF2) - сильно. Если имеются карбонильная, нитро- или нитрозогруппа, то в спектре дополнительно наблюдаются полосы
-электронов ароматич. системы. На вид спектра влияют заместители: такие как алкил, галогены - незначительно, группы с неподеленными парами электронов (ОН, OR, NH2, NF2) - сильно. Если имеются карбонильная, нитро- или нитрозогруппа, то в спектре дополнительно наблюдаются полосы 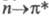 -перехода. В спектрах нек-рых замещенных бензола, напр. нитробензола, удается выделить полосы с внутримол. переносом заряда (соответствующие переходам, при к-рых происходит преимуществ, уменьшение электронной плотности на одном участке молекулы и ее увеличение на др. участке).
-перехода. В спектрах нек-рых замещенных бензола, напр. нитробензола, удается выделить полосы с внутримол. переносом заряда (соответствующие переходам, при к-рых происходит преимуществ, уменьшение электронной плотности на одном участке молекулы и ее увеличение на др. участке).
УФ спектры ароматич. соед. зависят не только от характера, но и от взаимного расположения заместителей, так, в спектрах орто- и меmа-нитроанилина имеются три полосы, вызванные переносом заряда от донора к акцептору, от кольца к акцептору и локальным возбуждением бензольного кольца с вкладом переноса заряда от донора к кольцу. пара-Изомер имеет те же переходы, но из-за совпадения направления переноса заряда во всех трех случаях в спектре появляется одна интенсивная полоса поглощения (при 320 нм).
Насыщ. гетероциклы имеют полосы, соответствующие 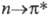 -переходам. Полосы поглощения кислород- и азотсодержащих соед. лежат в области вакуумного УФ. Серосодер-жащие соед. имеют соответствующие полосы в обычной УФ области.
-переходам. Полосы поглощения кислород- и азотсодержащих соед. лежат в области вакуумного УФ. Серосодер-жащие соед. имеют соответствующие полосы в обычной УФ области.
Замена в ароматич. кольце группы =СН на =N приводит к повышению интенсивности длинноволновой полосы поглощения и появлению полосы 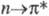 -перехода (к-рая в случае пиридина проявляется только в спектрах его паров). По мере увеличения числа атомов N в цикле полосы
-перехода (к-рая в случае пиридина проявляется только в спектрах его паров). По мере увеличения числа атомов N в цикле полосы 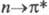 -переходов сдвигаются в длинноволновую область.
-переходов сдвигаются в длинноволновую область.
Наличие интенсивных характеристич. полос в УФ спектрах мн. хим. соединений используется для разработки методов их идентификации и количеств, определения. Последние основаны на законе Бугера-Ламберта-Бера (см. Абсорбционная спектроскопия)и отличаются селективностью и высокой чувствительностью - до 10-7% по массе. Имеются хим. сенсоры со световодами, измеряющие поглощение определяемого в-ва в УФ области.
УФС применяют также для изучения кинетики хим. и фотохим. р-ций, исследования люминесценции, уровней энергии и вероятностей квантовых переходов в твердых телах и т. д. Особое значение имеет УФС для установления состава космич. объектов и изучения протекающих на них процессов.
Лит.: Столяров К.П., Химический анализ в ультрафиолетовых лучах, M.-Л., 1965; Зайдель А.Н., Островская Г.В., Островский Ю.И., Техника и практика спектроскопии, 2 изд., M., 1976. Э. Г. Тетерин.
