Лоссена реакция
ЛОССЕНА РЕАКЦИЯ (Лоссена перегруппировка, Лоссена расщепление), превращение гидроксамовых к-т или их ацильных производных в изоцианаты при нагр. в присут. дегидратирующих агентов или без них: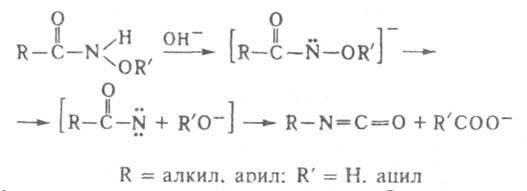
В качестве дегидратирующих агентов обычно используют Р2О5, SOCl2, (CH3CO)2O, полифосфорную к-ту и др. В случае ацильных производных р-цию проводят в присут. оснований. Выходы изоцианатов или продуктов их дальнейших превращ. (напр., аминов в случае гидролиза) 60-80%. Наличие электронодонорных заместителей в радикале R ускоряет Лоссена реакцию, присутствие этих же заместителей в R' оказывает противоположное действие. В случае оптически активных соед. стереохим. конфигурация сохраняется. Особенно легко Лоссена реакции подвергаются О-сульфонилированные и О-фосфорилированные гидроксамовые к-ты. Лоссена реакция по механизму близка к др. анионотропным перегруппировкам (Гофмана, Бекмана, Курциуса, Шмидта); разрыв связи N-О сопровождается синхронной миграцией радикала R. "Амидная модификация" Лоссена реакции - получение аминов (выходы до 80%) нагреванием гидроксамовых к-т, напр.:
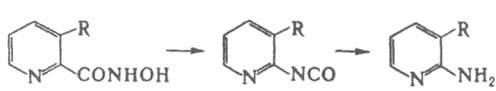
Лоссена реакция - препаративный способ синтеза аминов, уретанов, диизоцианатов, мочевин и др. Лоссена реакцией функционально замещенных гидроксамовых к-т получают, в частности, чувствительные к к-там полипептиды (напр., политриптофан), а также представляющие биохим. интерес гетероциклич. системы, содержащие кольцо N-гидроксиурацила. Р-ция открыта В. Лоссеном в 1872.
Литература
Общая органическая химия, пер. с англ., т. 4. М., 1983. с. 507-08; Bauer L., Ехnеr О., "Angew. Chem.", 1974, v. 13, №6, p. 376-82; Harger M. J. P., "J. Chem. Soc, Perkin Trans.", I, 1983, № II, p. 2699-2704. К. В. Вацуро.
Ещё по теме
Реакция Фаворского — перегруппировка галогенкетонов
Реакции Эльбса — особенности и применение
Перегруппировка Ортона — особенности и механизм реакции
Реппе реакции в органической химии
Прево реакция — механизм и применение
Сторка реакция — особенности и применение
Способы получения галоидальдегидов и галоидкетонов
Галоидзамещённые кислоты — способы получения
Реакция Розенмунда — особенности и применение
Xophepa реакция — особенности и применение
Реакции Штаудингера — механизмы и применение
