Фаворского реакции
ФАВОРСКОГО РЕАКЦИИ. 1) Перегруппировка a-га-логенкетонов в карбоновые к-ты, их эфиры или амиды при действии оснований - соотв. щелочей, алкоголятов или аминов (наз. также перегруппировкой Фаворского):
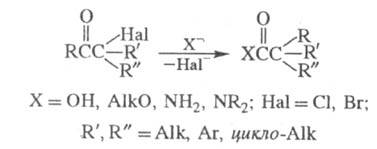
Обычно галогенкетон смешивают с конц. р-ром основания (напр., в спирте) или с суспензией основания в р-рителе (этаноле, эфире, толуоле) при т-ре от -20 до +30 0C. Реакц. смесь выдерживают 10-30 мин (в случае низкореакционно-способных кетонов - 2-4 ч при нагр.). Выходы 30-70%.
В классич. варианте перегруппировки радикал R содержит атом H у 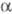 -атома С. В отсутствие
-атома С. В отсутствие 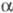 -H-атома р-ция обычно идет в сравнительно жестких условиях (напр., при кипячении с NaOH в толуоле) и наз. квазиперегруппировкой Фаворского.
-H-атома р-ция обычно идет в сравнительно жестких условиях (напр., при кипячении с NaOH в толуоле) и наз. квазиперегруппировкой Фаворского.
Перегруппировка циклич. кетонов протекает с сужением цикла, напр.:
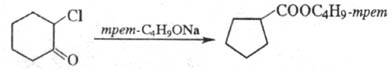
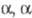 -Дигалогенкетоны и
-Дигалогенкетоны и 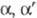 -дигалогенкетоны, содержащие
-дигалогенкетоны, содержащие 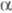 -H-атомы* в условиях Фаворского реакции образуют одну и ту же
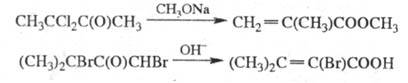
-H-атомы* в условиях Фаворского реакции образуют одну и ту же 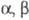 -ненасыщ. к-ту (или ее производное); тригалогенкетоны -галогензамещ. ненасыщ. к-ты, напр.:
-ненасыщ. к-ту (или ее производное); тригалогенкетоны -галогензамещ. ненасыщ. к-ты, напр.:
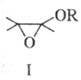
Осн. побочные продукты - эпоксиэфиры ф-лы I, образующиеся из них гидроксикетали и 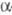 -гидроксикетоны, продукты расщепления связей С — С или замещения атома Hal на группы ОН, OR или NR2, а также винилкетоны.
-гидроксикетоны, продукты расщепления связей С — С или замещения атома Hal на группы ОН, OR или NR2, а также винилкетоны.
Механизм классич. перегруппировки включает образование на промежут. стадии циклопропанона (BH - основание):
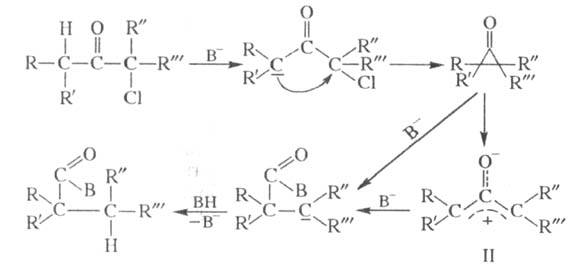
Циклопропаноны во мн. случаях (напр., при R, R: = трет-С4Н9)удается выделить. Полученные др. способами циклопропаноны дают продукты перегруппировки при действии на них CH3ONa и др. сильных оснований.
Квазиперегруппировка Фаворского протекает по т. наз. семибензильному механизму:
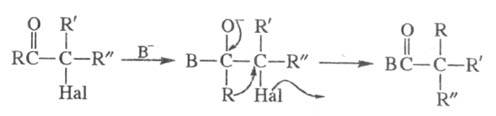
Известны случаи, когда семибензильный механизм реализуется и для кетонов с 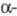 H-атомом (напр., для a-галогенциклобу-танонов). Видимо, в отдельных случаях в зависимости от условий может преобладать либо первый, либо второй механизм.
H-атомом (напр., для a-галогенциклобу-танонов). Видимо, в отдельных случаях в зависимости от условий может преобладать либо первый, либо второй механизм.
Оба механизма (за исключением варианта с образованием промежут. соед. II) предполагают обращение конфигурации при 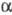 -C-атоме, у к-рого мигрирующая группа замещает атом галогена.
-C-атоме, у к-рого мигрирующая группа замещает атом галогена.
Превращения, аналогичные этой перегруппировке, претерпевают под действием оснований амиды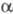 -галогенкарбоновых к-т,
-галогенкарбоновых к-т, 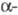 галогеналкилсульфамиды,
галогеналкилсульфамиды, 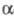 -галогеналкилсульфоны,
-галогеналкилсульфоны, 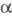 -гидроксикетоны и
-гидроксикетоны и 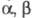 -эпоксикетоны, напр.:
-эпоксикетоны, напр.:
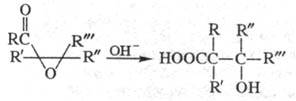
Р-цию используют в препаративной практике для получения циклич. кетонов и высокозамещ. (у 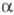 -С-атома) карбоно-вых к-т, в синтезе сложных прир. в-в (напр., стероидов).
-С-атома) карбоно-вых к-т, в синтезе сложных прир. в-в (напр., стероидов).
Р-ция открыта A. E. Фаворским в 1894.
Лит.: Кенде Э., в сб.: Органические реакции, пер. с англ., сб. 11, M., 1965, с. 267-326; Ахрем А. А. [и др.], "Успехи химии", 1970, т. 39, в. 9, с. 1560-90; Mарч Дж., Органическая химия, пер. с англ., т. 4, M., 1988, с. 1426.
2) Получение ацетиленовых спиртов присоединением ацетиленовых углеводородов к карбонильным соединениям в присут. оснований:
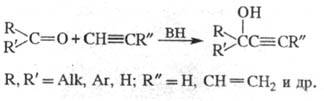
В р-цию вступают алициклич. кетоны и нек-рые альдегиды. В ряду ацетиленов чаще используют незамещ. ацетилен и винилацетилен. Обычно р-цию проводят с суспензией KOH или NaNH2 в р-рителе (эфире, бензоле, ДМФА и др.) при т-ре от -70 до +40 С, давлении 0,4-0,9 МПа и большом избытке ацетилена (вместо ацетилена можно использовать CaC2 в присут. KOH). Образовавшиеся алкоголяты обрабатывают H2O. Выходы 40-60%.
Осн. побочные продукты - смолы и ацетиленовые 1,4-ди-олы. Последние становятся осн. продуктом при использовании небольшого избытка ацетилена и т-ре ок. 20 0C:
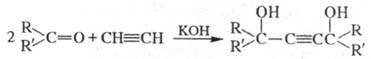
Считается, что механизм р-ции включает образование аце-тиленида, к-рый присоединяется к карбонильному соед. с образованием алкоголята ацетиленового спирта.
Р-цию используют в синтезе виниловых спиртов, диенов, разл. алициклич. и гетероциклич. соединений.
Р-ция открыта A. E. Фаворским в 1905.
Лит.: Котляревский И.Л., Швар цберг M. С., Фишер Л.Б., Реакции ацетиленовых соединений, Новосиб., 1967, с. 5-170; Михайловский Д.И. [и др.], "Ж. орган, химии", 1974, т. 10, в. 2, с. 188-91; Кондратьева Л. А. [и др.], там же, 1976, т. 12, в. 5, с. 940-44.
3) Изомеризация ацетиленовых углеводородов при нагр. в присуг. оснований:
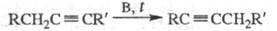
В = NaOH, KOH, Na, K2CO3
Направление р-ции существенно зависит от условий и строения исходного ацетилена. Напр., нагревание со спиртовой щелочью приводит к перемещению тройной связи в середину цепи, а нагревание с Na - к образованию ацетиле-нидов:
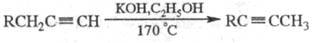
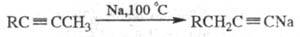
Наличие в молекуле Ar, R2N или группы COOH обычно облегчает изомеризацию (напр., достаточно использование K2CO3 при 40-90 0C или Na при 20 0C). Однозамещенные ацетилены с втор-алкильными радикалами изомеризуются в аллены (промежут. продукты Фаворского реакции; образуются во всех случаях в преобладающем кол-ве при понижении т-ры р-ции); соед. с трет-алкильными радикалами не изомеризуются.
Изомеризация - результат дважды реализующейся прото-тропной аллильной перегруппировки.
Перегруппировка открыта A. E. Фаворским в 1887.
Лит.: Темникова Т.Н., Курс теоретических основ органической химии, 2 изд., Л., 1962, с. 529-32; Wartanjan S. А., Badanjan S. О., "Angew. Chern.", 1963, Bd 75, S. 1034. Г. И. Дрозд.
