Галловая кислота
ГАЛЛОВАЯ КИСЛОТА (3,4,5-тригидроксибензойная к-та), мол. м. 170,11. Существует в виде моногидрата, обезвоживающегося при 100-120 °С; бесцв. кристаллы, темнеющие на свету; т. пл. 220°С (лабильная модификация), 240°С (с разл.; стабильная модификация); d461,694;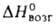 74,21 кДж/моль; рКа 4,40 (25 °С). Р-римость (г в 100мл р-рителя): в воде - 1,16 (25 °С), 33 (100°С); этаноле-27,2 (25 °С); эфире-2,5 (15°С).
74,21 кДж/моль; рКа 4,40 (25 °С). Р-римость (г в 100мл р-рителя): в воде - 1,16 (25 °С), 33 (100°С); этаноле-27,2 (25 °С); эфире-2,5 (15°С). 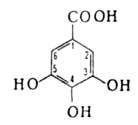
Обладает всеми св-вами гидроксикарбоновых к-т (см. Оксикислоты). Наиб. реакционноспособна ОН-группа в положении 4; напр., при метилировании диметилсульфатом в присут. 2 молей NaOH образуется 3,5-дигидрокси-4-метоксибензойная к-та, а в присут. 5 молей ЫаОН-3,4,5-триметоксибензойная к-та. Галловая кислота восстанавливает, напр., соли Аи и Ag до металлов, Fe2+ до Fe3+ . Щелочные соли галловой кислоты под действием О2 темнеют. Сухой перегонкой над пемзой в токе СО2 при 190-215 °С галловая кислота декарбоксилируется до пирогаллола. При нагр. ее с конц. H2SO4 образуется гексагидроксиантрахи-нон (руфигалловая к-та):
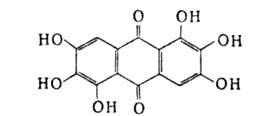
Галловая кислота в виде сложных эфиров содержится в таннинах чернильных орешков (галлов), растений сумаха и чая, а также дубовой коры. Получают ее щелочным или ферментативным гидролизом таннинов.
Цветная р-ция: сине-черное окрашивание с FeCl3. Галловую кислоту применяют в произ-ве пирогаллола, лек. в-в, красителей (галлофлавина, антрагаллола и др.), как реагент для отделения и фотометрич. определения Bi(III) и Се(Ш), как цветеобразующую компоненту в тсрмочувствит. копировальных бумагах. Сложные эфиры галловой кислоты- антиоксиданты жиров и масел. Галловая кислота открыта К. Шееле в 1786 в вытяжках из чернильных орешков. Н.Н.Артамонова.
