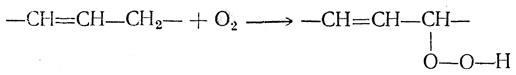II. Реакции окисления
Многие этиленовые углеводороды имеют склонность медленно окисляться кислородом воздуха, и вообще этиленовые соединения весьма чувствительны к действию окислителей, которое почти всегда направляется именно на этиленовую связь.
При осторожном действии на этиленовые углеводороды перманганата в щелочном растворе по двойной связи присоединяются атом кислорода и молекула воды и получаются двухатомные спирты, или гликоли (Е. Е. Вагнер), например:
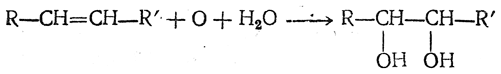
Еще легче получаются гликоли при нагревании олефинов с перекисью водорода в присутствии муравьиной кислоты; при этом сначала образуется надмуравьиная кислота
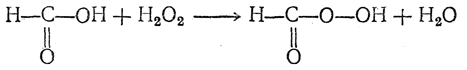
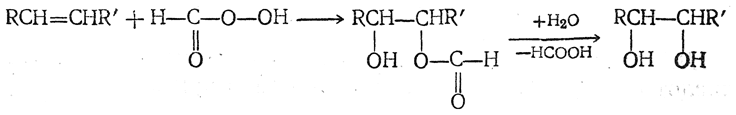
которая и присоединяется к олефину, давая после гидролиза гликоль:
При 150—350° С низшие олефины в газовой фазе окисляются воздухом над катализатором (серебром или золотом), образуя окиси олефинов, например:
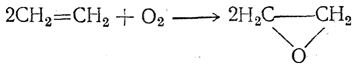
Олефины образуют окиси также и в растворах при низкой температуре под действием гидроперекисей кислот, в частности гидроперекиси бензоила (реакция Прилежаева):
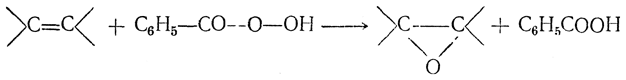
При более энергичном действии окислителей на этиленовые углеводороды цепь атомов углерода разрывается по месту двойной связи и получаются, в зависимости от строения исходного углеводорода, или органические кислоты, или кетоны. Так, например, триметилэтилен (СН3)2С=СН—СН3 расщепляется с образованием ацетона и уксусной кислоты; углеводород строения R—СН=СН—R' дает две кислоты: R—СООН и R'—СООН. Ввиду этого реакции окисления очень часто применяются для определения строения ненасыщенных соединений. Окисление перманганатом в нейтральной или щелочной среде применяется как качественная реакция на кратные связи (раствор перманганата моментально обесцвечивается с выделением бурой перекиси марганца). Этиленовые углеводороды гладко окисляются тетраацетатом свинца и осмиевым ангидридом; при этом двойная связь разрывается и образуются гликоли с тем же числом атомов углерода. Окисление в жидкой фазе кислородом или воздухом, вопреки прежним представлениям, направляется не на атомы углерода, связанные двойной связью, а на атом углерода, соседний с двойной связью; при этом первичными продуктами окисления оказываются непредельные перекисные соединения: