Бромметан
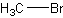
Синонимы:
метил бромистыйметилбромид
Внешний вид:
бесцветн. газБрутто-формула (система Хилла): CH3Br
Формула в виде текста: CH3Br
Молекулярная масса (в а.е.м.): 94,94
Температура плавления (в °C): -93,6
Температура кипения (в °C): 3,56
Растворимость (в г/100 г или характеристика):
бензол: растворимвода: 0,09 (20°C)
диэтиловый эфир: легко растворим
сероуглерод: смешивается
хлороформ: растворим
этанол: легко растворим
Метод получения 1.
(лабораторный синтез)Источник информации: Юрьев Ю. К. "Практические работы по органической химии" вып.3 2-е изд. М., 1964 стр. 226-227
В круглодонную колбу на 150—200 мл помещают 16,5 мл концентрированной серной кислоты и при непрерывном перемешивании и охлаждении колбы водой приливают небольшими порциями 10 мл метилового спирта и после этого 10 мл воды. Затем прибавляют 15 г тонко растертого бромистого калия и закрывают колбу резиновой пробкой со вставленным в нее обратным шариковым холодильником.
Верхний конец форштосса обратного холодильника закрывают резиновой пробкой со вставленной в нее изогнутой вниз стеклянной трубкой, к которой присоединяют прамыз-ную склянку Тищенко с 20%-ным раствором едкого натра; к этой склянке присоединяют еще одну склянку Тищенко с концентрированной серной кислотой. Отводную трубку, присоединенную ко второй промывной склянке, вставляют в стеклянную ампулу, подготовленную для запаивания и сильно охлаждаемую смесью лед—соль.
Реакционную смесь нагревают на небольшой песочной бане. Выделяющийся бромистый метил проходит через обратный холодильник, промывную склянку с раствором щелочи (для очистки от бромистого водорода, сернистого ангидрида и паров брома), промывную склянку с концентрированной серной кислотой (для очистки от диметилового эфира и высушивания) и конденсируется в приемнике-ампуле. Интенсивность выделения бромистого метила регулируют, изменяя силу нагревания (при охлаждении до комнатной температуры реакция прекращается) так, чтобы реакция протекала равномерно, но не бурно; в этом случае можно заметить конец реакции (по ослаблению ее) и прекратить нагревание.
Бромистый метил сохраняют в запаянной ампуле.
Выход 8,5—9,5 г.
Плотность:
1,732 (0°C, г/см3)0,003974 (25°C, г/см3)
Показатель преломления (для D-линии натрия):
1,4432 (-20°C)1,4218 (20°C)
Давление паров (в мм.рт.ст.):
1420 (20°C)Дипольный момент молекулы (в дебаях):
1,786 (20°C)Стандартная энтальпия образования ΔH (298 К, кДж/моль):
-35,6 (г)Стандартная энергия Гиббса образования ΔG (298 К, кДж/моль):
-25,9 (г)Стандартная энтропия образования S (298 К, Дж/моль·K):
245,77 (г)Стандартная мольная теплоемкость Cp (298 К, Дж/моль·K):
42,59 (г)Энтальпия плавления ΔHпл (кДж/моль):
5,98Энтальпия кипения ΔHкип (кДж/моль):
23,91Теплота сгорания Qp (кДж/моль):
769,8Критическая температура (в °C):
192,6Критическое давление (в МПа):
6,94- "Справочник химика" т.2, Л.-М.: Химия, 1964 стр. 788-789
- Рабинович В.А., Хавин З.Я. "Краткий химический справочник" Л.: Химия, 1977 стр. 160
