Зандмейера реакция
ЗАНДМЕЙЕРА РЕАКЦИЯ, замена диазониевой группы в ароматич. солях диазония на галоген или псевдогалоген в присут. солей Cu(I), напр.: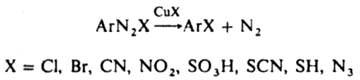
Для введения хлора или брома р-р соли диазония обычно добавляют при 0-35 °С к р-ру галогенида Cu(I) (от 0,1 до 1 моля на 1 моль диазосоединения) в галогеноводородной к-те. Выходы галогснидов 70-95%. Вместо солей меди можно применять порошок меди (р-ция Гаттермана) или соли др. металлов (напр., FeCl2). Иногда стадии диазотирования и замены диазониевой группы на галоген осуществляют без выделения промежут. продукта. Для введения нитрильной группы р-р соли диазония нейтрализуют, смешивают при охлаждении с р-ром комплексной соли Na [Сu (CN)2] или К [Сu (CN)2], затем нагревают. Выходы нитрилов обычно выше 60%. Скорость Зандмейера реакции увеличивается при введении электроноакцепторных и уменьшается при введении электронодонорных заместителей в ароматическое ядро. Побочные продукты при этой реакции - азосоединения, биарилы и фенолы. Предполагаемый механизм замены диазогруппы на галоген включает образование лабильного комплекса диазоний-катиона с солью Cu(I) (лимитирующая стадия), напр.:
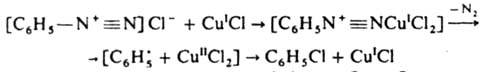
В ряду нафталина, фенантрена, бифенила Зандмейера реакция обычно дает низкие выходы галогенидов; в этих случаях используют термич. разложение двойных галогенидов диазония и ртути [ArN2]+ [HgHal3]- (р-ция Швехтена). Арилиодиды обычно получают нагреванием диазосоединений с р-ром KI, арилфториды - по Шимана реакции. Зандмейера реакцию используют для пром. синтеза промежут. продуктов в произ-ве орг. красителей, напр. 8-хлор- и 8-цианонафталин-1-сульфокислот, хлортолуолов, 2-цианофенилтиогликолевых к-т. Р-ция открыта Т. Зандмейером в 1884.
Литература
Эфрос Л. С., Горелик М. В., Химия и технология промежуточных продукгов. Л., 1980. с. 334-40. Е. М. Рохлин.
Синонимы/примеры:*
Реакция Зандмейера; Реакция Зандмайера
*подобраны ИИ, возможны неточности
Ещё по теме
Зандмейера реакция — особенности и применение
Диазосоединения — свойства и применение
Несмеянова реакция — особенности и применение
Диазотирование — реакция и применение в органическом синтезе
Методы обнаружения ионов металлов в химико-токсикологическом анализе
Реакция Розенмунда — особенности и применение
Диазометан — характеристики и применение
Диазотаты — свойства и применение
