Поверхностная активность
ПОВЕРХНОСТНАЯ АКТИВНОСТЬ, способность в-ва при адсорбции на границе раздела фаз понижать поверхностное натяжение (межфазное натяжение). Адсорбция Г в-ва и вызванное ею понижение поверхностного натяжения s связаны с концентрацией с в-ва в фазе, из к-рой в-во адсорбируется на межфазную пов-сть, ур-нием Гиббса (1876):

где R-газовая постоянная, Т-абс. т-ра (см. Адсорбция). Производная 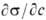 служит мерой способности в-ва понижать поверхностное натяжение на данной межфазной границе и также наз. поверхностной активностью. Обозначается G (в честь Дж. Гиббса), измеряется в Дж·м/моль (гиббсах).
служит мерой способности в-ва понижать поверхностное натяжение на данной межфазной границе и также наз. поверхностной активностью. Обозначается G (в честь Дж. Гиббса), измеряется в Дж·м/моль (гиббсах).
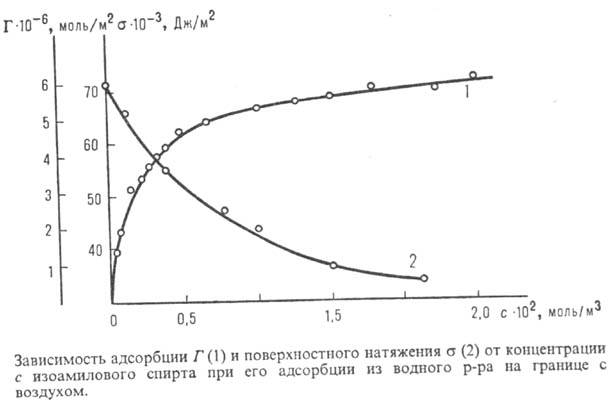
Поверхностную активность определяют с помощью изотерм адсорбции, на к-рых можно выделить линейный участок роста Г с увеличением с и предельное значение 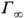 , соответствующее насыщению адсорбц. слоя (см. рис.). Согласно ур-нию Ленгмюра, при достаточно малых с линейный участок изотермы м. б. описан ур-нием
, соответствующее насыщению адсорбц. слоя (см. рис.). Согласно ур-нию Ленгмюра, при достаточно малых с линейный участок изотермы м. б. описан ур-нием 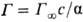 , к-рое совместно с ур-нием Гиббса позволяет вычислить поверхностную активность:
, к-рое совместно с ур-нием Гиббса позволяет вычислить поверхностную активность:
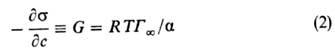
(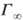 и a-эмпирич. постоянные, наз. константами Ленгмюра). Ур-ние Ленгмюра справедливо для пов-стей раздела жидкость-пар и жидкость - жидкость, а также в случаях адсорбции газа на твердых, в т. ч. пористых, телах. Определяемое по этому ур-нию значение поверхностной активности является постоянной величиной для данного в-ва и данной границы раздела фаз.
и a-эмпирич. постоянные, наз. константами Ленгмюра). Ур-ние Ленгмюра справедливо для пов-стей раздела жидкость-пар и жидкость - жидкость, а также в случаях адсорбции газа на твердых, в т. ч. пористых, телах. Определяемое по этому ур-нию значение поверхностной активности является постоянной величиной для данного в-ва и данной границы раздела фаз.
В случае адсорбции в-ва из р-ра поверхностная активность определяется на основании эмпирич. ур-ния Шишковского (1908):
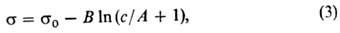
где s0 - поверхностное натяжение чистого р-рителя, В -эмпирич. постоянная, практически не зависящая от природы в-ва и равная примерно 0,2 при 293 К, 1/А-уд. капиллярная постоянная, характеризующая природу в-ва (см. Капиллярные явления). После дифференцирования ур-ние (3) принимает вид:

Ур-ние Шишковского позволяет определять поверхностную активность данного в-ва более строго, чем ур-ние Ленгмюра, из-за отсутствия концентрац. ограничений. Третьим ур-нием, используемым для определения поверхностной активности, является ур-ние изотермы адсорбции Фрумкина (1949):
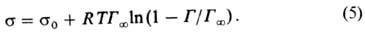
Все три ур-ния - Ленгмюра, Шишковского и Фрумкина - являются частными случаями ур-ния Гиббса (1).
При прочих равных условиях (т-ра, состав р-ра) поверхностная активность в-ва зависит в первую очередь от состава и строения молекул.
Наибольшей поверхностной активностью обладают, как показали в 1916-17 И. Ленг-мюр и У. Харкинс, в-ва, молекулы к-рых дифильны, т. е. состоят из полярных и неполярных частей. Такие в-ва наз. поверхностно-активными веществами (ПАВ). Полярная (гидрофильная) часть молекулы при адсорбции ориентируется в сторону полярной фазы (обычно воды), неполярная часть - углеводородный радикал - выталкивается из полярной фазы, ориентируясь в направлении менее полярной фазы, напр. воздуха, углеводородных или др. орг. жидкостей. Молекулы ПАВ образуют при адсорбц. насыщении как бы двухмерную (мономолекулярной толщины) кристал-лич. решетку. Это дает возможность определять размеры и структуру адсорбирующихся молекул и устанавливать их связь с поверхностной активностью (см. Мономолекулярный слои).
Осн. параметры адсорбц. слоя ПАВ, помимо уже упоминавшейся поверхностной активности 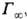 -это
-это 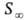 -площадь, занимаемая одной молекулой, и d-высота "частокола", образованного неполярными частями молекул. Значение
-площадь, занимаемая одной молекулой, и d-высота "частокола", образованного неполярными частями молекул. Значение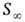 зависит от природы границы раздела фаз и равно:
зависит от природы границы раздела фаз и равно:

где NА - постоянная Авогадро. Значение d связано с массой M 1 моля в-ва в адсорбц. слое при насыщении:

где d- плотность в-ва в адсорбц. слое, равная его плотности в чистом состоянии. Из (6) и (7) следует:
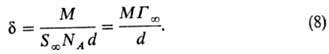
При адсорбции в-в, относящихся к одному гомологич, ряду, переход от одного члена ряда к следующему изменяет d на постоянную величину, равную длине звена CH2. Чем длиннее неполярная часть молекулы, тем сильнее ее склонность к ориентации. По этой причине поверхностная активность ПАВ возрастает с увеличением длины углеводородного радикала. Согласно эмпирич. правилу Дюкло-Траубе, при одинаковой концентрации в р-ре ПАВ его поверхностная активность возрастает в 3-3,5 раза при увеличении углеводородной цепи на одну группу CH2. Это значение подтверждается расчетом изменения работы переноса молекулы ПАВ из объема р-ра на межфазную границу для двух соседних гомологов.
Для р-ров ПАВ в неполярных р-рителях на границе с воздухом, в отличие от водных р-ров, с увеличением длины углеводородного радикала р-римость ПАВ возрастает. При адсорбции из углеводородного р-рителя на границе с водой размер углеводородного радикала практически не влияет на поверхностную активность. Напр., для жирных к-т работа адсорбции определяется переносом гл. обр. группы COOH из объема неполярной среды на границу раздела фаз. Аналогично протекает адсорбция жирных к-т из неполярных р-рителей на твердых полярных адсорбентах, напр. силикагеле. С увеличением мол. массы к-ты адсорбция даже уменьшается, т. к. высшие жирные к-ты лучше растворимы в неполярной среде, чем в воде. Адсорбция ПАВ из воды на неполярных адсорбентах подчиняется правилу Дюкло-Траубе. Отсюда следует, что чем меньше р-римость в-ва в к.-л. среде, тем больше его поверхностная активность на границе с этой средой. Так, поверхностная активность анилина на границе вода-толуол, вычисленная с водной стороны: GH2O = = 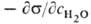 , примерно в 7-8 раз выше, чем
, примерно в 7-8 раз выше, чем 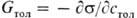 из-за различия р-римости анилина в указанных фазах.
из-за различия р-римости анилина в указанных фазах.
С повышением т-ры поверхностная активность любых в-в уменьшается вследствие десорбции.
Лит.: Абрамзон А. А., Поверхностно-активные вещества. Свойства и применение, 2 изд., Л., 1981; Успехи коллоидной химии, под ред. П. А. Ребиндера и Г. И. Фукса, M., 1973; то же, под ред. Ф. Д. Овчаренко, К., 1983; то же, под ред. И. В. Петрянова-Соколова и К. С. Ахмедова, Ташкент, 1987. В. П. Тихонов.
