Историческое отступление
Мы обещали касаться только вполне современных методов исследования, и не без оснований: классику легко найти в любом учебнике. И все-таки хочется отсупить от этого принципа и описать методы, с помощью которых были впервые выяснены конфигурации ассиметрических центров важнейших моносахаридов. Это – классическая работа Эмиля Фишера. Изложим ее несколько упрощенно, стремясь сохранить главное – логику исследования.
Прежде всего о том, что уже было известно Фишеру и что предстояло узнать. Была известна бутлеровская структура (см. с. 8) нескольких моносахаридов, было также известно, что для некоторых из них возможны взаимные превращения путем определенных реакций и что изомерные альдозы отличаются конфигурацией ассиметричемких центров. Установить же нужно было относительные конфигурации этих центров. Экспериментально Фишер использовал главным образом две реакции.
1. Циангидриновый синтез, т.е. присоединение к альдозам синильной кислоты с последующим гидролизом нитрильной группы и восстановлением карбоксильной до альдегидной. Результатом этой реакции является удлинение углеродной цепи альдозы на одно звено и возникновение нового ассиметрического центра, вследствие чего из каждого моносахарида получается не один, а два новых моносахарида – стереоизомеров по C-2. В общем виде эта последовательность показана на схеме:
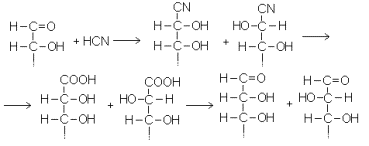
2. Окисление азотной кислотой. При этом и альдегидная группа, и концевое CH 2 OH-звено окисляются до карбонильных групп. В результате молекула приобретает повышенную симметрию – происходит уравнивание концов, причем в зависимости от относительной конфигурации ассиметрических центров эта симметрия может оказаться полной или неполной. Ниже эта реакция показана на примере D-галактозы:
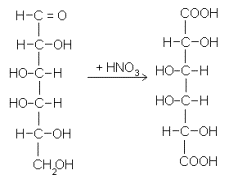
Фишер располагал тремя альдозами: глюкозой, маннозой и арабинозой. Для последней, если оперировать с сахарами D-ряда, принципиально возможны четыре конфигурации (4-7):
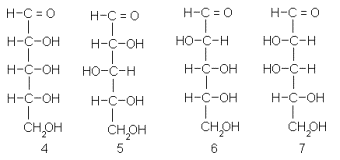
После окисления арабинозы азотной кислотой Фишер получил оптически деятельную, следовательно ассиметричную дикарбоновую кислоту. Это сразу исключало две структуры из четырех возможных. В самом деле, ожидаемые продукты из четырех возможных пентоз следующие (8-11):
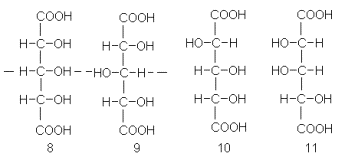
Первые две из этих кислот обладают плоскостью симметрии (указана на схеме пунктиром) и, значит, должны быть оптически неактивны. Таким образом, этот эксперимент оставлял для кислоты только две возможные структуры: 10 и 11, а для арабинозы – только 6 и 7.
Путем циангидринного синтеза из арабинозы были получены две гексозы: глюкоза и манноза. Из этого следовало, что у последних конфигурация центров при C-3, C-4 и C-5 такая же, как в арабинозе (у ее C-2, C-3 и C-4 соответственно), и что различия между глюкозой и маннозой сводятся только к различию конфигурации C-2. Таким образом, глюкозе и маннозе могут соответствовать либо пара конфигураций 12 и 13 (если арабиноза- это 6), либо пара 14 и 15 (если арабиноза – это 7).
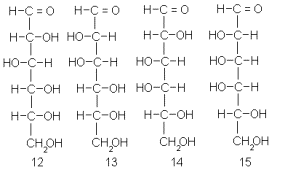
Для выбора между этими парами Фишер опять применил принцип уравнивания концов. Четырем гексозам 12-15 соответствуют четыре дикарбоновые кислоты (16-19):
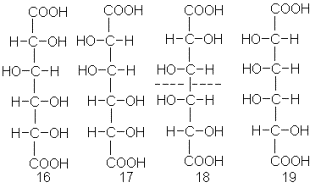
Из этих четырех кислот только одна – 18 – обладает плоскостью симметрии и, следовательно, оптически недеятельна. Окислив глюкозу и маннозу, Фишер получил две оптически активные кислоты. Таким образом, глюкозе и маннозе не может соответствовать пара конфигураций 14 и 15, а соответствует только пара 12 и 13. Следовательно, для арабинозы (из которой, как мы помним, могут быть получены эти две гексозы) остается только одна возможная структура – 6.
Теперь Фишер уже знал, что глюкоза и манноза имеют конфигурацию 12 и 13, но еще не знал, какая из этих конфигураций отвечает глюкозе, а какая маннозе. Вопрос был решен аналогичным образом: последовательным применением циангидринного синтеза и окисления, которые приводили к образованию C 7 -дикарбоновых кислот. Из маннозы при этом были получены две оптически активные кислоты, что возможно только при исходной конфигурации 13 (читатель может сам вывести их структуры и доказать асимметрию), а из глюкозы – две кислоты одна из которых была оптически недеятельна. Такая симметричная структура – кислота 20 –могла возникнуть только из гексозы с конфигурацией 12. Таким образом, и последний вопрос этой серии – конфигурация глюкозы и маннозы – был блестяще разрешен Фишером.
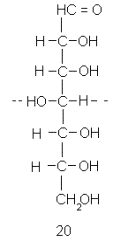
Позднее аналогичным образом он установил относительные конфигурации остальных основных пентоз и гексоз и тем самым впервые создал научную основу всей химии углеводов.
Работа Фишера, опубликованная в 1891 году, даже по сегодняшним меркам должна быть оценена как первоклассное исследование – по безукоризненной логике, тщательности экспериментального выполнения и полной строгости и надежности заключений. В настоящее время асимметрия насыщенного углеродного атома есть не вызывающая сомнений школьная истина. Однако во времена Фишера это была лишь сравнительно недавно сформулированная (Вант-Гоффом и Ле Белем в 1874 г.) стереохимическая гипотеза, имевшая очень немного экспериментальных подтверждений даже для очень простых систем, содержащих один-два ассиметрических атома. Нужна была глубокая убежденность в ее справедливости, глубокая уверенность в применимости строгой логики к сложным органическим соединениям и в надежности и однозначности превращений, чтобы задумать, предпринять и блестяще довести до конца такое (кстати сказать, экспериментально весьма сложное) исследование. Поэтому работу Эмиля Фишера по установлению конфигурации моносахаридов смело можно отнести к истинно гениальным творениям, которые не только приводят к блистательным конкретным результатам, но и освещают путь своим глубоким идейным содержанием новые пути в целой области науки. Начиная с этой работы стереохимическая гипотеза превратилась в стереохимическую теорию – одно из наиболее фундаментальных обобщений органической химии.
Логический приемы, введенные Фишером, широко используются в структурных исследованиях до сих пор (правда, на иной химической основе). Приведем здесь только два примера, в основу которых положено уравнивание концов: сведение D-арабинозы (21) и D-ликсозы (7) к одному и тому же полиолу (22), и идентификацию 3,4-ди-О-метил-D-ксилозы (23), для которой заведомый образец труднодоступен, в виде полиола 24 с его оптическим антиподом 25, который образуется из более доступной 2,3-ди-О-метил-D-ксилозы (26):
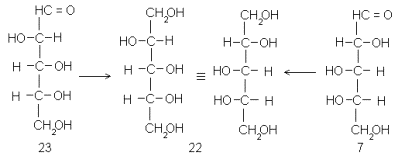
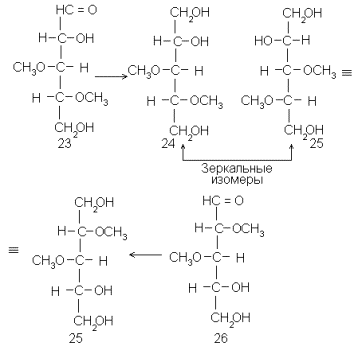
В обоих примерах для перехода от альдоз к полиолам использовано восстановление боргидридом натрия. Видно, что в обоих случаях, при всем внешнем несходстве, применена стереохимическая логика, заимствованная из работы Фишера.
Теперь поясним, как устанавливают структуру и конфигурации моносахаридов и их метилированных производных в современных работах. Здесь решающую роль играют два метода – осколочная масс-спектрометрия для установления структур (без стереохимии) и спектроскопия ядерного магнитного резонанса (ЯМР) для выяснения конфигураций ассиметрических центров.


