Орнитин
ОРНИТИН (2,5-диаминопентановая к-та, 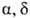 -диаминова-лериановая к-та, Orn) H2N(CH2)3CH(NH2)COOH, мол. м. 132,16; бесцв. кристаллы; т. пл. D-орнитина и L-орнитина 140 °С, гидрохлорида D, L-орнитина 233 °С (с разл.); для L-орнитина
-диаминова-лериановая к-та, Orn) H2N(CH2)3CH(NH2)COOH, мол. м. 132,16; бесцв. кристаллы; т. пл. D-орнитина и L-орнитина 140 °С, гидрохлорида D, L-орнитина 233 °С (с разл.); для L-орнитина 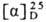 + 11,5° (6,5 г в 100 мл воды); раств. в воде и этаноле, плохо раств. в диэтиловом эфире. При 25 °С для L-орнитина рКа 1,94 (СООН), 8,65 (2-NH2) и 10,76 (5-NH2); pI 9,74.
+ 11,5° (6,5 г в 100 мл воды); раств. в воде и этаноле, плохо раств. в диэтиловом эфире. При 25 °С для L-орнитина рКа 1,94 (СООН), 8,65 (2-NH2) и 10,76 (5-NH2); pI 9,74.
По хим. св-вам орнитин - сильноосновная а-аминокислота. Для проведения селективных р-ций по 5-аминогруппе используют медную соль орнитина. С к-тами орнитин дает два ряда солей, напр, с НСl - гидрохлорид и дигидрохлорид. При действии на орнитин аммиака и СО2 образуется цитруллин H2NC(O)NH(CH2)3— —CH(NH2)COOH, декарбоксилирование орнитина приводит к пут-ресцину H2N(CH2)4NH2, при взаимод. H2NC(=NH)OCH3 с медной солью орнитина образуется аргинин. Синтез аргининсо-держащих пептидов м. б. осуществлен исходя из орнитина с превращ. 5-аминогруппы последнего на завершающей стадии в гуанидиногруппу.
Орнитин в незначит. кол-вах содержится в тканях человека и плазме крови; обнаружен также в нек-рых растениях. Он входит в состав антибиотиков-полипептидов: D-орнитин-в ба-цитрацин, D- и L-орнитин-в грамицидин S.
L-Орнитин-заменимая некодируемая аминокислота, в организме играет важную роль, особенно в биосинтезе мочевины (см. Орнитиновый цикл); его метаболизм тесно связан с пролином и оксипролином. В организме орнитин образуется при гидролизе аргинина, восстановит. аминировании 2-амино-4-формилмасляной к-ты (продукта восстановления глута-миновой к-ты); при окислит. отщеплении 5-аминогруппы орнитин может переходить в пролин.
Осн. путь биосинтеза: из глутаминовой к-ты через ее g-полуальдегид (5-оксо-2-аминопентановая к-та), переами-нирование к-рого приводит к орнитину. Синтетически орнитин может быть, напр., получен с выходом 85% по схеме:
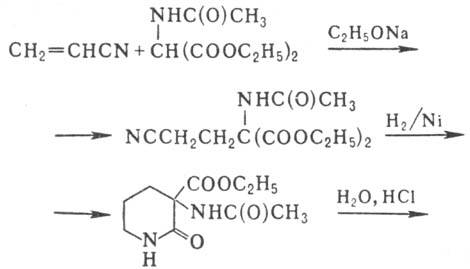
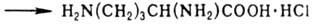
L-Орнитин впервые выделен из печени акулы в 1937 Д. Аккерма-ном, D-орнитин-из тироцидина в 1943 А. Гордоном. Мировое произ-во орнитина ок 50 т/год (1982)
В.В. Басе.
