Раймера-Тимана реакция
РАЙМЕРА-ТИМАНА РЕАКЦИЯ, получение ароматич. о-гидроксиальдегидов формулированием фенолов при нагр. с хлороформом и щелочью, напр.:
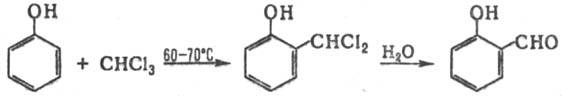
Р-цию обычно осуществляют в этаноле или пиридине. Наряду с о-гидроксиальдегидом, как правило, образуется незначит. кол-во пара-изомера, особенно в тех случаях, когда орто-положение в исходном феноле занято. Вместо СНС13 можно использовать др. галоформы-СНВr3 и СНI3.
В Раймера - Тимана реакцию вступают алкил-, алкокси- и галогенфенолы, причем легче всего реагируют соед., содержащие указанные заместители в пара-положении к гидроксигруппе. Выходы о-гидроксиальдегидов обычно меньше 50%. Наличие в ароматич. ядре электроноакцепторных заместителей (SO3H, СООН, NO2 и др.) затрудняет р-цию, и выходы ожидаемых продуктов обычно невелики. В случае о- и n-алкил(арил)-фенолов наряду с о-гидроксиальдегидами могут образовываться гем-производцые (аномальная Раймера - Тимана реакция), напр.:
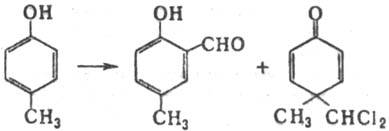
Механизм р-ции включает образование из СННаl3 под действием щелочи дигалогенкарбена, к-рый атакует фенолят-анион:
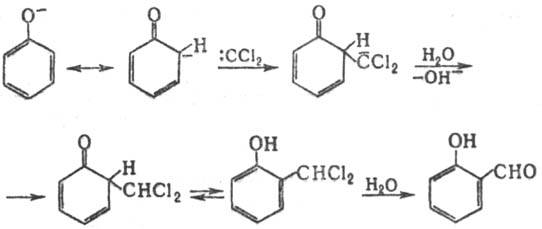
Формилирование фенолов возможно также действием на них галоформа при УФ облучении (т. наз. фотохимическая Раймера - Тимана реакция). В этом случае р-ция осуществляется по радикальному механизму (генерируются феноксильные радикалы и СННа12):
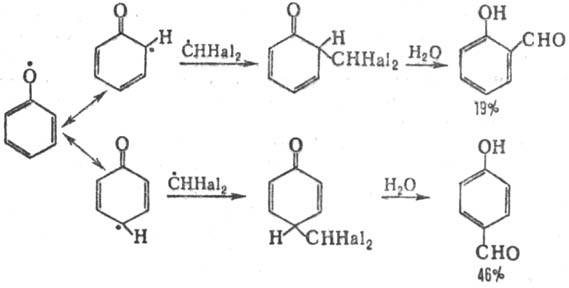
Аналогично происходит формилирование М.М-диалкиланилинов.
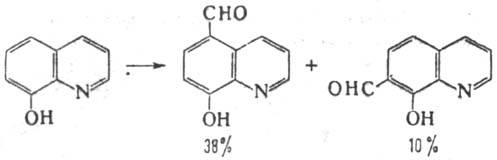
В р-цию, подобную Раймера - Тимана реакции, вступают также гидрокси-производные ряда нафталина, хинолина, трополона, тиазола и др., напр.
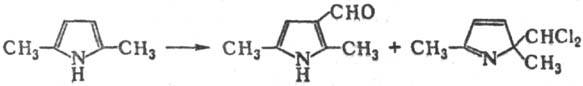
Изоэлектронные аналоги фенолов (пиррол, индол и их производные) реагируют с галоформами по механизму Раймера - Тимана реакции с образованием соотв. альдегидов, и гем-замещен-ных производных, напр.:
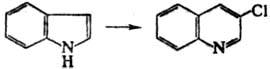
В нек-рых случаях в условиях Раймера - Тимана реакции наблюдалось расширение кольца вследствие внедрения дихлоркарбена (Ча-мичана-Деништедта р-ция), напр.:
Раймера - Тимана реакция находит практич. применение, напр., в пром. синтезе салицилового альдегида. Р-ция открыта К. Райме* ром и Ф. Тиманом в 1876.
Лит.: Трюс У.Э., в сб.: Органические реакции, пер. с англ., сб. 9, М., 1959, с. 45-81; Общая органическая химия, пер. с англ., т. 2. М., 1982, с. 711-12; Wynherg Н., "Cham. Rev.", 1960, v. 60, № 2, p. 169-84; Organic reactions, v. 28, N.Y., 1982, p. 1. Л.А. Хейфиц.
