Салициловый альдегид
САЛИЦИЛОВЫЙ АЛЬДЕГИД (2-гидроксибензальдегид), мол. м. 122,1; бесцв. жидкость с запахом горького миндаля; т.пл. -7°С,т.кип. 197°С, 93 °С/25 мм рт. ст.; 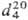 1,1674;
1,1674; 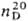 1,5740; m 9,539·10-30 Кл·м (бензол, 20 °С); e 17,09 (30 °С). Раств. в воде (1,72 г в 100мл при 8°С), бензоле (64,6 г в 100 мл при 12°С), диэтиловом эфире, этано ле. Перегоняется с водяным паром.
1,5740; m 9,539·10-30 Кл·м (бензол, 20 °С); e 17,09 (30 °С). Раств. в воде (1,72 г в 100мл при 8°С), бензоле (64,6 г в 100 мл при 12°С), диэтиловом эфире, этано ле. Перегоняется с водяным паром.
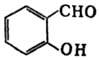
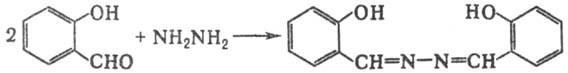
Обладает св-вами ароматич. альдегидов. Образует типичные для них производные: семикарбазон (т.пл. 231°С), фенилгидразон (т.пл. 143°С), оксим (т.пл. 57°С). С гидразином дает нерастворимый в воде салицилальдазин:
Характерное св-во салицилового альдегида-образование окрашенных комплексов с ионами металлов, напр.: с водным р-ром FeCl3-фиолетового цвета, с NaOH-желтого с сине-зеленой флуоресценцией при УФ облучении.
К окислению салициловый альдегид более устойчив, чем бензальдегид. Под действием Н2О2 в нейтр. среде окисляется до салициловой к-ты, в щелочной-до пирокатехина (р-ция Дейкина). Салициловый альдегид в присут. щелочи образует смесь о-гидроксибензилового (салицилового) спирта и салициловой к-ты; при взаимод. с (СН3СО)2О в присут. CH3COONa превращ. в кумарин (пром. способ получения).
В природе салициловый альдегид встречается в маслах нек-рых видов спиреи (Spiraea ulmaria, Spiraea digitata).
В пром-сти салициловый альдегид получают взаимод. о-крезола с РОСl3 или фосгеном при 120-150°С с послед. кислотным гидролизом образующихся фосфата или карбоната (способ Рашига); электролитич. восстановлением салициловой к-ты; р-цией фенола с уротропином и Н3ВО3 по Даффа реакции или с СНС13 в щелочной среде по Раймера-Тимана реакции.
Салициловый альдегид-исходный продукт в произ-ве кумарина, промежут. продукт в синтезе красителей, инсектицидов (напр., диок-сокарба); применяется в парфюмерии, для количеств. определения сивушного масла в этаноле, в орг. анализе.
Т. воспл. 530 °С, т. всп. 90 °С.
Лит.: Общая органическая химия, пер. с англ., т. 2, М., 1982, d 756; Hoyben-Weyl, Methoden der organischen Chemie, Bd 7, Tl 1, Stuttg., 1954; Ullmanns Encyklopadie, 4 Aufl., Bd 8, Weinheim, 1974, S. 349. H. Н. Артамонова.
