Фишера реакция
ФИШЕРА РЕАКЦИЯ, синтез индолов внутримол. конденсацией арилгидразонов в присут. кислых агентов:
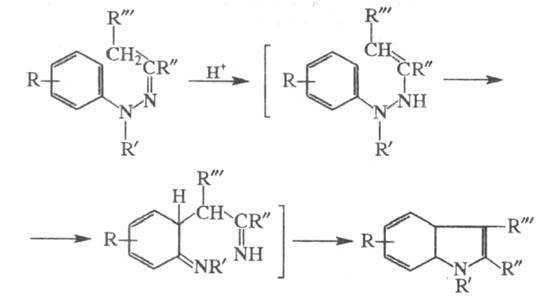
Фишера реакцию проводят, как правило, при нагр. р-ра арилгидразона в присут. протонной к-ты или к-ты Льюиса. Иногда ее осуществляют в присут. оснований, солей переходных металлов или термически.
В р-цию вступают арилгидразоны разл. альдегидов (труднее всего уксусного) и кетонов; электроноакцепторные заместители в арильном ядре неск. затрудняют р-цию. Циклизация мета-замещенных фенилгидразонов приводит к смеси изомерных 4- и 6-замещенных индолов.
Считается общепринятым, что ключевой стадией процесса является кислотно-катализируемая перегруппировка енгидра-зинной формы арилгидразона по схеме 3,3-сигматропного сдвига (т. наз. 3,4-диазаперегруппировка Коупа; см. также Коупа перегруппировка)с последующей ароматизацией 6-членного и замыканием пиррольного циклов.
Частные примеры Фишера реакции- синтез триптаминов и гомотриптаминов:
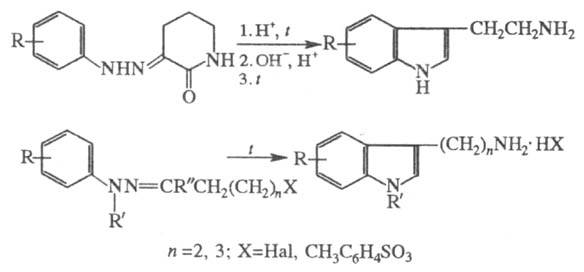
Близкие аналоги Фишера реакции- р-ция Бухерера - получение бензо-карбазолов при нагр. нафтолов и арилгидразинов с NaHSO3, а также синтез гидроксииндолов по Брукнеру (циклизацией N-ацил-N'-арилгидразинов) и a-аминоиндолов по Косту из N-ацил-N'-арилгидразинов (см. также Коста-Сагитуллина перегруппировка, Бухерера реакции}.
Р-ция открыта Э. Фишером в 1883.
Кроме этой р-ции Фишером было открыто еще неск. р-ций, также носящих его имя: 1) получение арилгидразинов восстановлением солей арилдиазония сульфитами щелочных металлов (1875); 2) образование озазонов при нагр. моносахаридов с избытком арилгидразина (1884); 3) получение О-алкилгли-козидов при нагр. моносахаридов со спиртами в кислой среде (1893); 4) получение сложных эфиров при взаимод. карбоно-вых к-т со спиртами в присут. минер. к-т (совместно с А. Шпайером; 1895); 5) синтез ацеталей при взаимод. альдегидов со спиртами в присут. HCl (1897); 6) синтез 2-дезокси-сахаров из моносахаридов (1914); 7) получение мочевой к-ты из псевдомочевой циклодегидратацией под действием к-т (1895); 8) синтез 2,5-диарилоксазолов кислотной конденсацией ароматич. альдегидов с нитрилами a-гидроксикислот (1896); 9) получение дипептидов гидролитич. расщеплением 2,5-дикетопиперазинов (1901); 10) синтез пептидов взаимод. хлорангидридов  галогенкарбоновых к-т с
галогенкарбоновых к-т с аминокислотами или их эфирами с послед. гидролизом и аммонолизом.
аминокислотами или их эфирами с послед. гидролизом и аммонолизом.
Лит.: Вацуро К.В., Мищенко Г.Л., Именные реакции в органической химии, M., 1976, с. 416-22; Пр жевал ьский Н.М. [и др.], Химия гетеро-циклич. соединений, 1988, № 7, с. 867-80. В.Н. Дрозд.
