Хлораты
ХЛОРАТЫ, соли хлорноватой к-ты НСlO3. Анион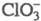 имеет структуру тригон. пирамиды, длина связей Сl — О 0,1452-0,1507 нм, угол ОС1О 106°. Анион С1О3 не образует ковалентных связей через атом О и не склонен образовывать координац. связи. Существует неск. соед., к-рые также относят к хлоратам, в них группа СlO3 связана ковалентно через атом С1 -FСlO3,
имеет структуру тригон. пирамиды, длина связей Сl — О 0,1452-0,1507 нм, угол ОС1О 106°. Анион С1О3 не образует ковалентных связей через атом О и не склонен образовывать координац. связи. Существует неск. соед., к-рые также относят к хлоратам, в них группа СlO3 связана ковалентно через атом С1 -FСlO3,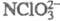 , С6Н5С1O3 и др.
, С6Н5С1O3 и др.
Хлорноватая к-та НС1О3 известна только в водном р-ре, предельная концентрация ок. 30%, попытка получить более конц. к-ту вакуумной отгонкой приводит к разложению и иногда взрыву; рКа -2,7;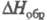 в бесконечно разб. водном р-ре -95,23 кДж/моль; при 18 oС плотн. 7,23%-ного р-ра 1,0421, 13,57%-ного 1,0829 и 25,87%-ного 1,1713 г/см3. НС1О3 легко восстанавливается до НС1, напр.:
в бесконечно разб. водном р-ре -95,23 кДж/моль; при 18 oС плотн. 7,23%-ного р-ра 1,0421, 13,57%-ного 1,0829 и 25,87%-ного 1,1713 г/см3. НС1О3 легко восстанавливается до НС1, напр.:

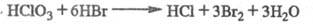
В слабокислой среде H2SO3 восстанавливает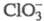 до Сl-, но при пропускании SO2, разбавленного воздухом, в сильнокислый р-р идет р-ция:
до Сl-, но при пропускании SO2, разбавленного воздухом, в сильнокислый р-р идет р-ция:
2HC1O3+H2SO3 2C1O2 + H2SO4 + H2O
2C1O2 + H2SO4 + H2O
Взаимод. солей Fе(II) в среде 5М Н3РО4 или H2SO4 с хлорат-ионом идет при 70-80 °С в присут. OsO4 и используется для количеств. определения хлоратов:

В сильнокислой среде устанавливается равновесие:

С ростом т-ры константа равновесия увеличивается от 0,038 (10 °С) до 0,073 (60 °С). При избытке Сl- возрастает вклад р-ции:
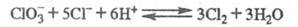
Получают НСlO3 действием H2SO4 на р-р Ва(СlO3)2 или в ионообменных колонках.
Хлораты - энергичные окислители как в р-ре, так и в твердом состоянии: смеси безводных хлоратов с S, углем и др. в-вами, способными окисляться, детонируют при быстром нагревании и ударе. Хотя хлор в хлоратах находится не в высшей степени окисления, окислить до
до в водном р-ре удается только электрохимически или под действием XeF2. O3 не окисляет хлораты до перхлоратов. В виде гидратов известны хлораты большинства металлов, в безводном состоянии выделены хлораты щелочных и щел.-зем. металлов, Ag, Тl(II), Рb(II), а также NH4Cl3, N(CH3)4C1O3 и т. п. Хлораты металлов переменной валентности, как правило, неустойчивы и склонны к взрывному распаду.
в водном р-ре удается только электрохимически или под действием XeF2. O3 не окисляет хлораты до перхлоратов. В виде гидратов известны хлораты большинства металлов, в безводном состоянии выделены хлораты щелочных и щел.-зем. металлов, Ag, Тl(II), Рb(II), а также NH4Cl3, N(CH3)4C1O3 и т. п. Хлораты металлов переменной валентности, как правило, неустойчивы и склонны к взрывному распаду.
Все хлораты щелочных металлов (табл.) разлагаются экзотермически на МС1 и О2 с промежут. образованием перхлоратов. Оксиды переходных металлов - MnO2, Fe2O3, CoO, NiO и др., а также Na2O2 катализируют распад хлоратов, снижая т-ру разложения на 100-200 °С. Выше 300 °С хлораты щелочных металлов имеют небольшое собств. давление пара и м. б. возогнаны. О св-вах NaClO3 см. Натрия хлорат.
СВОЙСТВА ХЛОРАТОВ ЩЕЛОЧНЫХ МЕТАЛЛОВ
| Показатель | LiClO3 | NaC1O3 | КСlO3 | RbClO3 | CsClO3 |
| Сингоння | _ | Кубич. | Моноклинная | Гексагoн. | Гексагон. |
| Пространств. группа | — | Р213 | Р21/т | R3m | R3m |
| Т. пл., °С | 129 | 263 | 357 | 342 | 388 |
| Т-ра начала разложения, oС | 367 | 465 | 472 | 480 | 483 |
| Плотн., г/см3 | 2,631 | 2,493 | 2,338 | 3,203 | _ |
| С0p Дж/(моль x К) | — | 100,1 | 100,3 | 103,2 | 104,6 |
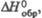 кДж/моль кДж/моль | -368,3 | -357,7 | -389,1 | -394,3 | -406,8 |
| Р-римость в воде, г в 100г | 406,3 | 95,89 | 8,58 | 6,61 | 7,60 |
Хлорат лития LiClO3 гигроскопичен; образует гидраты: LiC1O3-3H2O (т. пл. 8,5 °С), LiClO3 x H2O (т. пл. 20,5 oС, с разл.), LiClO3 x 0,25 Н2О (т. пл. 42 °С, с разл.). Эвтектич. смесь LiClO3 - NaClO3 имеет т. пл. 107,1 °С и содержит 69% LiС1O3. Бертоллетова соль КС1O3 при 250 °С переходит из моноклинной в ромбич. модификацию; негигроскопична, гидратов не образует; р-римость КС1O3 в воде при 100 °С достигает 56,0 г в 100 г; выше 220 °С реагирует с газообразным NH3, образуя KNO3, KC1, С12 и Н2О. Смеси КС1O3 с солями аммония и гидразония могут самовоспламеняться при хранении.
Хлорат магния Mg(ClO3)2 очень гигроскопичен; р-римость в воде при 25 °С 142 г в 100 г; образует гидраты: Mg(ClO3)2 x 2H2O (разлагается с частичной дегидратацией выше 100 oC), Mg(C1O3)2 x 4H2O (т. пл. 65,7 °С), Mg(ClO3)2 x 6H2O (т. пл. 34,2 °С), Mg(C1O3)2 x 12H2O (т. пл. -7,5 °С). Образует также кристаллич. комплекс с мочевиной Mg(ClO3)2 x 6CO(NH2)2. Хлорат кальция Са(С1O3)2 гигроскопичен; дает гидраты: Са(С1О3)2 x 2Н2О (т. пл. 76 °С), Са(С1O3)2 x 4Н2О (т. пл. -7,8 °С) и Са(С1O3)2 x 6Н2О (т. пл. -26,8 °С), все они плавятся инконгруэнтно; р-римость в воде при 25 °С 194,5 г в 100 г;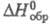 - 710,0 кДж/моль; получают хлорированием известкового молока при 70-80 °С. Хлорат бария Ва(С1O3)2 - кристаллы ромбич. сингонии (пространств. группа Fdd2); т. пл. 400 °С (с разл.; плотн. 3,347 г/см3;
- 710,0 кДж/моль; получают хлорированием известкового молока при 70-80 °С. Хлорат бария Ва(С1O3)2 - кристаллы ромбич. сингонии (пространств. группа Fdd2); т. пл. 400 °С (с разл.; плотн. 3,347 г/см3;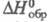 -738,0 кДж/моль; р-римость в воде при 25 °С 42,9 г в 100 г; моногидрат обезвоживается выше 135 °С. AgClO3 -кристаллы тетрагон. сингонии (пространств. группа I4/mmm), при 142 °С переходит в кубич. форму; т. пл. 231 °С; плотн. 4,439 г/см3;
-738,0 кДж/моль; р-римость в воде при 25 °С 42,9 г в 100 г; моногидрат обезвоживается выше 135 °С. AgClO3 -кристаллы тетрагон. сингонии (пространств. группа I4/mmm), при 142 °С переходит в кубич. форму; т. пл. 231 °С; плотн. 4,439 г/см3;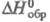 -25,5 кДж/моль; взрывает при нагревании, особенно после длит. хранения или пребывания на свету.
-25,5 кДж/моль; взрывает при нагревании, особенно после длит. хранения или пребывания на свету.
В пром-сти хлораты получают обменной р-цией NaClO3 с хлоридами металлов.
Расходуют хлораты в целлюлозно-бумажной пром-сти на получение С1O2 для отбеливания, на произ-во перхлоратов, в качестве гербицидов и дефолиантов хлопчатника и др. культур [Са(С1О3)2, Mg(ClO3)2], компонентов пиротехн. составов, окислителей в смесевых ВВ, КС1О3 - в произ-ве спичек, NaClO3 - в пиротехн. источниках кислорода.
При попадании в организм хлорат действует на кровь - переводят гемоглобин в метгемоглобин и вызывают распад эритроцитов. Токсичная доза для человека менее 1 г на 1 кг массы, 10 г могут вызывать смерть.
В. Я. Росоловский.
