§ 2. Хлор
По распространенности в природе хлор близок к фтору–на его долю приходится 0,02% от общего числа атомов земной коры. Человеческий организм содержит 0,25% хлора по весу.
Первичная форма нахождения хлора в природе отвечает его чрезвычайному распылению: небольшие количества этого элемента входят в состав самых различных минеральных пород земной коры. В результате работы воды, на протяжении многих миллионов лет разрушавшей горные породы и вымывавшей из них растворимые составные части, соединения хлора скоплялись в морях. Усыхание последних привело к образованию во многих местах земного шара мощных залежей NaCl, который и служит основным исходным сырьем для получения хлора.
Общее мировое потребление хлора (без СССР) составляет около 10 млн. т ежегодно. Используется он главным образом для беления тканей и бумажной массы, обеззараживания питьевой воды (примерно 1,5 г на 1 м3) и в химической промышленности.
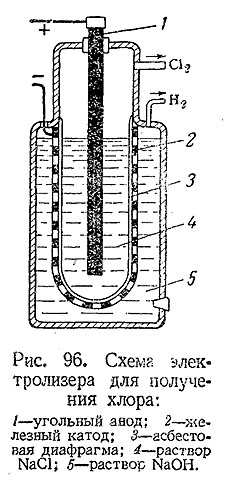
Основным промышленным методом получения хлора является электролиз концентрированного раствора NaCl (рис. 96). При этом на аноде выделяется хлор (2Сl’ – 2e– = Сl2 ), а в катодном пространстве выделяется водород (2Н· + 2e– = H2 ) и образует NaOH.
При лабораторном получении хлора обычно пользуются действием МnО2 или КМnО4 на соляную кислоту:
МnО2 + 4НСl = МnСl2 + Cl2 + 2Н2 О
2КМnО4 + 16НСl = 2КСl + 2МnСl2 + 5Сl2 + 8Н2 О
Вторая реакция протекает значительно энергичнее первой (требующей подогревания).
Свободный хлор представляет собой желто-зеленый газ (т. пл. -101 °С, т. кип. -34°С), состоящий из двухатомных молекул. Один объем воды растворяет около двух объемов хлора. Образующийся раствор часто называют «хлорной водой».
Хлор обладает резким запахом и вызывает воспаление дыхательных путей, В качестве средства первой помощи при острых отравлениях им применяется вдыхание паров смеси спирта с эфиром. Полезно также вдыхание паров нашатырного спирта.
По своей характерной химической функции хлор подобен фтору — он также является активным одновалентным металлоидом. Однако активность его меньше, чем у фтора. Поэтому последний способен вытеснять хлор из соединений.
Тем не менее химическая активность хлора очень велика - он непосредственно соединяется почти со всеми обычными металлами (иногда лишь в присутствии следов воды или при нагревании) и со всеми металлоидными элементами, кроме углерода, азота и кислорода. Важно отметить, что при отсутствии влаги хлор практически не действует на железо.
1) Взаимодействие хлора с фтором происходит лишь при нагревании их смеси выше 200 °С. В этих условиях образуется бесцветный ClF (т. пл. -154 °C,т. кип. -101 °С), а нагреванием его с избытком фтора может быть получен бесцветный ClF3 . Оба вещества характеризуются своей исключительно высокой реакционной способностью.
Взаимодействие хлора с водородом по реакции Н2 + Cl2 = 2HCl + 44 ккалпри обычных условиях протекает крайне медленно, но при нагревании смеси газов или ее сильном освещении (прямым солнечным светом, горящим магнием и т. д.) реакция сопровождается взрывом.
Детальное изучение этой реакции позволило выяснить характер протекания ее отдельных стадий (так называемых элементарных процессов). Прежде всего, за счет энергии ультрафиолетовых лучей (или нагревания) молекула хлора диссоциирует на атомы, которые затем реагируют с молекулами водорода, образуя НСl и атом водорода. Последний, в свою очередь, реагирует с молекулой хлора, образуя НСl и атом хлора, и т. д. Весь процесс может быть изображен следующей схемой:
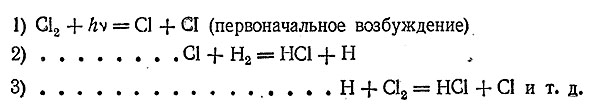
Таким образом получается как бы цепь последовательных реакций, причем за счет каждой первоначально возбужденной молекулы Сl2 образуется до миллиона молекул НСl. Реакции подобного типа называются цепными. Они играют большую роль при протекании многих химических процессов.
В настоящее время прямой синтез является основным промышленным методом получения НСl. Исходным сырьем служат хлор и водород, одновременно выделяющиеся при электролизе раствора NaCl. Спокойное протекание процесса обеспечивают смешиванием обоих газов лишь в момент взаимодействия.
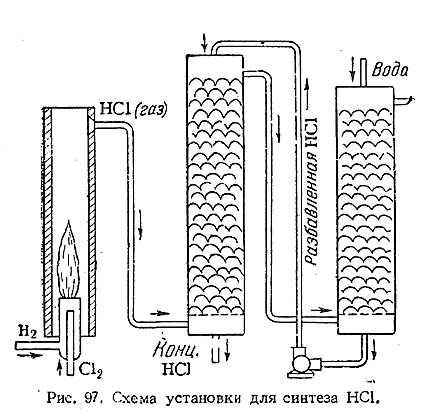
2) Для технического синтеза НСl служит установка, схематически показанная на рис. 97. После первоначального поджигания смесь хлора с водородом продолжает гореть спокойным пламенем, образуя хлористый водород. Последний проходит затем через две поглотительные башни, в которых и поглощается водой. Используемый в системе принцип противотока, т. е. противоположных направлений движения газа и жидкости, обеспечивает полноту поглощения НСl и позволяет проводить весь процесс непрерывно.
Другой метод технического получения НСl основан на взаимодействии NaCl и концентрированной H2 SO4 по реакциям:
NaCl + H2 SO4 = NaHSO4 + HCl
NaCl + NaHSO4 = Na2 SO4 + HCl
Первая из них отчасти протекает уже при обычных условиях и практически нацело – при слабом нагревании; вторая осуществляется лишь при более высоких температурах. Для проведения процесса служат механические печи большой производительности.
Хлористый водород представляет собой бесцветный газ (т. пл. –112°С, т. кип. –84 °С). В отсутствие влаги при обычных температурах он не действует на большинство металлов и их окислов. Газообразный кислород окисляет его только при нагревании.
На воздухе хлористый водород дымит вследствие образования с парами воды капелек тумана. Растворимость его весьма велика: при обычных условиях 1 объем воды способен поглотить до 450 объемов хлористого водорода.
Раствор НСl в воде называется хлористоводородной (иначе – соляной) кислотой. Последняя относится к числу наиболее сильных кислот. Концентрированная соляная кислота имеет плотность 1,19 и содержит около 37% хлористого водорода.
Подобно другим сильным кислотам, НСl энергично растворяет многие металлы. Большинство ее солей – хлористых, или хлоридов, – хорошо растворимо в воде. Из производных обычных металлов труднорастворимы лишь хлориды серебра и свинца.
Ежегодное мировое потребление соляной кислоты исчисляется миллионами тонн. Широкое практическое применение находят также многие ее соли.
Так как с кислородом хлор не взаимодействует, его кислородные соединения могут быть получены лишь косвенными методами. При рассмотрении путей их образования целесообразно исходить из обратимой реакции между хлором и водой
Сl2 + Н2 О = НСl + НОСl
При обычных условиях в насыщенном растворе гидролизовано около половины всего растворенного хлора.
Из образующихся при гидролизе хлора двух кислот – соляной и хлорноватистой (НОСl) –первая является очень сильной, а вторая – очень слабой (К = 3 ·10–8). Это резкое различие в силе обеих кислот можно использовать для их разделения.
Если в воде взболтать порошок мела (СаСОз) и затем пропускать в нее хлор, то соляная кислота реагирует с мелом (по уравнению СаСО3 + 2НСl = СаСl2 + СО2 + Н2 О), а хлорноватистая накапливается в растворе. Подвергая реакционную смесь перегонке, получают в приемнике разбавленный раствор НОСl.
Будучи соединением неустойчивым, НОСl медленно разлагается даже в таком разбавленном растворе. Соли хлорноватистой кислоты называются хлорноватистокислыми, или гипохлоритами. Сама НОСl и ее соли являются очень сильными окислителями.
Метод получения гипохлоритов основан на использовании приводившейся выше обратимой реакции взаимодействия хлора с водой. Так как оба вещества правой части равенства НСl и НОСl – дают в растворе ионы Н+, а оба исходных продукта – Сl2 и Н2 О – таких ионов практически не образуют, равновесие можно сместить вправо, связывая ионы Н+.
Добиться этого проще всего добавлением к реакционной смеси щелочи. Так как по мере образования ионы Н будут связываться ионами ОН' в недиссоциированные молекулы воды, равновесие сместится вправо. Применяя, например, NaOH имеем:
Сl2 + Н2 О <–––> НОСl + НСl
HOCl + НСl + 2NaOH –––>NaOCl + NaCl + 2H2 O
или в общем:
Сl2 + 2NaOH –––>NaOCl + NaCl + Н2 О
В результате взаимодействия хлора с раствором щелочи получается, следовательно, смесь солей хлорноватистой и соляной кислот. Образующийся раствор («жавелевая вода») обладает сильными окислительными свойствами и широко применяется для отбелки тканей и бумаги.
При взаимодействии хлора с более дешевой щелочью – Са(ОН)2 – образуется так называемая хлорная известь. Реакция может быть приближенно выражена уравнением
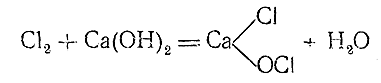
согласно которому хлорная известь является смешанной солью соляной и хлорноватистой кислот.
Хлорная (иначе, белильная) известь представляет собой белый порошок, обладающий сильными окислительными свойствами. Она применяется для беления и дезинфекции, а также служит одним из основных дегазаторов, т. е. средств для уничтожения боевых отравляющих веществ.
3) На воздухе хлорная известь постепенно разлагается, в основном, по уравнению: 2СаСl(ОСl) + СО2 = СаС2 + СаСОз + Сl2 О. При действии на нее соляной кислоты выделяется хлор: Ca(Cl)OCl + 2HCl = CaCl2 + H2 O + Cl2 . Хорошим продажным сортам хлорной извести приближенно соответствует состав ЗСа(Сl)ОСl ×Са(ОН)2 × xH2 O и содержание «активного» (т. е. выделяемого под действием соляной кислоты) хлора около 35% по весу.
Свободная хлорноватистая кислота испытывает в растворе три различных типа превращений, которые осуществляются независимо друг от друга и поэтому называются параллельными реакциями:
1) НОСl = НСl + О
2) 2НОСl = Н2 О + Сl2 О
3) 3HOCl = 2НСl + НСlО3
Все эти процессы способны протекать одновременно, но их относительные скорости сильно зависят от имеющихся условий. Изменяя последние, можно добиться того, что превращение пойдет практически нацело по какому–нибудь одному направлению.
Под действием прямого солнечного света разложение хлорноватистой кислоты идет по первому из них. Так же протекает оно в присутствии веществ, способных легко присоединять кислород, и некоторых катализаторов (например» солей кобальта).
При распаде по второму типу получается окись хлора (Сl2 О). Эта реакция идет в присутствии водоотнимающих веществ (например, СаСl2 ). Окись хлора представляет собой взрывчатый буровато–желтый газ (т. пл. –121 °С, т. кип. +2°С) с запахом, похожим на запах хлора. При действии Сl2 О на воду образуется НОСl, т. е. окись хлора является ангидридом хлорноватистой кислоты.
Распад НОСl по третьему типу особенно легко идет при нагревании. Поэтому действие хлора на горячий раствор щелочи выражается суммарным уравнением:
ЗСl2 + 6КОН = KClO3 + 5КСl + 3Н2О
Продуктами реакции являются КСl и калийная соль хлорноватой кислоты (НСlOз). Так как соль эта труднорастворима в холодной воде, при охлаждении раствора она осаждается.
Свободная НСlOз известна только в растворе. Она является сильной кислотой (диссоциированной приблизительно так же, как НСl и HNO3 ) и энергичным окислителем. Соответствующий ей ангидрид неизвестен.
В противоположность свободной НСlOз для ее солей (хлор–новатокислых, или хлоратов) окислительные свойства в растворах не характерны. Большинство хлоратов бесцветно (как и сама НСlO3 ) и хорошо растворимо в воде. Все ели сильно ядовиты.
4) При нагревании до 60 °С увлажненной смеси КСlО3 и щавелевой кислоты (Н2 С2 О4 ) по реакции
2КСlO3 + Н2 С2 O4 = K2 CO3 + CO2 + H2 O + 2ClO2
образуется зеленовато–желтая двуокись хлора (г. пл. – 59 °С, т. кип. + 10 °С). Свободная ClO2 малоустойчива и способна разлагаться со взрывом. В воде она хорошо растворима.
5) Взаимодействие СlО2 с раствором щелочи сопровождается образованием солей двух кислот – хлорноватой и хлористой: 2СlO2 + 2КOН = КСlOз + КСlO2 + Н2 О. Отдельно от хлорноватой можно получить хлористую кислоту по следующим реакциям: BaO2 +2ClO2 = Ba(ClO2 )2 +O2 и Ba(ClO2 )2 + H2 SO4 = BaSO4 2НСlO2 .
Малоустойчивая хлористая кислота (К = 5·10–3) известна только в разбавленных растворах, при хранении которых быстро разлагается. Соли ее (хлориты), как правило, бесцветны и хорошо растворимы в воде. В отличие от гипохлоритов, они характеризуются наличием сильно выраженных окислительных свойств только в кислой среде. Содержащие NaClO2 препараты находят применение в текстильной промышленности (для беления тканей).
При нагревании КСlOз около 400 °С начинает разлагаться, причем распад может идти по двум направлениям:
4КСlО3 = 4КСl + 6О2
или
4КСlО3 = ЗКСlО4 + КСl
Реакция протекает преимущественно по первому типу при наличии катализатора (МnО2 и т. п.), по второму – в его отсутствие. Образующийся при распаде по второму типу хлорнокислый калий (или перхлорат калия) очень мало растворим в воде и поэтому легко отделяется от хлористого калия.
В технике КСlО4 получают обычно электролизом раствора КСlO3 [по схеме: Н2 О + КСlО3 = Н2 (катод)+КСlО4 (анод)]. Его термический распад по уравнению КСlО4 = КСl + 2О2 начинается лишь выше 600 °С.
Действием на перхлорат калия концентрированной серной кислоты может быть получена свободная хлорная кислота (НСlO4 ), представляющая собой бесцветную, дымящую на воздухе жидкость. Так как НСlO4 летуча и под уменьшенным давлением перегоняется без разложения, ее легко выделить из реакционной смеси:
КСlО4 + H2 SO4 = KHSO4 + НСlO4
Безводная НСlО4 (т. пл. –112°С, т. кип. +39°С при 56 мм. рт. ст.) малоустойчива и иногда взрывается даже просто при хранении. В продажу обычно поступает вполне устойчивая 72%–ная килота. Как окислитель НСlO4 гораздо менее активна, чем НСlО3 , и в разбавленных растворах практически не обнаруживает окислительных свойств. Напротив, кислотные свойства выражены у нее исключительно резко: она является самой сильной из всех известных кислот.
Соли HClO4 , как правило, легкорастворимы в воде. Подобно самой кислоте, большинство перхлоратов бесцветно.
При слабом нагревании под уменьшенным давлением смеси безводной хлорной кислоты с фосфорным ангидридом (Р2 О5 ) перегоняется бесцветная маслянистая жидкость, которая представляет собой хлорный ангидрид, образующийся по реакции:
2НСlО4 + Р2 О5 = 2НРО3 + Сl2 О7
Строение молекулы хлорного ангидрида (т. пл. –91 °С, т. кип. +82°С) отвечает формуле О3 Сl–О–СlО3 . От сильного нагревания (и удара) Сl2 О7 взрывается. При взаимодействии его с водой медленно образуется хлорная кислота.
Хотя выше уже приводились названия кислородных кислот хлора и их солей, однако полезно сопоставить эти названия, включив в рассмотрение также малоустойчивую кислоту НСlO2 .
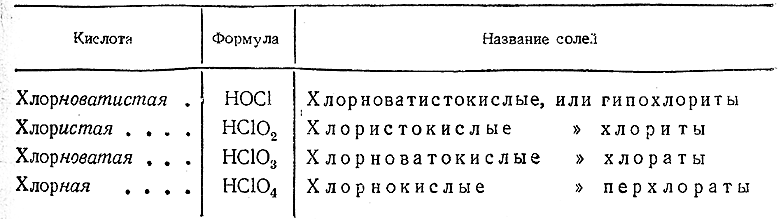
Структурные формулы всех четырех кислот приводятся ниже:
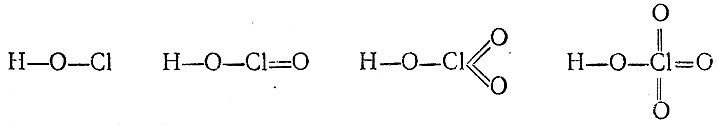
Как видно из этих формул, валентность хлора в рассматриваемых кислотах меняется по ряду: +1, +3, +5, +7.
Если сопоставить друг с другом кислородные кислоты хлора по важнейшим для них химическим свойствам – кислотности и окислительной активности, – то получается следующая схема:
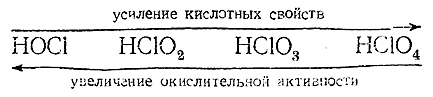
Кислотность изменяется, следовательно, противоположно окислительной активности. Последняя, в общем, тем больше, чем кислота менее устойчива. Действительно, хлорноватистая и хлористая кислоты более или менее устойчивы только в разбавленных растворах,
концентрацию хлорноватой можно довести уже до 40%, тогда как хлорная известна в безводном состоянии. Первые три кислоты в растворах постепенно разлагаются, а хлорная может сохраняться сколь угодно долго. Соответствующие соли обычно значительно устойчивее свободных кислот, но относительная их устойчивость примерно такова же, как и последних.


