Ненасыщенные спирты и простые эфиры
В ненасыщенных спиртах гидроксильная группа может находиться или у атома углерода, связанного двойной связью, или у связанного лишь простыми связями. Примером спиртов первого типа может служить так называемый виниловый спирт СН2=СН—ОН, примером вторых — аллиловый спирт СН2=СН—СН2ОН. Однако ненасыщенные спирты первого типа существуют лишь в исключительных случаях. Обычно же при реакциях, когда такие спирты, казалось бы, могут образоваться, вместо них получаются изомерные им предельные альдегиды и кетоны. Например, при нагревании с водой бромистого винила СН2=СНВr или хлористого изопропенила СН3—ССl=СН2 вместо соответствующих спиртов получаются уксусный альдегид и ацетон:
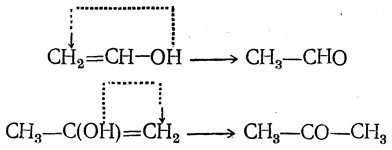
Неустойчивость группировки, в которой и двойная связь и гидроксил содержатся при одном и том же атоме углерода (правило А. П. Эльтекова), становится легко понятной, если рассмотреть этот вопрос с энергетической точки зрения. Например, сравнив виниловый спирт СН2=СН—ОН с уксусным альдегидом СН3—СН=О, мы увидим, что в основном различие этих соединений сводится к различию между группировками:

При переходе от первой ко второй разрывается связь О—Н и одна π-связь С—С; взамен этого образуется новая связь С—Н и вторая связь между С и О. Расчет показывает (ср. стр. 538), что при этом затрачивается 104,7 + 61,2=165,9 ккал/моль и выделяется 98,7 + 89,1 = 187,8 ккал/моль. Таким образом, превращение такого алкоголя (енола) в карбонильное соединение (альдегид или кетон) связано с выигрышем энергии 187,8—165,9=21,9 ккал/моль.
Долгое время считалось, что ненасыщенные спирты с гидроксилом при двойной связи вовсе не могут существовать в свободном виде вследствие того, что скорость их превращения в альдегиды и кетоны практически бесконечно велика Однако Гриньяр показал (1931), что в отсутствие катализаторов — минеральных кислот и щелочей — скорость превращения сравнительно невелика. Омыляя кипящей водой уксусные эфиры таких спиртов, синтезированные действием уксусного ангидрида или хлористого ацетила на смешанные магниевые алкоголяты, он получил сами спирты:
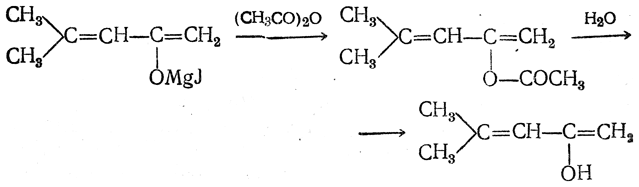
В присутствии даже следов минеральных кислот или щелочей скорость превращения таких непредельных спиртов в альдегиды и кетоны оказывается действительно очень большой, и для простейших спиртов этого типа достигается полное превращение.
Наоборот, эфиры ненасыщенных спиртов этого типа являются веществами устойчивыми. Простые эфиры могут быть получены различными способами, например отнятием молекулы спирта от ацеталей путем нагревания их с фосфорным ангидридом. Так, из диэтилацеталя ацетальдегида получается винилэтиловый эфир (жидкость с т. кип. 35,5° С):
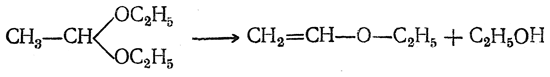
Простые виниловые эфиры могут получаться также действием ацетилена на спирты в присутствии кислых катализаторов:
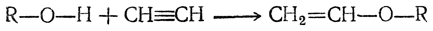
Однако в присутствии избытка спирта реакция обычно идет дальше и вместо эфиров образуются ацетали:
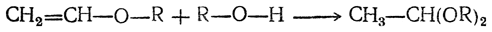
Еще легче простые виниловые эфиры получаются из ацетилена и спиртов в присутствии твердого едкого кали под небольшим давлением (А. Е. Фаворский, М. Ф. Шостаковский). Этот способ настолько прост, что он дал возможность получить большое число эфиров СН2=СН—OR, где R — различные радикалы алифатического и ароматического рядов.
Простые виниловые эфиры легко омыляются.
Дивиниловый тиоэфир, или сернистый дивинил, СН2=СН—S—СН=СН2 встречается в природе как составная часть эфирного масла одного из видов лука Аllium ursinum. При действии окиси серебра он обменивает серу на кислород и дает дивиниловый эфир СН2=СН—О—СН=СН2. Последний получен также действием едких щелочей на β,β'-дихлордиэтиловый эфир (СН2Сl—СН2)2О. Дивиниловый эфир представляет собой жидкость ст. кип. 28,3° С и относительной плотностью d420=0,773.
Уксусновиниловый эфир, или винилацетат, получается путем присоединения уксусной кислоты к ацетилену под влиянием катализаторов, например солей ртути:
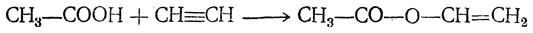
Он представляет собой жидкость (т. кип. 73° С), обладающую слезоточивым действием, легко полимеризующуюся в поливинилацетат. Омылением ацетильных групп получается поливиниловый спирт — белое аморфное вещество, нерастворимое в органических растворителях.

При достаточной полноте омыления поливиниловый спирт водорастворим, но путем специальной обработки ему может быть придана частичная или даже полная нерастворимость в воде. Поливинилацетаты применяются в технике (лаки, клеи, эмульгаторы и др.). Водорастворимый поливиниловый спирт в виде волокна применяется в медицине (нитки для хирургических швов, саморассасывающиеся после заживления раны), в водонерастворимой форме он используется для изготовления высокопрочного волокна (винол, куралон и др.).
Сложные эфиры вторичных спиртов с гидроксилом при двойной связи, например уксусноизопропениловый эфир СН2=С(СН3)—О—СО—СН3, представляют собой довольно прочные соединения. В настоящее время имеется два хороших способа их получения: действие кетена на кетоны в присутствии минеральных кислот
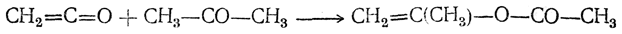
и действие уксусного ангидрида на кетоны в присутствии n-толуолсульфокислоты как катализатора:



