Пиримидин
ПИРИМИДИН, мол. м. 80,09; бесцв. ромбич. кристаллы со специфич. запахом, содержат в элементарной ячейке 4 молекулы; кольцо пиримидина практически плоское; т. пл. 22.5 0C, т. кип. 123-1240C; 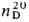 1,4998; m 6,33· 10-30 Кл·м; слабое основание, рКа 1,3. Легко раств. в воде, этаноле, диэтиловом эфире. Производные: сульфат, т. пл. 950C; нитрат, т. пл. 1350C; пикрат, т. пл. 1560C; перхлорат, т. пл. 1920C.
1,4998; m 6,33· 10-30 Кл·м; слабое основание, рКа 1,3. Легко раств. в воде, этаноле, диэтиловом эфире. Производные: сульфат, т. пл. 950C; нитрат, т. пл. 1350C; пикрат, т. пл. 1560C; перхлорат, т. пл. 1920C.
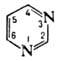
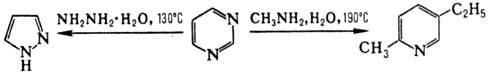
Пиримидин устойчив в холодных р-рах щелочей, медленно разлагается в кипящем 1 н. р-ре NaOH. Нуклеоф. атака пиримидина происходит в электронодефицитные четные положения, электрофильная-по атомам N или атому С-5. Нуклеоф. р-ции часто происходят с раскрытием цикла и сопровождаются послед. рециклизацией, напр. при действии гидразина или метиламина:
С магний- и литийорг. соединениями пиримидин образует в мягких условиях 4-алкил(арил)-3,4-дигидропроизводные. Пиримидин не вступает в р-ции нитрования, сульфирования; в виде соли броми-руется в положение 5. При активации кольца одним или неск. электронодонорными заместителями (амино-, гидроксигруппа и др.) возможны р-ции нитрования, нитро-зирования, сульфирования, азосочетания, формилирования и др. в положение 5. Под действием алкилгалогенидов, борфторида триэтилоксония и др. электроф. агентов пиримидин превращ. в моно- или бисчетвертичные соли; легкость ква-тернизации существенно зависит от характера заместителей в кольце. Под действием арильных радикалов, генерированных из солей n-нитрофенилдиазония, пиримидин вступает в р-ции гомолитич. замещения с образованием 2- и 4-арил-замещенных.
Окисление пиримидина H2O2 и надкислотами приводит к N-оксиду, каталитич. гидрирование (на Pd или Pt)- к тетрагидро-производным.
Пиримидин и его производные обычно получают конденсацией b-карбонильных соед. (или их эквивалентов, напр. ацеталей, енаминов и др.) с формамидом, ами-динами, мочевиной, тиомочевиной или гуанидином, напр.:
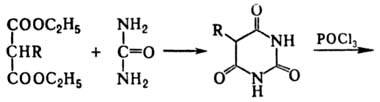
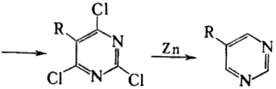
Сам пиримидин синтезируют обычно конденсацией 3-аминоакролеина с мочевиной или каталитич. восстановлением 2-хлор, 2,4-ди-хлор- или 2,4,6-трихлорпроизводных пиримидина в присут. оснований. Ядро пиримидина входит в состав нуклеиновых к-т, витаминов (напр., B1), антибиотиков (амицетин, блеомицин), лек. препаратов (барбитураты, пиримидиновые сульфамиды, фторафур, оротовая к-та), сильных ядов (тетродотоксин), коэнзимов (уридинфосфатглюкоза) и др.
Лит.: Пожарский А. Ф., Теоретические основы химии гетероцик-лов, M., 1985; Общая органическая химия, пер. с англ., т. 8, M., 1985, с. 121-27; Brown D. J., The pyrimidines, N. Y., L, 1962; suppl. 1-2, N.Y.-L., 1970-85; Comprehensive heterocyclic chemistry, v. 3, Oxf., 1984, p. 57. О. А. Загуляева.
