7.2.4. Выбор эмульгатора и характеристика эмульгирующих свойств ПАВ
Если взять примерно одинаковое количество воды и углеводорода, например, бензола, и путем взбалтывания приготовить эмульсию, то получим одновременно как эмульсию прямого типа – м/в, так и эмульсию обратного типа – в/м. Однако обе эти эмульсии будут неустойчивы и разрушаются практически мгновенно. Если в систему ввести соль жирной кислоты щелочного металла, растворимую в воде, то получим эмульсию прямого типа. Если взять соль жирной кислоты щелочноземельного металла, лучше растворимую в углеводородной фазе, то получим обратную эмульсию. Таким образом, первым условием для выбора эмульгатора или стабилизатора является их лучшая растворимость в той жидкости, которую предполагается сделать внешней фазой.
Вторым условием, определяющим выбор стабилизатора, следует рассматривать хорошую адсорбционную способность на границе раздела двух выбранных жидкостей. Стабилизатор должен стремиться на поверхность раздела и располагаться преимущественно между фазами, а не в объеме любой из них. Следовательно, стабилизатор должен иметь дифильное строение, т.е. содержать группы, обладающие сродством к обеим фазам. В результате адсорбции стабилизатор должен снижать разность полярностей фаз и уменьшать свободную энергию системы.
Однако высокая адсорбционная способность еще не обеспечивает устойчивости эмульсий. Например, использование солей щелочных металлов низших жирных кислот не позволяет получить устойчивых эмульсий, хотя эти вещества обладают высокой поверхностной активностью и, кроме того, создают двойной слой на поверхности раздела фаз. Очевидно, для получения устойчивых эмульсий недостаточно снижения свободной энергии системы или образования двойного ионного слоя. Только соли высших жирных кислот, соли сульфокислот или неионогенные ПАВ, обладающие развитым углеводородным радикалом, способны придавать устойчивость эмульсиям. Это позволило предположить, что молекулы стабилизатора должны иметь такую длину, что образовавшийся со стороны внешней фазы адсорбционный слоя не допустит сближения капель на расстояния, где начинается преобладание ван-дер-ваальсова притяжения. Это является третьим условием для выбора стабилизатора.
Как мы видели выше, в процессе эмульгирования устойчивые эмульсии образуются только в том случае, если эмульгатор способен достаточно быстро заполнять адсорбционный слой и в дальнейшем залечивать дефекты адсорбционного слоя при его нарушении. Это приводит к тому, что высокомолекулярные мыла подчас оказываются худшими стабилизаторами, чем гомологи с меньшим числом метиленовых групп в углеводородном радикале. Следовательно, стабилизатор должен обладать определенной подвижностью в адсорбционных слоях.
И, наконец, стабилизатор должен иметь способность к образованию тиксотропной структуры в адсорбционном слое, т.е. адсорбционный слой должен быть гелеподобным, с определенным пределом прочности и способностью быстро восстанавливать структуру межфазовой пленки после ее разрушения. Ряд исследований показали, что в устойчивых эмульсиях адсорбционный слой стабилизатора имеет структуру жидкого кристалла.
Таким образом, хороший стабилизатор обладает полным комплексом свойств. Неспособность стабилизатора удовлетворить хотя бы одному из указанных требований приведет к образованию неустойчивой эмульсии.
Теория эмульгирования и устойчивости эмульсий еще не разработана и поэтому приходится опытным путем подбирать эмульгатор и стабилизатор для каждого конкретного случая. Известную пользу приносят эмпирические характеристики эмульгатора, например, гидрофильно-липофильный баланс (ГЛБ), показывающий баланс между действием полярной и неполярной частей молекул. Эта характеристика хотя и не имеет под собой строгой теоретической основы, позволяет заранее предсказать тип получаемой эмульсии, но не характеризует ее устойчивость, так как одному значению ГЛБ может соответствовать различное строение молекул ПАВ, особенно неионогенных. Согласно шкале Гриффина, все поверхностно-активные вещества можно разделить на группы по значению ГЛБ, табл. 2.3.
Таблица 2.3
Области применения в зависимости
от гидрофильно-липофильного баланса
Г Л Б | Область применения |
3 – 6 | Эмульгаторы эмульсий в/м |
7 – 8 | Смачиватели |
8 – 15 | Эмульгаторы эмульсий м/в |
12 – 15 | Моющие вещества |
15 – 18 | Солюбилизаторы |
Следует подчеркнуть, что ГЛБ ПАВ зависит от присутствия в растворе солей и неэлектролитов, а также от температуры. Поэтому стабилизирующее действие будет меняться под влиянием этих факторов.
Для неионогенных ПАВ ГЛБ можно рассчитать по формулам, предложенным Гриффином. Эти формулы связывают степень оксиэтилирования и ГЛБ. Для оксиэтилированных спиртов и алкилфенолов расчет проводится по формуле
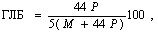 (2.7.4)
(2.7.4)
где 44 – молекулярная масса одной группы окиси этилена; Р – степень полимеризации (оксиэтилирования); М – молекулярная масса гидрофобного радикала. Уменьшение ГЛБ указывает на преобладание гидрофобной части молекул ПАВ.
Существует ряд методов определения ГЛБ, например, из диэлектрических измерений, газожидкостной хроматографии и т.д. Величина ГЛБ способна лишь указать на тип эмульсии, образуемой с данным эмульгатором, но не говорит о способности ПАВ стабилизировать эмульсию. Эмульгирующее действие ПАВ часто оценивается по максимальному объему фаз, диспергированному в заданном количестве раствора эмульгатора. Эта характеристика также недостаточно объективна, так как количество эмульгированной фазы часто зависит от условий и метода приготовления эмульсии.
Более объективной оценкой следует считать максимальную площадь межфазовой поверхности предельной высококонцентрированной эмульсии, полученной с заданным количеством эмульгатора (Аm). Еще одна характеристика, используемая для оценки эмульгирующей способности – минимальная концентрация эмульгатора, при которой данное ПАВ способно еще стабилизировать эмульсию.
Для объективной оценки эмульгирующей способности ПАВ следует сопоставлять:
- устойчивость (прочность) защитных слоев, для чего необходимо определять постоянную коалесценции;
- величину поверхности, которую способна стабилизировать единица объема раствора ПАВ;
- нижний предел концентрации эмульгатора, при которой еще происходит стабилизация.


