Иммуноглобулины
ИММУНОГЛОБУЛИНЫ (Ig), группа близких по хим. природе и св-вам глобулярных белков позвоночных животных и человека, к-рые обычно обладают св-вами антител, т.е. специфич. способностью соединяться с антигеном, к-рый стимулирует их образование. Иммуноглобулины продуцируются В-лимфоцитами и находятся либо в своб. виде в крови и нек-рых др. жидкостях организма, либо в виде рецепторов на поверхностных мембранах клеток. Семейство иммуноглобулинов у высших позвоночных включает в себя неск. классов; у человека их известно пять (G, М, A, D, Е). Классы иммуноглобулинов делятся на подклассы. Молекулы иммуноглобулинов симметричны. Они построены из "легких" (ок. 220 аминокислотных остатков) и "тяжелых" (450-600 аминокислотных остатков) полипептидных цепей (соотв. L- и Н-цепи), скрепленных дисульфидными связями и нековалентными взаимодействиями (см., напр., на рис. 1 схему строения IgG). В антителах человека обнаружено два вида легких цепей (( и l) и пять видов тяжелых цепей (g, m, a, d и e), отличающихся аминокислотной последовательностью. При обозначении иммуноглобулинов в ниж. индексах греческих букв цифры показывают, сколько цепей содержится в молекуле. Тяжелые цепи, характерные для каждого из классов и подклассов иммуноглобулинов, содержат по одному или более олигосахаридному фрагменту.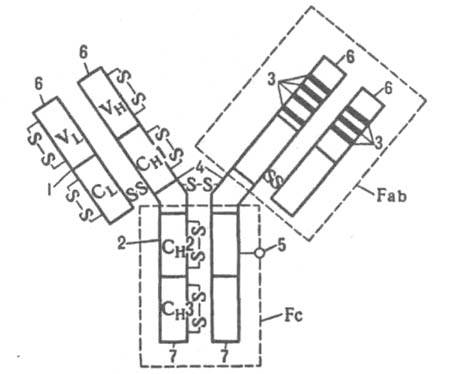
Рис. 1. Схема строения иммуноглобулина G: 1 - легкая цепь; 2 - тяжелая цепь; 3 - гипервариабельные участки; 4 - шарнирная область; 5 - остаток олигосахарида; 6 - N-концы; 7 - С-концы; VL и VH - соотв. вариабельные домены легкой и тяжелой цепей; CH1, CH2 и СH3 - постоянные домены тяжелой цепи; пунктиром обведены Fab- и Fc-фрагменты.
Легкие и тяжелые пептидные цепи каждого класса иммуноглобулинов построены из двух осн. областей - вариабельной (имеет антител из-за вставок и делеций (потери одного из внутр. участков в сегментах); в среднем она равна у легких цепей 108, а у тяжелых 120 аминокислотным остаткам. Осн. различия между вариабельными областями антител разной специфичности сосредоточены в определенных положениях полипептидной цепи - т. наз. гипервариабельных участках; их четыре в тяжелых и три в легких цепях. Эти участки (за нек-рыми исключениями) принимают участие в контакте с антигеном, что и определяет специфичность антител. Постоянные области цепей иммуноглобулинов кодируются одним геном (для каждого класса и подкласса). Молекулы иммуноглобулинов связанные с пов-стью лимфоцитов, имеют дополнит. гидрофобные "хвосты" на С-концах тяжелых цепей, к-рые встроены в мембраны клеток. Пептидные цепи иммуноглобулинов и ряда белков клеточных мембран (антигены гистосовместимости, рецепторы для антигенов Т-лимфоцитов) по своей первичной структуре сходны между собой, что указывает на общее эволюционное происхождение всех этих белков. Отрезки легких и тяжелых цепей иммуноглобулинов примерно в ПО аминокислотных остатков свернуты в относительно независимые компактные глобулы (домены), каждый из к-рых содержит один дисульфидный мостик; легкие цепи содержат два домена (вариабельный и постоянный), тяжелые - четыре или пять (в зависимости от класса иммуноглобулинов), один из к-рых вариабельный. По данным рентгеноструктурного анализа, осн. тип укладки цепи в доменах соответствует антипараллельной b-структуре (см. Белки). Посредине тяжелых цепей иммуноглобулинов имеется т. наз. шарнирная область с межцепьевыми дисульфидными связями (у IgG и IgA между первыми и вторыми доменами; на рис. 1 - между СН1 и СН2), длины к-рых неодинаковы у разных подклассов этих белков. Шарнирная область чувствительна к протеолитич. ферментам. При расщеплении ими (напр., папаином) иммуноглобулин распадается на два идентичных Fab-фрагмента и один Fc-фрагмент. Fab-Фрагмент слагается из четырех доменов. Два из них принадлежат легкой цепи, два других - N-концу тяжелой цепи. Fab-Фрагменты сохраняют способность к связыванию с антигеном. Fc-Фрагмент состоит из четырех или шести доменов двух тяжелых цепей и определяет такие св-ва иммуноглобулинов, как связывание им комплемента, возможность проникать через плаценту, присоединяться к клеткам и фиксироваться в коже. Благодаря высокой подвижности в шарнирной области, Fab- и Fc-фрагменты обладают определенной свободой вращения относительно друг друга. Такая гибкость позволяет молекулам иммуноглобулинов оптимально присоединяться к антигенам, имеющим разное пространств. строение. Область, контактирующая с антигеном (паратоп, или активный, антигенсвязывающий центр), располагается на N-конце Fab-фрагментов; она представляет собой более или менее глубокую полость, стенки к-рой сформированы аминокислотными остатками гипервариабельных участков легкой и тяжелой цепей. У антител, связывающих белки и полисахариды, в полость может входить до 6-7 остатков аминокислот или моносахаров. У молекул IgG, IgD, IgE и IgA (молекула IgA построена подобно молекуле IgG) 2 активных центра, у молекул IgM - 10. Комплекс с антигеном образуется в результате нековалентных взаимод., характер к-рых может варьировать в зависимости от специфичности антитела. Сила связывания с антигеном увеличивается на неск. порядков, если молекула антитела реагирует сразу двумя (или более) областями связывания с неск. детерминантами одной молекулы антигена. Каждая молекула IgG (осн. класса иммуноглобулинов у человека) состоит из двух идентичных легких и двух тяжелых цепей ((2g2 или l2g2). При расщеплении папаином молекула IgG распадается на три части - два идентичных Fab-фрагмента и один Fc-фрагмент. Антитела IgM [((2m2)5 или (l2m2)5] - эволюционно наиб. древние иммуноглобулины; они синтезируются на первых стадиях иммунной р-ции. Их молекулы состоят из пяти субъединиц (рис. 2), напоминающих молекулу IgG и соединенных друг с другом дисульфидными связями (такие иммуноглобулины наз. полимерными).
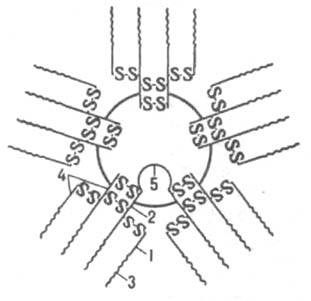
Рис. 2. Упрошенная схема строения иммуноглобулина М: 1 - легкая цепь; 2 - тяжелая цепь; 3 - вариабельная область; 4 - постоянные области легкой и тяжелой цепей; 5 - J-цепь.
Каждая молекула IgM имеет по одной J-цепи (мол. м. ок. 15000), к-рая присоединена дисульфидными связями к тяжелым цепям и участвует в образовании молекулы IgM из субъединиц. Для IgA [((2a2)n или (l2a2)n] характерна способность проникать в разл. секреты слюну, молозиво, слезы, кишечный сок. В состав IgA кроме J-цепи входит также еще одна пептидная цепь с мол. м. ок. 60000 (т. наз. секреторный компонент), к-рая образуется в эпителиальных клетках и присоединяется к молекуле IgA дисульфидными связями. Молекулы минорных классов иммуноглобулинов - IgD ((2d2 или l2d2) и IgE ((2e2 или l2e2) - по общей структуре сходны с молекулами IgG. Вместе с субъединицами IgM молекулы IgD чаще других иммуноглобулинов обнаруживаются на пов-сти В-лимфоцитов, где выполняют ф-ции антигенных рецепторов. Молекулы IgE, расположенные на пов-сти тучных и базофильных клеток, также являются рецепторами для антигенов. После присоединения к ним антигена (аллергена) происходит выбрасывание из этих клеток гистамина и серотонина, вызывающих аллергич. р-цию. На иммунизацию организм отвечает синтезом очень неоднородной популяции антител, молекулы к-рых могут сильно отличаться друг от друга по сродству к антигену. Такая неоднородность объясняется участием в иммунном ответе очень большой популяции В-лимфоцитов, каждый из к-рых синтезирует лишь одну разновидность молекул антител. С помощью техники гибридом (гибридные клетки, получаемые слиянием злокачественных и нормальных антителобразующих клеток лимфоцитов) удается получить в больших кол-вах однородные моноклональные антитела, к-рые широко используют в качестве высокоспецифич. реагентов для обнаружения, локализации и выделения разл. в-в, а также для диагностики и лечения нек-рых заболеваний. Гомог. иммуноглобулины накапливаются в больших кол-вах в крови и моче больных при ряде злокачеств. поражений лимфоцитов (т. наз. миеломные иммуноглобулины). Выделение чистых иммуноглобулинов проводится с помощью ионообменных смол с послед. гель-фильтрацией. Для мн. целей используют препараты миеломных иммуноглобулинов, особенно минорных классов. Антитела выделяют с помощью иммуносорбентов - фиксированных на нерастворимых носителях (напр., целлюлозе) антигенов. Обнаружение и количеств. определение иммуноглобулинов разных классов проводят иммунологич. методами с помощью соответствующих антисывороток. Для определения кол-ва антител используют методы преципитации (иммунная р-ция осаждения антигена антителом), агглютинации (взаимод. антитела с двумя клетками), нейтрализации бактерий и вирусов и др. Широкое распространение получают радиоиммунные и ферментно-иммунные методы, обладающие исключительно высокой чувствительностью и позволяющие определять очень малые кол-ва антител (или антигенов) в смесях с др. в-вами. Литература
