Четвертичная структура белка
Под четвертичной структурой подразумевают способ укладки в пространстве отдельных полипептидных цепей, обладающих одинаковой (или разной) первичной, вторичной или третичной структурой, и формирование единого в структурном и функциональном отношениях макромолекулярно-го образования. Многие функциональные белки состоят из нескольких полипептидных цепей, соединенных не главновалентными связями, а неко-валентными (аналогичными тем, которые обеспечивают стабильность третичной структуры). Каждая отдельно взятая полипептидная цепь, получившая название протомера, мономера или субъединицы, чаще всего не обладает биологической активностью. Эту способность белок приобретает при определенном способе пространственного объединения входящих в его состав протомеров, т.е. возникает новое качество, не свойственное мономерному белку. Образовавшуюся молекулу принято называть олигоме-ром (или мультимером). Олигомерные белки чаще построены из четного числа протомеров (от 2 до 4, реже от 6 до 8) с одинаковыми или разными молекулярными массами – от нескольких тысяч до сотен тысяч. В частности, молекула гемоглобина состоит из двух одинаковых α- и двух β-полипептидных цепей, т.е. представляет собой тетрамер. На рис. 1.23 представлена структура молекулы гемоглобина, а на рис. 1.24 хорошо видно, что молекула гемоглобина содержит четыре полипептидные цепи, каждая из которых окружает группу гема – пигмента, придающего крови ее характерный красный цвет (см. главу 2).
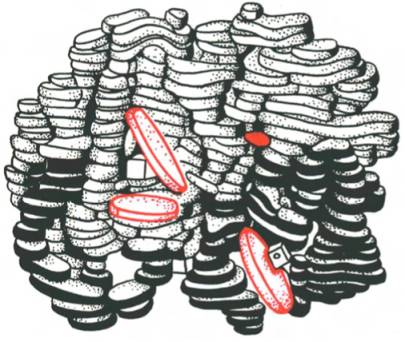
Рис. 1.23. Олигомерная молекула гемоглобина (красные диски – группы гема).
В определенных условиях (присутствие солей, 8М мочевины или резкие изменения рН) молекула гемоглобина обратимо диссоциирует на две α-и две β-цепи. Эта диссоциация обусловлена разрывом водородных связей. После удаления солей или мочевины происходит автоматическая ассоциация исходной молекулы гемоглобина (рис. 1.25).
Классическим примером олигомерной молекулы, или надмолекулярной структуры, является вирус табачной мозаики, представляющий собой гигантскую молекулу с мол. м. около 40•106. Он состоит из одной молекулы РНК (см. главу 3) и 2130 белковых субъединиц, масса каждой из которых составляет 17500. Длина вируса примерно 300 нм, ширина – около 17 нм. РНК вируса имеет спиралеобразную форму. Вокруг РНК нанизаны белковые частицы, образующие гигантскую надмолекулярную спиральную структуру, в которой насчитывается около 130 витков (рис. 1.26). Удивительной особенностью вируса является то, что после разъединения соответствующими приемами (добавление детергента) РНК и белковых субъединиц и последующего их смешивания (с предварительным удалением детергента) наблюдаются полная регенерация четвертичной структуры, восстановление всех физических параметров и биологических функций (инфектив-ная способность вируса). Подобная точность процесса спонтанной самосборки вируса обеспечивается, вероятнее всего, информацией, содержащейся в первичной структуре молекулы РНК и белковых субъединиц. Таким образом, последовательность аминокислот содержит в себе информацию, которая реализуется на всех уровнях структурной организации белков.
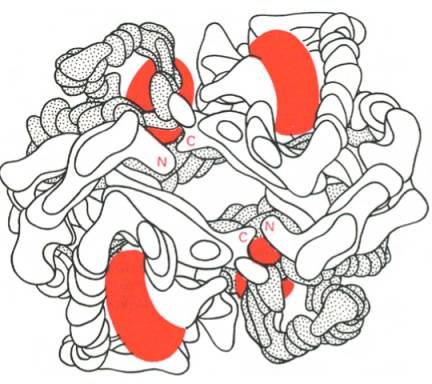
Рис. 1.24. Модель гемоглобина (по Перутцу).
α-Цепи светлые; β-цепи темные; группы гема красные.
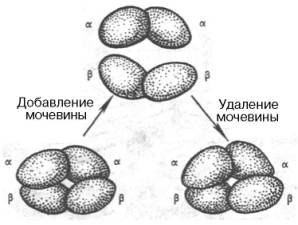
Рис. 1.25. Обратимая диссоциация молекулы гемоглобина.
Многие ферменты также обладают четвертичной структурой, например фосфорилаза а, состоящая из двух идентичных субъединиц, в каждой из которых по две пептидные цепи. Вся молекула фосфорилазы а, таким образом, представляет собой тетрамер. Отдельные субъединицы чаще всего не обладают каталитической активностью; вообще регуляторные ферменты (см. главу 4) имеют четвертичную олигомерную структуру. Они наделены функцией обеспечения в клетке требуемых скоростей химических реакций.
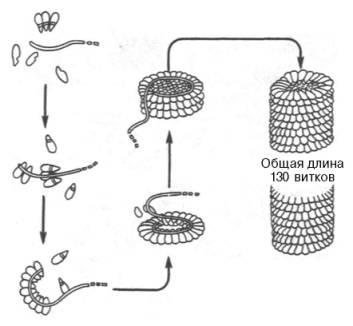
Рис. 1.26. Самосборка вируса табачной мозаики.
Наиболее изученным олигомерным ферментом является лактатдегидро-геназа (она катализирует обратимое превращение пировиноградной кислоты в молочную), содержащая два типа полипептидных цепей: Н – сердечный тип (от англ. heart – сердце) и М – мышечный тип (от англ. muscle – мышца) – и состоящая из 4 субъединиц. Этот фермент благодаря различным сочетаниям субъединиц может существовать в 5 формах. Такие ферменты получили название изоферментов, или, в соответствии с новой классификацией, множественных форм ферментов (см. главу 4).
К настоящему времени субъединичная структура обнаружена у нескольких сотен белков. Однако только для немногих белков, в том числе для молекулы гемоглобина, методом рентгеноструктурного анализа расшифрована четвертичная структура . Основными силами, стабилизирующими четвертичную структуру, являются нековалентные связи между контактными площадками протомеров, которые взаимодействуют друг с другом по типу комплементарности – универсальному принципу, свойственному живой природе. Структура белка после его синтеза в рибосоме может частично подвергаться модификации (посттрансляционный процессинг): например, при превращении предшественников ряда ферментов или гормонов (инсулин).
Таким образом, имеются все основания для подтверждения мнения о существовании 4 уровней структурной организации белков. Более того, каждый индивидуальный белок характеризуется уникальной структурой, обеспечивающей уникальность его функций. Поэтому выяснение структуры разнообразных белков может служить ключом к познанию природы живых систем и соответственно сущности жизни. На этом пути научного поиска могут быть решены также многие проблемы наследственных заболеваний человека, в основе которых лежат дефекты структуры и биосинтеза белков.
Некоторые исследователи склонны рассматривать, и не без основания, существование пятого уровня структурной организации белков. Речь идет о полифункциональных макромолекулярных комплексах, или ассоциатах из разных ферментов, получивших название метаболических олигомеров, или метаболонов, и катализирующих весь путь превращений субстрата (синте-тазы высших жирных кислот, пируватдегидрогеназный комплекс, дыхательная цепь).


