Пептидные антибиотики
ПЕПТИДНЫЕ АНТИБИОТИКИ, антимикробные соед , в молекулах к-рых имеются пептидные связи. В хим. отношении это весьма разнородная группа в-в, большинство из к-рых-циклич. или линейные олиго- и полипептиды, содержащие заместители непептидной природы (остатки жирных к-т, алифатич. аминов и спиртов, гидроксикислот, а также Сахаров и гетероциклов).
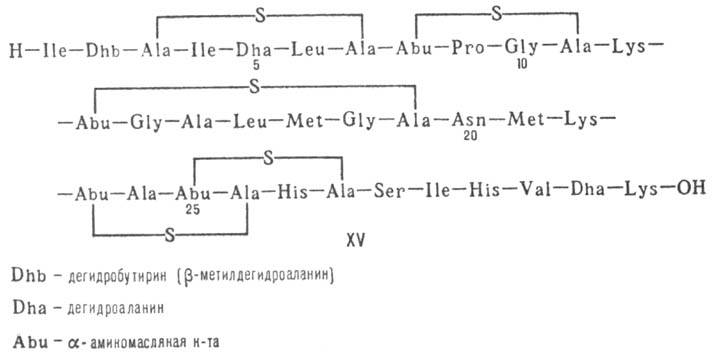
Различают пять осн. видов пептидных антибиотиков: 1) производные аминокислот (напр., циклосерин, b-лактамные антибиотики)и дикетопиперазина (глиотоксин, ф-ла I); 2) гомомерные пеп-тиды-линейные (грамицидин А, II) и циклические [бацит-рацин А, III (здесь и ниже буквы греч. алфавита показывают положение аминогрупп, к-рые участвуют в образовании связей); виомицин,, IV; капреомицин 1-А, V], а также олиго-пептиды (нетропсин, VI; дистамицин, VII); 3) гетеромерные пептиды [напр., полимиксины В, E и M, ф-лы соотв. VIII, IX и X; R = 6-метилоктаноил (B1, E1 и M1) или изооктаноил (B2, E2 и M2); Dab -2,4-диаминомасляная к-та], в т.ч. хелато-образующие (блеомицины); 4) пептолиды-хромопептолиды (актиномицины), липопептолиды (стендомицин, XI; здесь и ниже буквы Me перед лат. обозначениями аминокислот, кроме Pro, указывают на наличие в них метильной группы у атома N; МеРго 4-метилпролин), гетеропептолиды (мика-мицин В, XII; стафиломицин S, XIII), простые пептолиды (гризелимицин A, XIV) и депсипептиды (валиномицин; см. Ионофоры); 5) макромолекулярные пептиды полипептиды (низин, XV; сульфидные мостики связывают b-С-атомы Ala и Abu), белки (неокарциноста-тин, содержащий 109 аминокислотных остатков), протеиды (аспарагиназа, лизостафнин с мол. м. 32000).
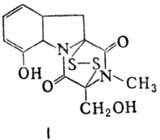
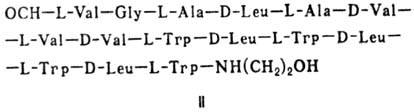
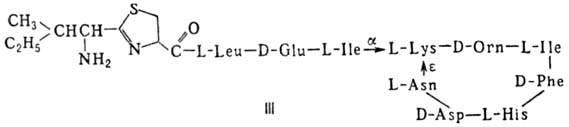
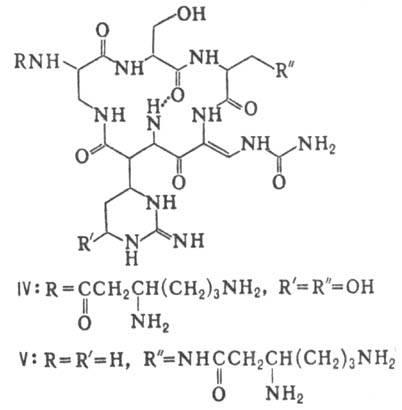
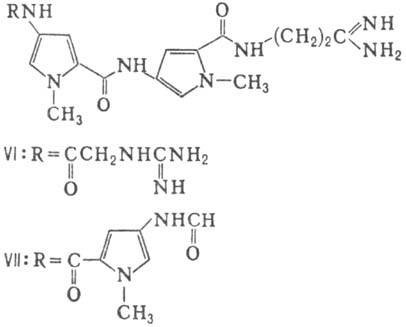
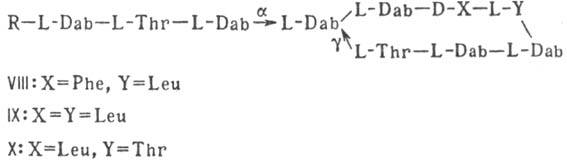
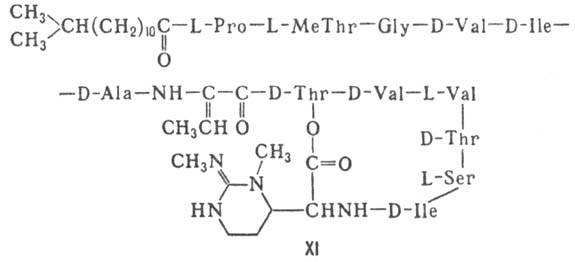
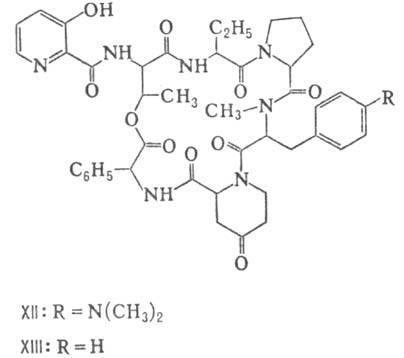
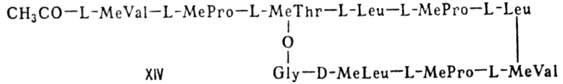
Гомо- и гетеромерные пептиды, пептолиды имеют ряд характерных особенностей, к-рые отличают их от обычных полипептидов и белков: а) низкое содержание нек-рых простых аминокислот (аргинин, гистидин, метионин), наличие аминокислот D-конфигурации и аминокислот необычной структуры (серосодержа-щих, сложных гетероциклич., ненасыщенных, N-метилированных, имино-, b- и g-аминокис-лот, производных пролина); б) наличие в составе молекул заместителей непептидной природы; в) преим. циклич. или линейно-циклич. структура без своб. карбокси- и аминогрупп; циклизация между собств. аминокислотными радикалами с образованием тиазолинов, окса-золинов и др. гетероциклич. структур. Кроме того, пептидные антибиотики, как правило, устойчивы к действию гидролаз, хотя нек-рые из них (полимиксины, блеомицины) чувствительны к аминоацилазам и пептидазам микробного и растит. происхождения.
Пептидные антибиотики продуцируются в виде смеси родственных соед., отличающихся друг от друга одним или неск. аминокислотными остатками или вариациями в строении компонентов непептидной природы. Продуцентами являются разл. виды актиномицетов, бактерий и грибов. Биосинтез пептидов и депсипептидов осуществляется без участия рибосом и РНК с помощью специфич. ферментных комплексов-синтетаз антибиотиков, содержащих всю необходимую информацию. Для ряда пептидных антибиотиков выяснен мол. механизм биосинтеза или установлен состав синтетаз. В процессе полимеризации или после образования пептидной цепи происходит циклизация молекулы и модификация отдельных аминокислот. Биосинтез макромолекулярных пептидных антибиотиков (в частности, низина) происходит на рибосомах с послед. модификацией белка-предшественника.
Пептидные антибиотики имеют разнообразные биол. св-ва. Среди.них встречаются ингибиторы синтеза клеточной стенки (бацитрацин А) и синтеза липопротеидов наружной мембраны грамотри-цат, бактерий (бицикломицин), ингибиторы репликации и транскрипции (актиномицин D, блеомицины) и синтеза белка (виомицин), ингибиторы функционирования клеточной мембраны (полимиксины, грамицидин, валиномицин), антиметаболиты (аланозин, циклосерин). Пептидные антибиотики обладают высокой антибиотич. активностью в отношении грамполо-жит. (бацитрацин А) и грамотрицат. (полимиксины) бактерий, а также микобактерий (капреомицин 1-А, виомицин). Ряд антибиотиков проявляют противоопухолевую (актино-мицины, аспарагиназа) и противогрибковую активность; дистамицин весьма активен в отношении вирусов.
Пептидные антибиотики широко применяют в ветеринарии (микамицин В, нетропсин), в качестве кормовых добавок (бацитрацин А, стафиломицины), как консерванты (низин), в биохим. исследованиях (валиномицин, грамицидины, актиномицины). Использование пептидных антибиотиков в терапии довольно ограниченно из-за нежелат. побочных эффектов, в частности нефроток-сичности. Широко применяют лишь полимиксины В, E и M, нек-рые противоопухолевые (блеомицин A2, актиномицин D, аспарагиназа) и противотуберкулезные препараты (циклосерин, виомицин, капреомицин 1-А, лизостафнин). Пептидные антибиотики, однако, вытесняются из мед. практики менее токсичными антибиотиками.
Лит. Ланчини Д.. Паренти Ф., Антибиотики, пер. с англ., M., 1985; Антибиотики-полипептиды (структура, функция, биосинтез), под ред. H. С. Егорова, M., 1987; Bioactive peptides produced by microorganisms, ed. by H. Umezawa, T. Takita, T. Shiba, Kodansha, Tokyo, 1978; Berdy J., CRC Handbook of antibiotic compounds, v. 4, pt 1 2, Boca Raton, 1980. А. А. Зинчепко.
