Кремния диоксид
КРЕМНИЯ ДИОКСИД (кремнезем) SiO2, бесцв. кристаллич., аморфное или стеклообразное в-во.Структура.Кремния диоксид существует в неск. полиморфных модификациях (см. табл.). Т-ры перехода при нормальном давлении: a-кварц D b-кварц 575 °С (DH0 перехода 0,41 кДж/моль), р-кварц D р-кристобалит 927 °С (2,26 кДж/моль), р-кварц D g-тридимит 867 °С (0,50 кДж/моль), a-тридимит D b-тридимит 115°С (0,27 кДж/моль), b-тридимит D g-тридимит 160°С (0,15 кДж/моль), g-тридимит D b-кристобалит 1470 °С (0,21 кДж/моль), a-кристобалит D b-кристобалит 270 °С. Т. пл. р-кварца 1610°С (DH0пл 8,53 кДж/моль), g-тридимита 1680 °С, b-кристобалита 1723°С (DH0пл 9,6 кДж/моль). Полиморфные превращ. кварца, тридимита и кристобалита сопровождаются изменением объема. Кристаллич. формы кремния диоксида построены из тетраэдров SiO4, a- и b-формы отличаются небольшим смещением и поворотом тетраэдров. Для низкотемпературных тридимитов приводятся данные и для др. кристаллич. модификаций, однако все они в качестве осн. структурной единицы содержат b-тридимит, но различно искаженный. Напр., описаны триклинный и моноклинный тридимиты. В природе встречается также кубич. модификация SiO2 - меланфлогит (a = 1,3402 нм, z = 48, пространств. группа Рт3п). При высоких давлениях образуются китит (80-130 МПа, 400-500 °C), коэсит (1,5-4 ГПа, 300-1700 °C), стишовит (16-18 ГПа, 1200-1400 °С). Стишовит - единственная модификация кремния диоксида, построенная из октаэдров SiO6. Устойчивость тридимита, вероятно, определяется примесями Na и Аl. Неустойчивая форма кремния диоксида - ромбо-дипирамидальный "волокнистый кремнезем". Кроме кристаллических для кремния диоксида характерны и др. формы существования. Скрытокристаллич. формы (халцедоны) по структуре аналогичны кварцу. При экстрагировании к-той катионов из нек-рых силикатов получают гидратир. кристаллич, кремнеземы. Они наследуют текстуру исходных минералов, образуя волокнистые, чешуйчатые (лепидоидальныe) и листоподобные слоистые структуры. Известны аморфные анизотропные и изотропные (опал) образования, тонкодисперсный прир. кремнезем (трепел, синтетич. коллоидный кремнезем и кремнеземные порошки). Гидратир. аморфный кремнезем, осаждаемый из р-ров силиката Na и др., полимеризован до сферич. частиц диаметром менее 100 нм, обычно 2-3 нм. Получен аморфный кремнезем в форме листочков, ленточек и волокон (см. Силикагель). При высоких т-рах из газовой фазы выделяются тонкодисперсные порошки пирогенного безводного кремнезема - аэросил и др. О стеклообразном кремнеземе см. Стекло кварцевое.
Свойства. Давление пара кремния диоксида 13,3-133 Па вблизи т-ры плавления. Кремния диоксид - диэлектрик, r 1012 Ом.м (20°С), 9.10-1 Oм.м (1600°C). Монокристаллы a-кварца обладают хиральной структурой, что обусловливает их оптич. активность и пьезоэлектрич. св-ва. Кварц прозрачен для УФ и частично ИК лучей.
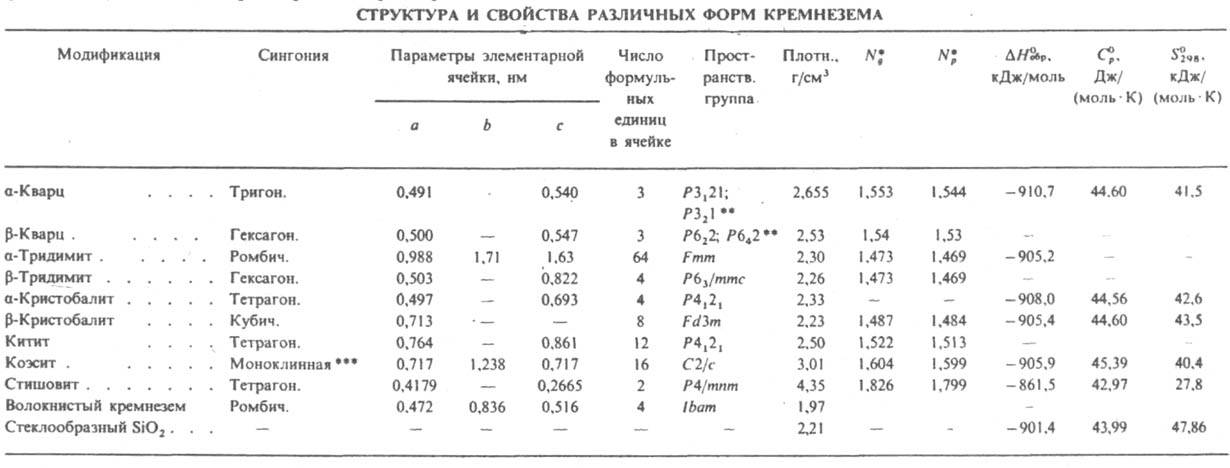
* Показатели преломления: Ng - больший, Np - меньший. ** У a- и b-кварца по две пространств. группы, т.к. для обеих форм возможны левый и правый оптич. изомеры. *** b-120°С.
Р-римость a-кварца в воде 10-3% по массе (25°C), аморфных форм кремнезема 0,007-0,015% (о водных р-рах SiO2 см. Кремниевые кислоты). Р-римость кремния диоксида в кислых и щелочных средах определяется природой р-рителя. Кремния диоксид не раств. в большинстве орг. р-рителей. Реагирует с фтористоводородной к-той, образуя кремнефтористоводородную кислоту. При 250-400 °С взаимод. с газообразным HF, F2 (давая SiF4), при 200-250°С - с NH4HF2. В смеси с углем реагирует с Сl2 при нагр., образуя SiCl4. Аморфный кремнезем медленно раств. в водных р-рах щелочей, Na2CO3 (давая силикаты) и NH4F (образуя фторосиликаты), скорость растворения увеличивается при повышении давления и т-ры. При нагр. смесей порошкообразного кремния диоксида с разл. оксидами образуются силикаты, при сплавлении с Na2CO3 и Na2SO4 - водорастворимый натрия силикат (см. также Стекло растворимое).
Распространение в природе. Содержание своб. кремния диоксида в земной коре 12%; он входит также в состав горных пород в виде разл. силикатов или в виде смесей с др. минералами (граниты). Кварц - один из наиб. распространенных минералов, намного реже встречаются тридимит, кристобалит, лсшательит (прир. кварцевое стекло), халцедоны, опалы. Мелкие, различно ориентированные кристаллы кварца образуют "жильный" кварц. При разрушении горных пород возникают кварцевые пески, уплотнение к-рых приводит к образованию песчаников и кварцитов. Hаиб. чистый кварц - горный хрусталь, кристаллы к-рого могут достигать неск. метров и весить десятки тонн. Монокристаллы кварца прозрачны, бесцветны (горный хрусталь) или окрашены примесями в фиолетовый (аметист), черный (марион), желтый (цитрин), дымчатый (раух-топаз) цвета. Разновидности скрытокристаллич. формы кварца: розово-красный сердолик, синеватый сапфирин, яблочно-зеленый хризопраз, полосчатые агаты и ониксы, тонко-окрашенная яшма, кремни и роговики. Уиикален аморфный "благородный" опал, состоящий из однородных коллоидных частиц диаметром 0,1-0,3 мкм, плотно упакованных в упорядоченные агломераты; содержание воды в нем менее 1% по массе (для большинства рядовых опалов 4-9%). Прир. месторождения кремнезема образуют также трепел, диатомит и др. Из кремнезема построены панцири диатомовых водорослей, скелеты нек-рых губок; он упрочняет стебли растений - хвощей, бамбука, тростника, содержится в соломе. Кремния диоксид ответствен за окремнение форм живых организмов растений. В крови и плазме человека концентрация кремнезема составляет 0,001% по массе.
Получение. Синтетич. кремния диоксид получают: действием к-т (H2SO4, HCl, СО2) на силикат Na, реже - на др. р-римые силикаты (осн. способ произ-ва в капиталистич. странах); из коллоидного кремнезема коагуляцией под действием ионов Na+, NH4, F- или замораживанием; гидролизом SiCl4, SiF4, (NH4)2SiF6, (C2H5O)4Si в водных, водно-аммиачных р-рах (иногда с добавлением этанола или орг. оснований) и в газовой фазе. Аморфный кремния диоксид получают также из трепела и диатомита, прокаливанием рисовой шелухи, размалыванием плавленого кварцевого песка. Безводные порошки кремния диоксида с высокой уд. пов-стью получают хим. осаждением из газовой фазы путем сжигания паров SiCl4 в смеси Н2 и О2 (аэросилы, в США - кабосил), окисления и гидролиза паров сложных эфиров Si (пирогенный кремнезем), а также SiF4 (флуосил). Первично конденсируемые частицы кремния диоксида диаметром 1 нм плотно упакованы во вторичных конгломератах, объединенных в рыхлую структуру с уд. пов-стью 200-400 м2/г. Монокристаллы a-кварца выращивают из щелочных р-ров кремния диоксида в автоклавах высокого давления (35-120 МПа) при 300-420 °С (см. Гидротермальные процессы). В произ-ве используемых в технике материалов на основе кремния диоксида применяют след. процессы:
- хим. осаждение из газовой фазы при высокотемпературном сжигании SiCl4, предварительно очищенного ректификацией. Частицы кремния диоксида, образующиеся в кислородно-водородном пламени или плазме, осаждаются давая массивные кварцевые стекла или слои заготовок волоконных световодов;
- окисление пов-сти монокристаллич. Si с образованием гетероструктур (в произ-ве интегральных схем);
- спекание мелкодисперсного кремния диоксида в кварцевую керамику (см. также Керамика);
- золь-гель процесс, включающий гидролиз орг. соед. Si, медленную дегидратацию образовавшегося геля и умеренное нагревание. Используется для получения кварцевых и высококремнеземистых стекол;
- получение особо чистого кремния диоксида и пористых стекол (типа "викор") путем термич. обработки лидирующего боросиликатного стекла, выщелачивания к-той и отмывки кремнеземистого каркаса.
Прир. кремнезем используют в произ-ве силикатных стекол, изделий из фарфора и фаянса, абразивов, бетона, силикатного кирпича, динаса, керамики. Синтетич. кремния диоксид ("белая сажа") - наполнитель в произ-ве резин (до 70% производимого кремния диоксида). Преим. используют осажденные гидратир. кремнеземы (содержащие 85-95% SiO2) с уд. пов-стью 60-300 м2/г, в меньшей степени - безводные кремнеземы типа аэросила. Аэросил - также адсорбент в хроматографии, загуститель смазочных материалов, клеев, красок. Монокристаллы кварца применяют в радиотехнике (пьезоэлектрич. стабилизаторы частоты, фильтры, резонаторы и др.), в акустооптике и акустоэлекронике (см. Акустические материалы), в оптич. приборостроении (призмы для спектрографов, монохроматоров, линзы для УФ оптики и др.), в ювелирном деле (прозрачные, красиво окрашенные разновидности - полудрагоценные камни). Силикагели с эффективным диаметром пор 2-15 нм используют как пром. сорбенты и носители катализаторов. Синтетич. кремния диоксид и горный хрусталь являются сырьем для произ-ва монокристаллов кварца, кварцевого стекла, керамики и кварцевых волокон. Кварцевое стекло и керамика - конструкц. материал в авиац. пром-сти (напр., для обтекателей окон и иллюминаторов летательных аппаратов), в оптике (для входных окон оптич. приборов УФ и И К диапазонов), в электронике (линии задержки) и др. Кварцевая ткань -теплозащитный материал. Кварцевые волокна используют для создания волоконно-оптич. (световодных) линий связи и систем передачи информации. Произ-во синтетич. кремния диоксида в капиталистич. странах 600-700 тыс. т/год (1980). При попадании кремния диоксида в живые ткани медленно развиваются гранулемы. Кремнеземная пыль вызывает раздражение верх. дыхат. путей и бронхов, заболевание желудочно-кишечного тракта, при длит. вдыхании - тяжелое заболевание - силикоз легких. ПДК при содержании SiO2 в пыли св. 70% - 1 мг/м3, 10-70% - 2 мг/м3, 2-10% - 4 мг/м3. Литература
