Фракции крахмала
Полисахариды крахмала можно разделить более или менее точно на две фракции — амилозу и амилопектин, отличающиеся строением входящих в их состав 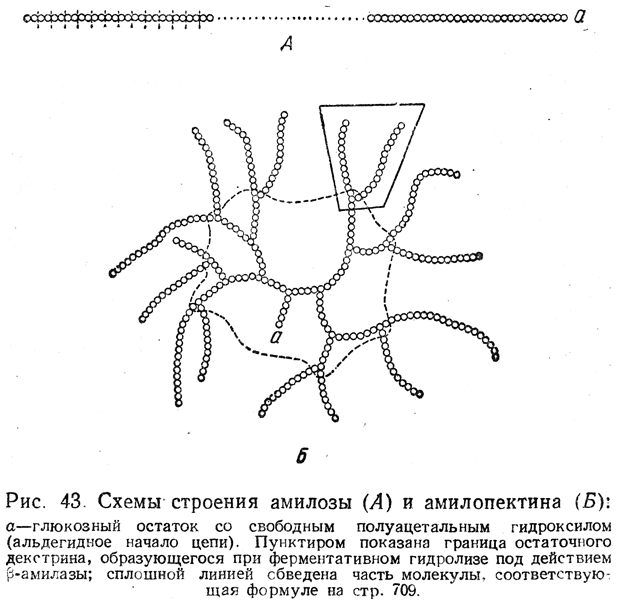
полисахаридов. Полисахариды амилозы имеют неразветвленную или очень мало разветвленную цепь глюкозных остатков (рис. 43, А); молекулы амилопектина представляют собой многократно разветвленные цепи глюкозных остатков (рис. 43, Б). Содержание фракций амилозы и амилопектина в крахмале, выделенном из различных растений, различно: обычно от 15 до 25% амилозы и от 75 до 85% амилопектина.
Ранее считали, что амилоза сосредоточена в центральных частях крахмальных зерен, тогда как амилопектин составляет их оболочку. В последние годы исследования методом меченых атомов показали, что это распределение различно для крахмалов разных растений.
Фракционирование крахмала связано с большими трудностями, так как трудно подобрать такие агенты, которые разъединяли бы комплекс амилозы и амилопектина, не затрагивая связей между остатками глюкозы. В настоящее время пользуются четырьмя группами методов фракционирования крахмала:
1. Извлечение амилозы горячей водой.
2. Избирательная адсорбция амилозы или амилопектина.
3. Избирательное осаждение амилозы, например некоторыми спиртами (бутиловыми, амиловыми), тимолом и т. д
4. Хроматографирование на бумаге и окиси алюминия.
Полученные фракции амилозы и амилопектина разделяют далее на ряд субфракций (субфракционирование), отличающихся, например в случае амилозы, средними молекулярными весами и длиной цепи.
Основным методом выяснения строения фракций крахмала был метод метилирования; наряду с этим ценные сведения получены при изучении ферментативного расщепления. Если метилирование моносахаридов и олигосахаридов протекает очень легко, то метилирование высших полиоз представляет весьма трудоемкую операцию. Так, исчерпывающее метилирование полисахаридов крахмала требует 24-кратной обработки диметилсульфатом. После предварительного ацетилирования требуется шести-восьмикратное метилирование (при метилировании ацетильные группы отщепляются).
Амилоза. При фракционировании крахмала методом избирательного осаждения удается получить кристаллическую амилозу, присутствие которой и обусловливает обнаруживаемую рентгеновским анализом кристалличность некоторых препаратов крахмала. Амилоза дает с иодом чисто синее окрашивание; она может быть полностью расщеплена ферментом β-амилазой до мальтозы (если препарат не содержит точек ветвления или β-гликозидных связей).
Содержание фосфора (который в виде остатков фосфорной кислоты связан в крахмале с некоторыми глюкозными остатками) в амилозе очень мало — до 0,03%. Растворы амилозы весьма нестойки; амилоза вскоре выпадает в виде нерастворимого осадка. Это явление носит название ретроградации.
При кислотном гидролизе триметиламилозы — продукта исчерпывающего метилирования амилозы — получается около 99% 2,3,6-триметилглюкопиранозы и примерно 0,4% 2,3,4,6-тетраметилглюкопиранозы. Кислотный гидролиз метилированной амилозы протекает по схеме, приведенной на стр. 707.
Образование в качестве продукта гидролиза почти исключительно 2,3,6-триметилгюкопиранозы со свободными гидроксилами у первого и четвертого атомов углерода свидетельствует о том, что глюкопиранозные остатки в молекуле амилозы связаны между собой гликозидными связями 1,4'. Эти связи являются α-гликозидными, что подтверждается, в частности, образованием мальтозы (дисахарида с α-гликозидной связью) при ферментативном и кислотном гидролизе амилозы. Содержание в продуктах гидролиза метилированной амилозы ничтожного количества 2,3,4,6-тетраметилглюкопиранозы при отсутствии диметилглюкопиранозы, которая должна была бы образоваться в местах ветвления цепи, указывает на то, что амилоза имеет длинную неразветвленную цепь. Молекулярный вес амилоз, определяемый различными методами, равен 160 000—1000 000 (и даже выше), что соответствует наличию в молекуле от 1000 до 6000 и более глюкозных остатков.
Приведенное на стр. 707 строение амилозы хорошо объясняет присущую ей весьма малую восстанавливающую способность.
Начиная с 1949—1950 гг. восстанавливающей способностью амилозы (а также амилопектина) стали пользоваться для определения ее молекулярного веса (химический метод). Каждая молекула амилозы содержит лишь один свободный полуацетальный гидроксил, который может переходить в способную окисляться альдегидную группу:
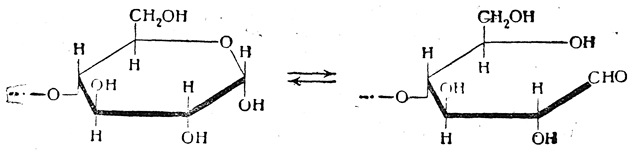
Если определить восстанавливающую способность полисахарида до гидролиза, а затем, гидролизовав его, определить количество образовавшейся глюкозы, то можно вычислить степень полимеризации, а отсюда и молекулярный вес. Для определения весьма малой восстанавливающей способности полисахарида его окисляют динитросалициловой кислотой, цвет которой при восстановлении в нитроаминосалициловую кислоту переходит из желтого в коричневый. Изменение цвета определяют фотометрически. Однако значения молекулярного веса, найденные химическим методом, всегда занижены по сравнению с найденными физико-химическими методами.
В последнее время было показано, что в некоторых фракциях амилозы содержатся не только линейно построенные, но и крайне слабо разветвленные полисахариды.
Амилопектин дает с иодом фиолетовое окрашивание; он расщепляется β-амилазой на 50—60%, причем наряду с мальтозой всегда образуются остаточные декстрины, называемые β-декстринами. Содержание фосфора в амилопектине значительно выше, чем в амилозе (0,20—0,22%). Амилопектин сильно набухает в воде. При приготовлении клейстера из природного крахмала амилопектин препятствует ретроградации амилозы.
Молекулярный вес амилопектина значительно выше, чем у амилоз. Недавно для одного амилопектина был найден молекулярный вес порядка 5 ∙ 108. Молекулы амилопектина имеют разветвленное строение.
При гидролизе триметиламилопектина наряду с 2,3,6-триметилглюколиранозой образуются приблизительно равные количества (примерно по 4%) 2,3-диметилглюкозы и 2,3,4,6-тетраметилглюкозы (Фрейденберг). Это свидетельствует
Схема кислотного гидролиза метилированной амилозы
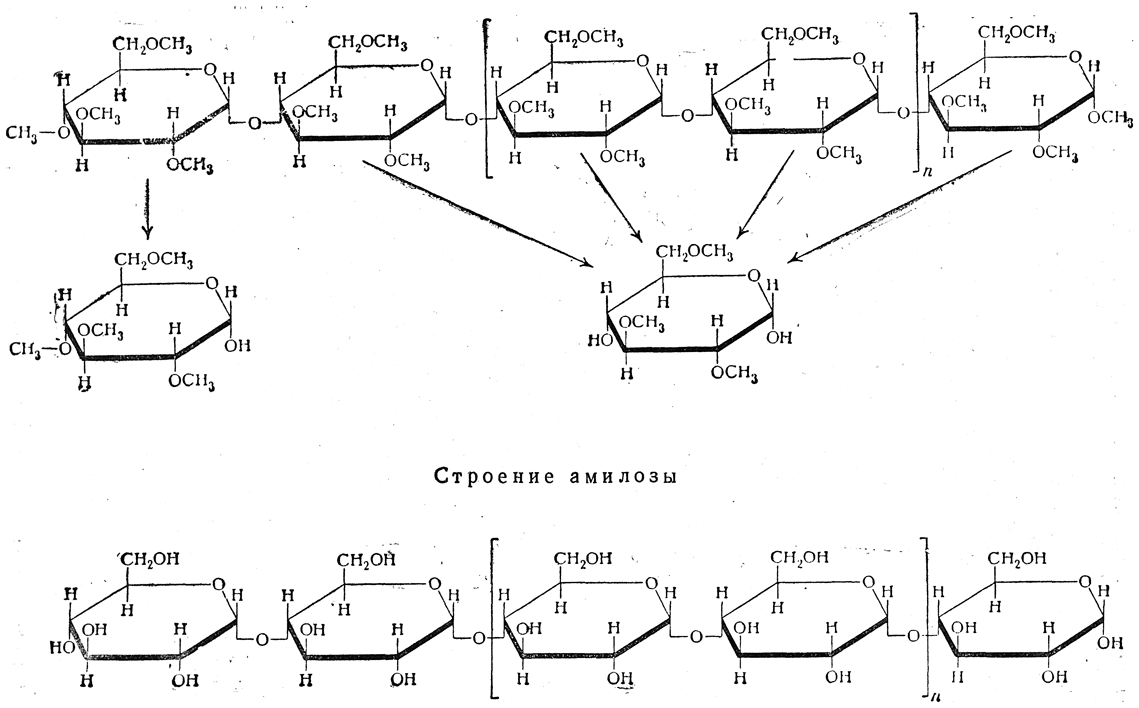
о сильном дихотомическом ветвлении цепей амилопектина, так как тетраметилглюкоза образуется из концевых глюкозных остатков, а диметилглюкоза — из глюкозных остатков, являющихся точками ветвления полисахаридной цепи. Образование 2,3,6-триметилглюкозы, 2,3-диметилглюкозы и 2,3,4,6-тетраметилглюкозы при гидролизе метилированного амилопектина, свидетельствующее о наличии в амилопектине 1,4'-связей, видно на схеме, приведенной на стр. 709.
Гликозидные связи в молекуле амилопектина являются α-гликозидными, о чем свидетельствует образование при ферментативном и кислотном гидролизе значительных количеств мальтозы (дисахарида с α-гликозидной связью).
Применение наряду с методом метилирования методов ферментативного расщепления существенно расширило представления о строении амилопектина. Путем исследования остаточных декстринов, получаемых при ферментативном расщеплении амилопектина β-амилазой, удалось доказать, что наружные цепи амилопектина (от концевых остатков до первых точек ветвления) длиннее участков между точками ветвления в центральных частях молекулы (К. Мейер).
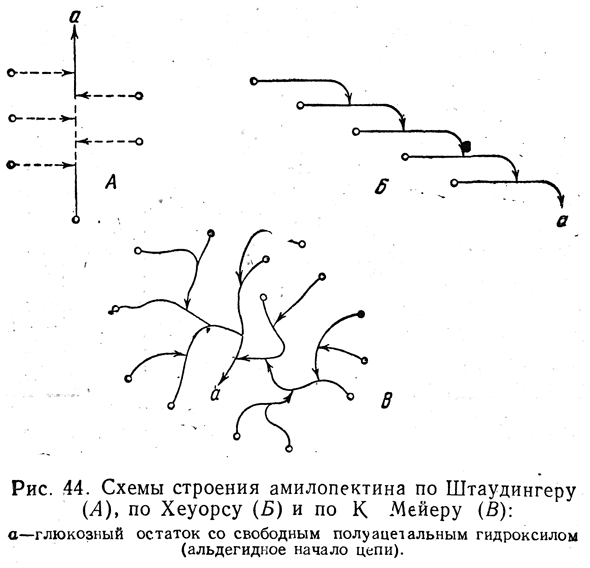
Приведенная на рис. 43, Б схема строения амилопектина далеко не сразу получила признание. Обсуждалась и схема Штаудингера, названная «гребешковой», согласно которой в основе молекулы амилопектина (и гликогена) лежит сравнительно короткая основная цепь, и к ней присоединен ряд боковых цепей (рис. 44, А) при помощи 1,6', 1,3' и 1,2'-связей.
Схема кислотного гидролиза метилированного амилопектина
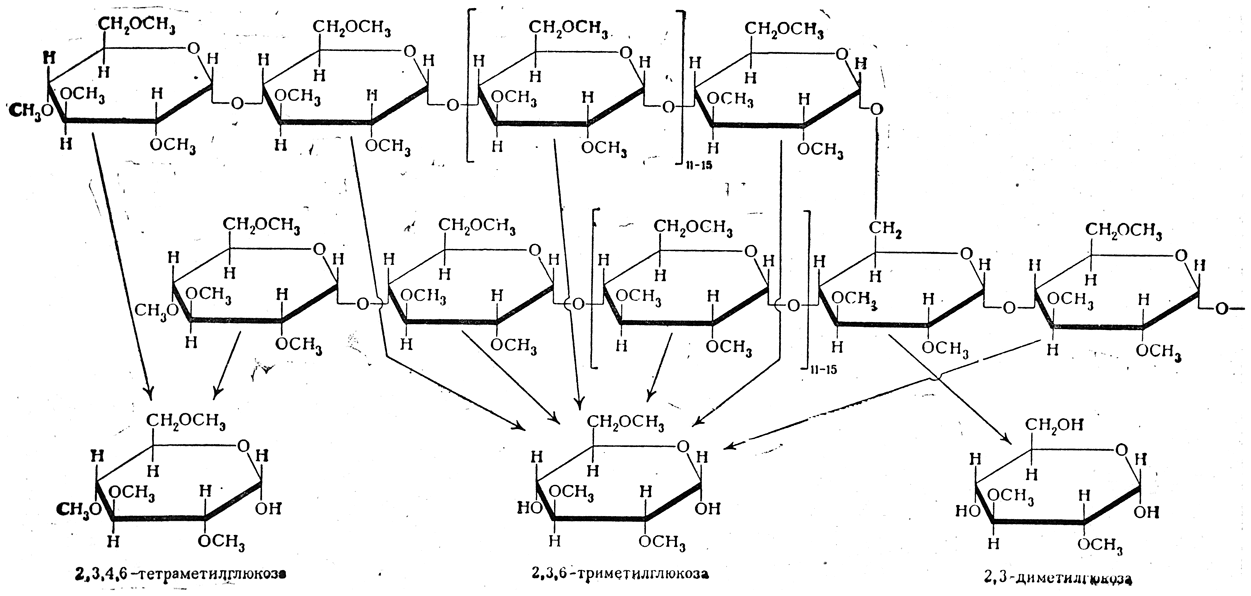
До недавнего времени обсуждалась также ламинарная схема Хеуорса (рис. 44, Б), согласно которой амилопектин не имеет стержневой части; цепи глюкозных остатков, соединенных α-1,4'-связями, присоединяются одна к другой таким образом, что «альдегидный» конец такой цепи присоединен при помощи 1,6'-связи к какому-то среднему глюкозному остатку следующей цепи. Наиболее обоснованной в настоящее время является схема К. Мейера (рис. 44, В).


