Натрия борогидрид
НАТРИЯ БОРОГИДРИД (тетрагидридоборат натрия) NaBH4, бесцв. кристаллы с кубич. гранецентрир. решеткой (а = 0,6164 нм, z = 4, пространств. группа Fm3m); ниже — 80 °С переходит в тетрагон. модификацию (а = 0,4354 нм, с = 0,5907 нм); т. пл. 505 °С (с разл.); плотн. 1,074 г/см3; С0р 2,3 кДжДкг•К); DH0обр - 190 кДж/моль, DG0298 — 119,5 кДж/моль; S0298 101,4 ДжДмоль • К). Хорошо раств. в полярных р-рителях, не раств. в диэтиловом эфире, диок-сане, углеводородах; р-римость (г в 100 г): в воде-40,6 (0°С), 56 (25 °С), в жидком NH3-99 (-22,5 °С), гидразине-25,4 (25 °С), ТГФ - менее 0,1, ДМСО - 5,8 (25 °С), ДМФА -18, этаноле-4,0 (20 °С, с медленным разложением). В водных р-рах натрия борогидрид постепенно гидролизуется, образуя Na3BO3 и Н2, в щелочных р-рах гидролиз замедляется, в кислых - значительно ускоряется; в присут. орг. к-т, солей переходных металлов скорость гидролиза резко увеличивается. Из воды ниже 36,3 °С натрия борогидрид кристаллизуется в виде дигидрата NaBH4-2H2O, выше этой т-ры-в виде безводной соли. В системе NaBH4-NH3 образуются аммиакаты NaBH4.nNH3, где п = 3, 4, 5, конгруэнтно плавящиеся соотв. при —16 и — 20,6 °С. Гидразин, ДМФА, пиридин также образуют с натрия борогидридом сольваты.
По хим. св-вам натрия борогидрид -типичный представитель борогид-ридов металлов. Окисление натрия борогидрида на воздухе начинается при 300 °С, при этом образуются вода и NaBO2. Кристаллический натрия борогидрид с хлоридами металлов в зависимости от их природы взаимод. с образованием соответствующего боро-гидрида или диборана и металла (или гидрида) либо борида. В неводных р-рителях натрия борогидрид реагирует с галогенидами металлов I, II, III гр. и лантаноидов с образованием борогидри-дов; борогидриды переходных металлов образуются в присут. комплексообразователя (напр., R3P).
Получают натрия борогидрид взаимод. NaH или Na и Н2 с разл. соед. В:
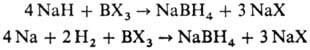
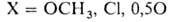
Др. группа способов основана на использовании диборана, напр.:
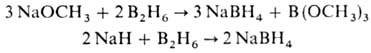
Натрия борогидрид используют как селективный восстановитель в орг. (для восстановления групп С=О, C=N, NO2, напр. при пром. произ-ве антибиотиков, витаминов, стeроидных препаратов) и неорг. синтезе, для получения бороводородов, борогидридов и гидридов др. металлов, катализаторов гид-рирования, для нанесения металлич. покрытий на разл. пов-сти из водных р-ров, как порообразователь для пластиков.
Натрия борогидрид токсичен при приеме внутрь, раздражает кожу. Особенно опасна пыль натрия борогидрида. Раздражают кожу также р-ры натрия борогидрида в жидком NH3, аминах и др.
Лит.: Жигач А.Ф., Стасиневич Д.С., Химия гидридов, Л.. 1969; Мальцева Н.Н., Хаип B.C., Борогидрид натрия, М., 1985.
А. И. Горбунов, П. А. Стороженко.
