Нитриты неорганические
НИТРИТЫ НЕОРГАНИЧЕСКИЕ, соли азотистой к-ты HNO2. Используют прежде всего нитриты щелочных металлов и аммония, меньше-щел.-зем. и 3d-металлов, Рb и Ag. О нитритах остальных металлов имеются только отрывочные сведения.
Нитриты металлов в степени окисления +2 образуют кристаллогидраты с одной, двумя или четырьмя молекулами воды. Нитриты образуют двойные и тройные соли, напр. CsNO2 x х AgNO2 или Ba(NO2)2•Ni(NO2)2•2KNO2, а также комплексные соед., напр. Na3[Co(NO2)6].
Кристаллич. структуры известны лишь для неск. безводных нитритов (см. табл.). Анион NO-2 имеет нелинейную конфигурацию; угол ONO 115°, длина связи N—О 0,115 нм; тип связи М—NO2 ионно-ковалентный.
СВОЙСТВА НЕКОТОРЫХ НЕОРГАНИЧЕСКИХ НИТРИТОВ
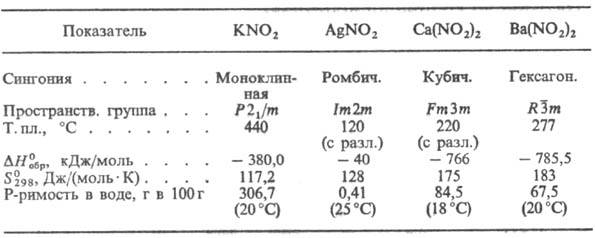
Хорошо раств. в воде нитриты К, Na, Ba, плохо-нитриты Ag, Hg, Сu. С повышением т-ры р-римость нитритов увеличивается. Почти все нитриты плохо раств. в спиртах, эфирах и малополярных р-рителях.
Нитриты термически малоустойчивы; плавятся без разложения только нитриты щелочных металлов, нитриты остальных металлов разлагаются при 25-300 °С. Механизм разложения нитритов сложен и включает ряд параллельно-последоват. р-ций. Осн. газообразные продукты разложения-NO, NO2, N2 и О2, твердые-оксид металла или элементный металл. Выделение большого кол-ва газов обусловливает взрывное разложение нек-рых нитритов, напр. NH4NO2, к-рый разлагается на N2 и Н2О.
Характерные особенности нитритов связаны с их термич. нестойкостью и способностью нитрит-иона быть как окислителем, так и восстановителем, в зависимости от среды и природы реагентов. В нейтр. среде нитриты обычно восстанавливаются до NO, в кислой окисляются до нитратов. Кислород и СО2 не взаимод. с твердыми нитритами и их водными р-рами. Нитриты способствуют разложению азотсодержащих орг. в-в, в частности аминов, амидов и др. С орг. галогенидами RX нитриты реагируют с образованием как нитритов RONO, так и нитросоединений RNO2.
Пром. получение нитритов основано на абсорбции нитрозно-го газа (смеси NO + NO2) р-рами Na2CO3 или NaOH с послед. кристаллизацией NaNO2; нитриты остальных металлов в пром-сти и лабораториях получают обменной р-цией солей металлов с NaNO2 или восстановлением нитратов этих металлов.
Анализ нитритов на нитрит-ион основан на его восстановлении сплавом Деварда (50% Сu, 45% Аl, 5% Zn) до NH3 и поглощении NH3 титрованными р-рами к-т. См. также Натрия нитрит.
Нитриты применяют для синтеза азокрасителей, в произ-ве капролактама, в качестве окислителей и восстановителей в резинотехн., текстильной и металлообрабатывающей пром-сти, как консерванты пищ. продуктов. Нитриты, напр. NaNO2 и KNO2, токсичны, вызывают головную боль, рвоту, угнетают дыхание и т.д. При отравлении NaNO2 в крови образуется метгемоглобин, повреждаются мембраны эритроцитов. Возможно образование нитрозаминов из NaNO2 и аминов непосредственно в желудочно-кишечном тракте.
Лит.: Миниович М. А., Миниович В. М., Соли азотистой кислоты. Нитриты, М., 1979. П.М. Чукуров.
