Свойства
Непредельные кислоты представляют собой или жидкости, или кристаллические вещества. Низшие кислоты растворимы в воде и обладают острым кислотным запахом. Кислоты этого ряда являются значительно более сильными кислотами (особенно те, у которых двойная связь находится рядом с карбоксильной группой), чем предельные жирные кислоты. Непредельные кислоты обладают всеми характерными свойствами органических кислот, т. е. способностью давать соли, хлорангидриды, ангидриды, сложные эфиры, амиды и прочие производные карбоновых кислот. Но, кроме того, наличие этиленовой связи придает этим кислотам способность вступать в свойственные этиленовым углеводородам реакции присоединения, а также способность легко расщепляться при реакциях окисления.
Кислоты с удаленными от карбоксильной группы этиленовыми связями, начиная с винилуксусной СН2=СН—СН2—СООН, обладают такой же способностью к реакциям присоединения, как и сами этиленовые углеводороды. Еще легче идут реакции присоединения, если этиленовая связь находится рядом с карбоксильной группой (α,β-ненасыщенные кислоты), как в акриловой кислоте СН2=СН—СООН и ее гомологах.
Из реакций, в которых участвует двойная связь (в первую очередь, реакций присоединения), можно отметить следующие:
1. Присоединение водорода. Кислоты типа акриловой кислоты особенно легко присоединяют водород при действии амальгамы натрия в водном растворе, превращаясь в предельные кислоты:

Гладко идет присоединение водорода при гидрировании в жидкой фазе в присутствии катализаторов (Ni, Pt, Pd). 2. Присоединение галоида, например:
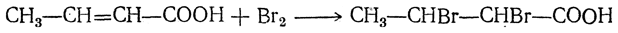
3. Присоединение галоидоводородов. Эта реакция особенно легко идет для α,β-ненасыщенных кислот, причем атом галоида всегда присоединяется к более удаленному от карбоксильной группы атому углерода, например:
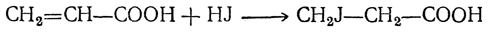
4. Присоединение воды. Акриловая кислота и ее гомологи (α,β-ненасыщенные кислоты) под действием, например, серной кислоты легко присоединяют воду с образованием β-оксикислот:
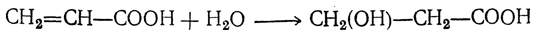
β,γ-Ненасыщенные кислоты под влиянием серной кислоты дают соединения, называемые лактонами;
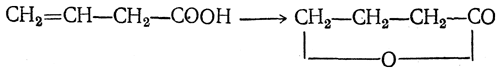
5. Присоединение аммиака. Присоединяя молекулу аммиака, α,β-ненасыщенные кислоты дают β-аминокислоты:
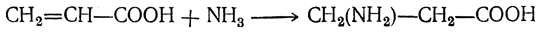
Особенности реакций присоединения в случае α,β-ненасыщенных кислот объясняются наличием в них сопряженных двойных связей, а именно углерод-углеродной и углерод-кислородной:
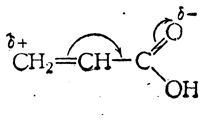
Благодаря этому присоединение идет прежде всего в положении 1,4, т. е. к крайнему атому углерода этиленовой связи и к атому кислорода карбонильной группы.
Присоединение водорода дает сначала двухатомный спирт, немедленно изомеризующийся (как показано стрелкой) в пропионовую кислоту
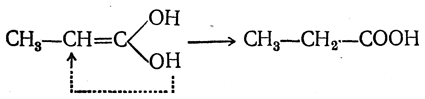
Присоединение бромистого водорода сначала дает бромзамещенный двухатомный спирт, а затем β-бромпропионовую кислоту:
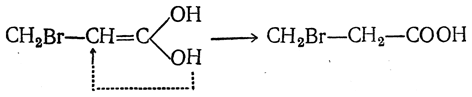
Таким образом объясняется особая легкость восстановления кислот этого типа, а также протекание реакции не в согласии с правилом Марковникова, т. е. то, что галоид галоидоводорода (или гидроксил в случае гидратации) присоединяется к более гидрогенизированному атому углерода, всегда образуя β-замещенные производные кислот.
Присоединение же галоидов в положение 1,2 объясняется тем, что кислород не обладает склонностью соединяться с галоидами.
6. Окисление. При окислении перманганатом в щелочной среде образуются диоксикислоты:
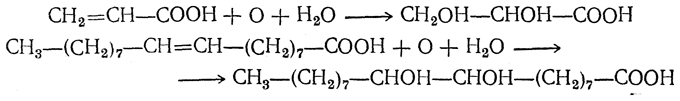
Более энергичное окисление приводит к расщеплению молекулы кислоты по месту двойной связи. Благодаря этому по числу атомов углерода в продуктах расщепления можно установить положение двойной связи в исходной молекуле.
В зависимости от строения исходной ненасыщенной кислоты продуктами окисления могут быть одноосновные и двухосновные кислоты, а также кетоны, кетонокислоты и продукты дальнейшего окисления первичных продуктов реакции. Так, олеиновая кислота
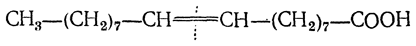
при окислении дает одноосновную кислоту С8Н17СООН и двухосновную кислоту С7Н14(СООН)2; кислота строения
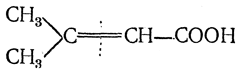
дает ацетон (СН3)2СО и щавелевую кислоту НООС—СООН.
При некоторых реакциях окисления может происходить изомеризация, состоящая в перемещении двойной связи, вследствие чего получаются продукты окисления, не отвечающие структуре исходного соединения; это затрудняет суждение о строении ненасыщенной кислоты. Такие ненормальные продукты окисления иногда получаются при окислении в присутствии сильных минеральных кислот, а также при сплавлении ненасыщенных кислот с едкими щелочами. Так, например, при сплавлении олеиновой кислоты с едкими щелочами молекула ее расщепляется, но продуктами окисления являются кислоты пальмитиновая С15Н31СООН и щавелевая НООС—СООН, что объясняется, вероятно, превращением олеиновой кислоты в изомерную ей α,β-ненасыщенную кислоту:

7. Превращение стереоизомерных кислот друг в друга. У стереоизомерных ненасыщенных кислот, изомерия которых определяется наличием двойной связи (цис-транс-изомерия, стр. 89), наблюдаются чрезвычайно характерные взаимные отношения. Они заключаются в том, что из двух стереоизомерных кислот одна является более устойчивой, чем другая, причем неустойчивый изомер («лабильная» форма) может в определенных условиях превращаться в устойчивый («стабильная» форма):

Превращение иногда происходит при простом нагревании, в других же случаях — при действии химических агентов (концентрированная серная кислота, едкая щелочь при кипячении, следы азотистой кислоты). Быстро и количественно такое превращение идет в присутствии следов иода или брома под действием прямого солнечного света.
Обратное превращение происходит при действии ультрафиолетовых лучей и может быть, кроме того, осуществлено химическим путем.


