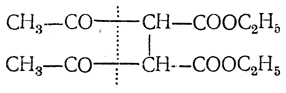
Реакции ацетоуксусного эфира
Из многочисленных реакций ацетоуксусного эфира укажем следующие, наиболее характерные:
1. Восстановление водородом. При восстановлении ацетоуксусного эфира водородом in statu nascendi получается β-оксикислота:
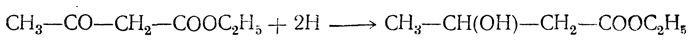
2. Действие синильной кислоты. При взаимодействии с синильной кислотой получается циангидрин строения СН3—С(ОН)(CN)—СН2—СООС2Н5.
3. Образование бисульфитных соединений. С кислым сернистокислым натрием получается соответствующий кетонам продукт присоединения.
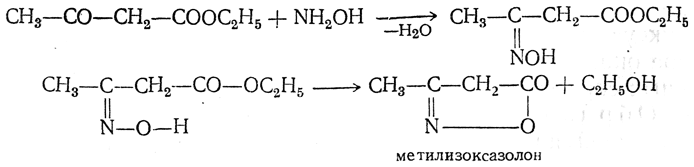
4. Действие г и д р о к с и л а м и н а. Оксим, который должен был бы образоваться в результате реакции с гидроксиламином, превращается с отщеплением молекулы спирта в метилизоксазолон:
5. Действие фенилгидразин а. При действии фенилгидразина, как и при реакции с гидроксиламином, получается гетероциклическое соединение — фенилметилпиразолон:
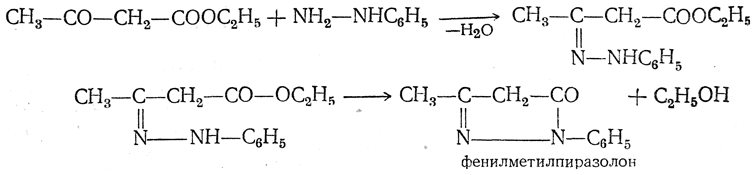
Все приведенные реакции хорошо объясняются кетонным строением ацетоуксусного эфира. Далее рассматриваются реакции, приводящие к веществам с этиленовой связью, родственным оксикротоновому эфиру.
6. Действие галоидангидридов. Действием галоидангидридов в присутствии органических оснований (пиридина) получаются сложные эфиры оксикротонового эфира:
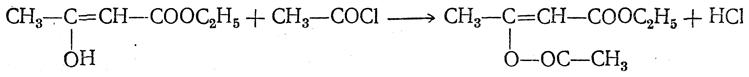
7. Действие аммиака. Действием аммиака получается β-аминокротоновая кислота:
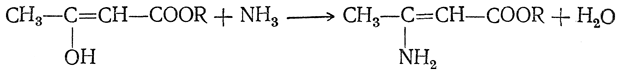
8. Действие пяти хлористого фосфора приводит к образованию β-хлоркротонового эфира:
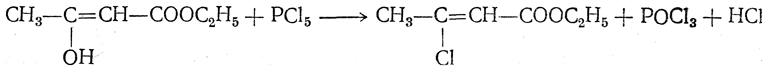
Образование хлоркротонового эфира может, однако, объясняться отщеплением хлористого водорода от продукта нормальной кетонной реакции — эфира β,β-дихлормасляной кислоты:
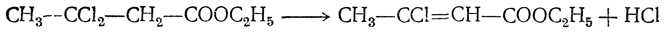
9. Реакция с хлорным железом. Обыкновенный ацетоуксусный эфир дает с хлорным железом интенсивное фиолетовое окрашивание. Эта реакция чрезвычайно характерна для енольных соединений и совершенно отсутствует у кетонов.
10. Образование С-п роизводных. Чрезвычайно важной реакцией является способность ацетоуксусного эфира при действии натрия, а также при осторожном действии водными или спиртовыми щелочами (алкоголятами) замещать атом водорода на натрий и образовывать соединение, известное под названием натрийацетоуксусного эфира. Это соединение представляет собой натриевое производное енольной формы ацетоуксусного эфира:
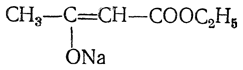
То, что натрийацетоуксусный эфир имеет такое строение, а не представляет собой смесь таутомеров
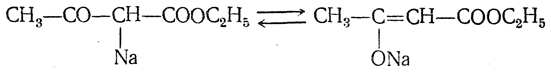
явствует из результатов исследований (А. Н. Несмеянов и сотр.) натриевых, литиевых и магниевых енолятов дифенилпропиомезитилена — соединения, вполне аналогичного ацетоуксусному эфиру. Этот енолят имеет следующее строение (пунктиром выделена часть молекулы, имеющаяся и в натрийацетоуксусном эфире):
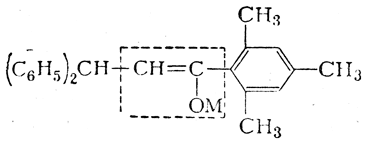
Отсутствие таутомерии здесь доказывается существованием цис- и транс-форм енолятов, выделенных в индивидуальном виде и не способных к взаимному превращению в растворах. Стереоизомерные еноляты способны к образованию и С-производных и О-производных, причем при образовании О-производных не изменяется пространственная конфигурация молекулы. Следовательно, рассматриваемое соединение может иметь строение только енола и его двойственная реакционная способность не вызвана таутомерией. Способность енолятов дифенилпропиомезитилена образовывать не только О-производные, но и С-производные может быть объяснена как результат эффекта сопряжения и переноса реакционного центра от атома кислорода (связанного с металлом) к углероду метинной группы:
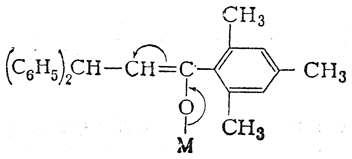
Аналогично может быть объяснена двойственная реакционная способность натрийацетоуксусного эфира:
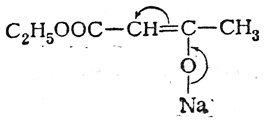
При действии на натрийацетоуксусный эфир всевозможных галоидных соединений радикал, вступающий вместо натрия в молекулу ацетоуксусного эфира, в получаемых соединениях оказывается связанным с атомом углерода. Так, например, из галоидных алкилов и натрийацетоуксусного эфира получаются гомологи ацетоуксусного эфира:
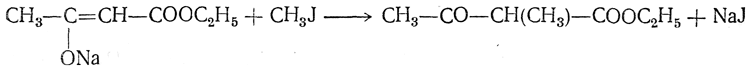
Однозамещенные гомологи ацетоуксусного эфира могут заменять еще один атом водорода на натрий, и с ними могут быть произведены дальнейшие синтезы:
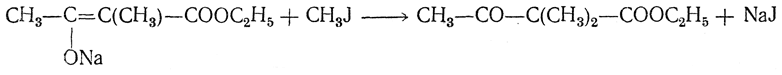
Двухзамещенные гомологи ацетоуксусного эфира не способны реагировать с натрием, и вместе с тем они не дают никаких реакций, отвечающих енольному строению.
11. Образование О-п р о и з в о д н ы х. В более редких случаях натрийацетоуксусный эфир может реагировать, образуя производные оксикротонового эфира, т. е. радикал, входящий вместо натрия, связывается с кислородом (образуются так называемые О-производные). Преимущественно в этом направлении реагирует с натрийацетоуксусным эфиром хлоругольный эфир:
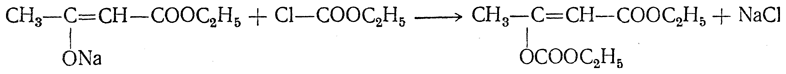
Однако наряду с О-соединением получается также и С-соединение:
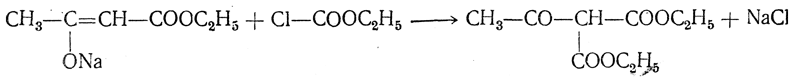
12. Действие кислот и щелочей. Концентрированные щелочи при нагревании производят так называемое кислотное расщепление β-кетонокислот, образующихся в результате омыления ацетоуксусного эфира. При этом молекула β-кетонокислоты распадается на две молекулы одноосновных кислот, например:
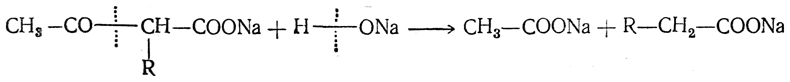
На этой реакции основаны многочисленные синтезы с помощью ацетоуксусного эфира, аналогичные синтезам с малоновым эфиром и позволяющие получать различные гомологи уксусной кислоты, а также ряд более сложных кислот.
Разбавленные щелочи на холоду омыляют эфиры β-кетонокислот, причем получается спирт и соль β-кетонокислоты. При нагревании соль и особенно легко — свободная кислота, получающаяся при подкислении раствора соли, распадаются на СО2 и кетон (кетонное расщепление β-кетонокислот):

Такая же реакция происходит и при кипячении эфиров β-кетонокислот с минеральными кислотами.
Методом кетонного расщепления удалось осуществить множество синтезов кетонов.
13. Действие иода. Действие иода на натрийацетоуксусный эфир приводит к образованию диацетилянтарного эфира
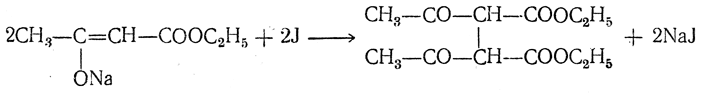
который может далее подвергаться кетонному или кислотному расщеплению. При кетонном расщеплении получается ацетонилацетон
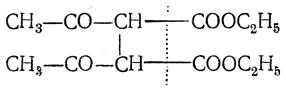
при кислотном — смесь уксусной и янтарной кислот