Окисление - восстановление
Окисление-восстановление, окислительно-восстановительные реакции, химические реакции, сопровождающиеся изменением окислительных чисел атомов. Первоначально (со времени введения в химию кислородной теории горения А. Лавуазье, конец 18 в.) окислением назывались только реакции соединения с кислородом, восстановлением — отнятие кислорода. С введением в химию электронных представлений (1920—30) оказалось возможным широко обобщить понятие окисления-восстановления и распространить его на реакции, в которых кислород не участвует. Согласно электронной теории, окислением называется отдача электронов атомом, молекулой или ионом: Zn – 2 = Zn2+.
= Zn2+.
Восстановлением называется присоединение электронов атомом, молекулой или ионом: Cl2 + 2 = 2Cl–.
= 2Cl–.
Окислителями называется нейтральный атом, молекула или ион, принимающие электроны (во втором примере молекула хлора Cl2), восстановителями — нейтральный атом, молекула или ион, отдающие электроны (в первом примере — атом Zn). Окисление и восстановление — взаимосвязанные процессы, которые всегда протекают одновременно. Когда одно вещество окисляется, то другое восстанавливается, и наоборот. Так, приведённые выше частные реакции окисления и восстановления составляют единый процесс окисления-восстановления: Zn + Cl2 = ZnCl2.
Здесь Zn окисляется до Zn2+, а Cl2 восстанавливается до 2Cl–.
В химии окислительно-восстановительные реакции принадлежат к числу наиболее распространённых. Например, на них, как правило, основано получение простых веществ (металлов и неметаллов)
CuO + H2 =Cu + H2O,
2КВг + Cl2 = Br2 + 2KCl.
В основе технического производства таких важнейших химических продуктов, как аммиак, азотная кислота, серная кислота, процессов сжигания топлива и горения также лежат реакции окисления-восстановления. В гальванических элементах (см. Химические источники тока) возникновение электродвижущей силы обусловлено протеканием реакции окисления-восстановления. При проведении электролиза на аноде происходит электрохимическое окисление, на катоде — электрохимическое восстановление. Например, при производстве хлора электролизом раствора NaCl на аноде идёт реакция Cl– – 1 = 1/2Cl2 (окисление аниона Cl–), на катоде Н+ + 1
= 1/2Cl2 (окисление аниона Cl–), на катоде Н+ + 1 =1/2Н2 (восстановление катиона Н+). Коррозия металлов также связана с реакциями окисления-восстановления и заключается в окислении металлов.
=1/2Н2 (восстановление катиона Н+). Коррозия металлов также связана с реакциями окисления-восстановления и заключается в окислении металлов.
Дыхание, усвоение растениями углекислого газа с выделением кислорода (см. Фотосинтез), обмен веществ и др. биологически важные явления представляют собой реакции окисления-восстановления (см. Окисление биологическое).
При составлении уравнений реакций окисления-восстановления основная трудность заключается в подборе коэффициентов, особенно для реакций с участием соединений, в которых химическая связь носит не ионный, а ковалентный характер. В этом случае полезны понятия электроотрицательности и окислительного числа (степени окисления). Электроотрицательность — способность атома в молекуле притягивать и удерживать около себя электроны. Степень окисления — такой заряд, который возник бы на атоме в молекуле, если бы каждая пара электронов, связывающая его с др. атомами, была полностью смещена к более электроотрицательному атому (см. Валентность). Нахождение степени окисления атома в молекуле основано на том, что молекула в целом должна быть электрически нейтральной. При этом учитывается, что степень окисления атомов некоторых элементов в соединениях всегда постоянна (щелочные металлы +1, щёлочноземельные металлы и цинк +2, алюминий +3, кислород, кроме перекисей, –2 и т.д.). Степень окисления атома в простых веществах равна нулю, а одноатомного иона в ионном соединении равна заряду этого иона. Например, рассчитаем степень окисления атома Cr в соединении K2Cr2O7. Пользуясь постоянными значениями степеней окисления для К и О, имеем 2·(+1) + 7·(–2) = –12. Следовательно, степень окисления одного атома Cr (чтобы сохранить электронейтральность молекулы) равна +6. На основе введённых понятий можно дать другое определение окисления-восстановления: окислением называется увеличение степени окисления, восстановлением называется понижение степени окисления.
Восстановителями являются почти все металлы в свободном состоянии, отрицательно заряженные ионы неметаллов (S2– – 2 = S°), положительно заряженные ионы металлов в низшей степени окисления (
= S°), положительно заряженные ионы металлов в низшей степени окисления (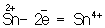 ), сложные ионы и молекулы, содержащие атомы в промежуточной степени окисления (
), сложные ионы и молекулы, содержащие атомы в промежуточной степени окисления ( ,
, 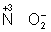 ). В промышленности и технике широко используются такие восстановители, как углерод и окись углерода (восстановление металлов из окислов)
). В промышленности и технике широко используются такие восстановители, как углерод и окись углерода (восстановление металлов из окислов)
ZnO + С = Zn + СО, FeO +СО = Fe + СО2.
сульфит натрия Na2SO3 и гидросульфит натрия NaHSO3 — в фотографии и красильном деле, металлический натрий и свободный водород — для получения чистых металлов
TiCl4 + 4Na = Ti + 4NaCI,
GeO2 +2Н2 = Ge + 2H2O.
Окислителями могут быть нейтральные атомы неметаллов (в особенности галогенов и кислорода), положительно заряженные ионы металлов в высшей степени окисления (Sn4+ + 2 = Sn2+), сложные ионы и молекулы, содержащие атомы элементов в более высокой степени окисления (
= Sn2+), сложные ионы и молекулы, содержащие атомы элементов в более высокой степени окисления (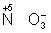 ,
,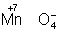 ,
,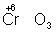 ). Промышленное значение как окислители имеют: кислород (особенно в металлургии), озон, хромовая и двухромовая кислоты и их соли, азотная кислота, перекись водорода, перманганат калия, хлорная известь и др. Самый сильный окислитель — электрический ток (окисление происходит на аноде).
). Промышленное значение как окислители имеют: кислород (особенно в металлургии), озон, хромовая и двухромовая кислоты и их соли, азотная кислота, перекись водорода, перманганат калия, хлорная известь и др. Самый сильный окислитель — электрический ток (окисление происходит на аноде).
Для подбора коэффициентов в уравнениях реакций окисления-восстановления служит общее правило: число электронов, отданных восстановителем, должно равняться числу электронов, принятых окислителем. Применяют обычно два метода подбора коэффициентов: метод электронного баланса и электронно-ионный метод.
В методе электронного баланса подсчёт числа принятых и отданных электронов производят на основании значений степеней окисления элементов до и после реакции. Например,
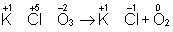
Таким образом, 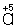 является окислителем, а
является окислителем, а 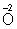 — восстановителем. Составляют частные реакции окисления и восстановления:
— восстановителем. Составляют частные реакции окисления и восстановления:
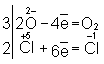
В соответствии с приведённым выше правилом числа отданных и принятых электронов уравнивают. Полученные величины подставляют в исходное уравнение:
2KClO3 = 2KCl + 3O2.
В электронно-ионном методе схему реакции записывают в соответствии с общими правилами составления ионных реакций, т. е. сильные электролиты записывают в виде ионов, а неэлектролиты, слабые электролиты, газы и осадки — в виде молекул. Не изменяющиеся в результате реакции ионы в такую схему не входят. Например,
KMnO4 + KI + H2SO4 ® K2SO4 + I2+ MnSO4 + H2O,
в ионном виде:
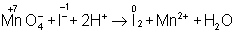
Рассчитав степени окисления, определяют окислитель и восстановитель и составляют частные реакции окисления и восстановления:
2I– – 2 = I2,
= I2,
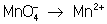
Во втором уравнении, перед тем как записать переход электронов, необходимо составить «материальный» баланс, т.к. в левой части уравнения есть атомы О, а в правой их нет. Избыточные атомы О связываются в молекулы воды ионами Н+, присутствующими в сфере реакции (кислая среда):
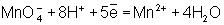
Далее, как и в первом методе, находят коэффициенты-множители к частным уравнениям для достижения электронного баланса (в приведённом примере 5 и 2 соответственно). Окончательное уравнение имеет вид:
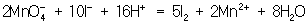 .
.
Полученные коэффициенты подставляют в исходное уравнение:
2KMnO4 + 10KI + 8H2SO4 = 6K2SO4 + 5I2 + 2MnSO4 + 8H2O.
Аналогично составляют и уравнения реакций окисления-восстановления в щелочной среде (вместо ионов Н+ в частных уравнениях фигурируют ионы OH–). Т. о. , в уравнивании реакций по второму методу учитывают характер реакционной среды (кислая или щелочная либо нейтральная), которая сильно влияет и на направление реакции окисления-восстановления и на продукты, получаемые в результате реакции. Например, равновесие окислительно-восстановительной реакции 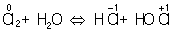 в кислой среде смещено влево, а в щелочной — вправо. Сильный окислитель ион
в кислой среде смещено влево, а в щелочной — вправо. Сильный окислитель ион 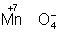 в кислой среде восстанавливается до иона Mn2+, в щелочной среде — до иона
в кислой среде восстанавливается до иона Mn2+, в щелочной среде — до иона 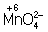 , в нейтральной — до молекулы
, в нейтральной — до молекулы  . См. также Окисление металлов, Восстановление металлов.
. См. также Окисление металлов, Восстановление металлов.
Лит.: Кудрявцев А. А., Составление химических уравнений, М., 1968; Химия. Курс для средней школы, пер. с англ., 2 изд., М., 1972, гл. 12; Химия. Пособие для преподавателей средней школы, пер. с англ., ч. 1, М., 1973, гл. 12.
В. К. Бельский.
