Диазоаминосоединения
ДИАЗОАМИНОСОЕДИНЕНИЯ (триазены), моно-, ди- или тризамещенные производные не выделенного соединения - триазена 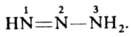 Все заместители м.б. орг. радикалами либо один из них - группой ОН (N-гидрокситриазены), NO2 (N-нитротриазены), NO (N-нитрозотриазены), СООН (триазен-N-карбоновые к-ты), SO3H (триазен-N-сульфокислоты). Наиб. значение имеют ди- и тризамещенные диазоаминосоединения, а из них - ароматич. и жирно-ароматические. диазоаминосоединения - бесцв. или желтые гл. обр. твердые в-ва. Плавятся с разл.; при 100-150°С взрываются. Хорошо раств. в орг. р-рителях; в воде раств. диазоаминосоединения, содержащие группы СООН, SO3 или ОН. Лучший метод очистки нек-рых диазоаминосоединений - перегонка с водяным паром и хроматография. Для диазоаминосоединений, как и для прочих стабильных диазосоединений, термодинамически устойчива транс-конфигурация, к-рая переходит в циc-конфигурацию при УФ облучении. Диазоаминосоединения - более сильные основания, чем азосоединения. При их протонировании образуется неустойчивый диазоаммониевый катион, диссоциирующий на катион диазония и амин:
Все заместители м.б. орг. радикалами либо один из них - группой ОН (N-гидрокситриазены), NO2 (N-нитротриазены), NO (N-нитрозотриазены), СООН (триазен-N-карбоновые к-ты), SO3H (триазен-N-сульфокислоты). Наиб. значение имеют ди- и тризамещенные диазоаминосоединения, а из них - ароматич. и жирно-ароматические. диазоаминосоединения - бесцв. или желтые гл. обр. твердые в-ва. Плавятся с разл.; при 100-150°С взрываются. Хорошо раств. в орг. р-рителях; в воде раств. диазоаминосоединения, содержащие группы СООН, SO3 или ОН. Лучший метод очистки нек-рых диазоаминосоединений - перегонка с водяным паром и хроматография. Для диазоаминосоединений, как и для прочих стабильных диазосоединений, термодинамически устойчива транс-конфигурация, к-рая переходит в циc-конфигурацию при УФ облучении. Диазоаминосоединения - более сильные основания, чем азосоединения. При их протонировании образуется неустойчивый диазоаммониевый катион, диссоциирующий на катион диазония и амин:
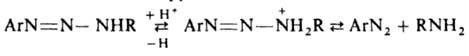
Кислотный гидролиз диазоаминосоединений широко используется для генерирования катионов диазония. Диазоаминосоединения, содержащие остаток ароматич. амина, у к-рого свободно пара- или орто-положение, в кислой среде в присут. соответствующего амина при 40-50°С перегруппировываются в аминоазосоединения по межмолекулярному механизму кислотного гидролиза (с образованием соли диазония и послед. ее азосочетанием с амином):
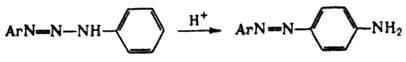
Диазоаминосоединения проявляют также кислотные св-ва, в частности способность к N-металлированию: ArN=N—NHR + MX : ArN=N—NMR + HX, где М = Ag, Cu, Hg или др., Х = NO3, Cl, OCOCH3 или др. Металлированные диазоаминосоединения присоединяют NH3, пиридин, тиомочевину и др. основания, а также р-рители (напр., спирт, ацетон, воду), образуя прочные ярко окрашенные комплексы.
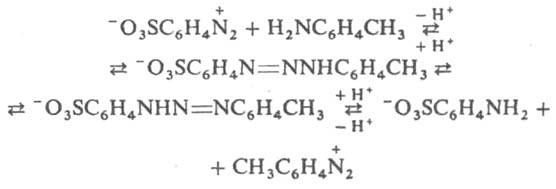
Восстанавливаются диазоаминосоединения обычно в производные гидразина и ариламина:
ArNH—N=N—Аr + 2Н2 : ArNH2 + ArNHNH2
Термич. распад диазоаминосоединений происходит с выделением N2 и своб. радикалов 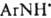 ,
, 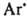 и
и 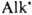 , диспропорционирование и рекомбинация к-рых со средой приводят к образованию ArNH2, АrН, Аr2 и др. углеводородов. Осн. способ получения диазоаминосоединений - взаимод. солей диазония с первичными или вторичными аминами при 0-20 °С чаще всего в воде (реже - в этаноле, уксусной или муравьиной к-те, а также в полярных апротонных р-рителях, напр. ДМФА). Образование диазоаминосоединений по аналогии с азосочетанием следует рассматривать как электроф. замещение у атома N аминогруппы с промежут. образованием диазоаммониевого катиона, концентрация к-рого мала и постоянна:
, диспропорционирование и рекомбинация к-рых со средой приводят к образованию ArNH2, АrН, Аr2 и др. углеводородов. Осн. способ получения диазоаминосоединений - взаимод. солей диазония с первичными или вторичными аминами при 0-20 °С чаще всего в воде (реже - в этаноле, уксусной или муравьиной к-те, а также в полярных апротонных р-рителях, напр. ДМФА). Образование диазоаминосоединений по аналогии с азосочетанием следует рассматривать как электроф. замещение у атома N аминогруппы с промежут. образованием диазоаммониевого катиона, концентрация к-рого мала и постоянна:
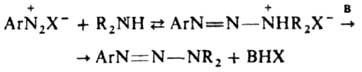
[В-р-ритель, а также основания, напр., пиридин и его аналоги, анионы слабых к-т (фталевой, уксусной и пр.)]. Т. к. скорость образования диазоаминосоединений в значит. степени лимитируется отрывом протона от диазоаммониевого катиона, р-ция катализируется основаниями. Для успешного образования диазоаминосоединения необходимо, чтобы не происходил его гидролиз. Поэтому чем основнее диазоаминосоединение, тем ниже должна быть кислотность среды при его образовании (получение ароматич. диазоаминосоединения из компонентов с электронодонорными заместителями нельзя вести в кислой среде). При взаимод. соли диазония с алифатич. амином среда должна быть слабощелочной. Если используется первичный алифатич. амин, происходит замена второго атома Н в амине с образованием бис-диазоаминосоединения (пентаза-1,4-диена) ArN=N—N(Alk)—N=NAr. Диазоаминосоединения не образуются при р-ции соли диазония с нафтиламинами. Многие диазоаминосоединения синтезируют взаимод. магнийорг. соединений с азидами:
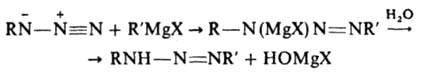
(X - галоген, R и R' - алифатич. или ароматич. радикалы). Осн. метод анализа и идентификации ароматич. и жирно-ароматич. диазоаминосоединений - кислотный гидролиз с послед, азосочетанием с нафтолами и колориметрич. определение азокрасителя. Для анализа диазоаминосоединений используется также цветная р-ция образования кадмиевого производного. В пром-сти диазоаминосоединения применяют для получения аминоазосоединений (азосоставляющая - анилин, N-алкиланилины и их производные), для крашения (компоненты диазаминолов; см. Азогены). Диазоаминосоединения открыты П. Гриссом в 1862.
