Неорганические полимеры
НЕОРГАНИЧЕСКИЕ ПОЛИМЕРЫ. Имеют неорг. главные цепи и не содержат орг. боковых радикалов. Главные цепи построены из ковалентных или ионно-ковалентных связей; в нек-рых неорганических полимерах цепочка ионно-ковалентных связей может прерываться единичными сочленениями координац. характера. Структурная классификация неорганических полимеров осуществляется по тем же признакам, что и орг. или элементоорг. полиме-ров (см. Высокомолекулярные соединения). Среди природных неорганических полимеров наиб. распространены сетчатые, входящие в состав большинства минералов земной коры. Многие из них образуют кристаллы типа алмаза или кварца. К образованию линейных неорганических полимеров способны элементы верх. рядов III-VI гр. периодич. системы. Внутри групп с увеличением номера ряда способность элементов к образованию гомо- или гете-роатомных цепей резко убывает. Галогены, как и в орг. полимерах, играют роль агентов обрыва цепи, хотя всевозможные их комбинации с др. элементами могут составлять боковые группы. Элементы VIII гр. могут входить в главную цепь, образуя координац. неорганические полимеры. Последние, в принципе, отличны от орг. координационных полимеров, где система координац. связей образует лишь вторичную структуру. Мн. оксиды или соли металлов переменной валентности по макроскопич. св-вам похожи на сетчатые неорганические полимеры.
Длинные гомоатомные цепи (со степенью полимеризации п >= 100) образуют лишь углерод и элементы VI гр.-S, Se и Те. Эти цепи состоят только из основных атомов и не содержат боковых групп, но электронные структуры углеродных цепей и цепей S, Se и Те различны. Линейные полимеры углерода - кумулены =С=С=С=С= ... и кар-бин —С=С—С=С—... (см. Углерод); кроме того, углерод образует двухмерные и трехмерные ковалентные кристаллы-соотв. графит и алмаз. Сера, селен и теллур образуют атомные цепочки с простыми связями и очень высокими п. Их полимеризация имеет характер фазового перехода, причем температурная область стабильности полимера имеет размазанную нижнюю и хорошо выраженную верхнюю границы. Ниже и выше этих границ устойчивы соотв. циклич. октамеры и двухатомные молекулы.
Др. элементы, даже ближайшие соседи углерода по псриодич. системе-В и Si, уже неспособны к образованию гомоатомных цепей или циклич. олигомеров с п >= 20 (безотносительно к наличию или отсутствию боковых групп). Это обусловлено тем, что лишь атомы углерода способны образовывать друг с другом чисто ковалентные связи. По этой причине более распространены бинарные гетероцепные неорганические полимеры типа [—М—L—]n (см. табл.), где атомы М и L образуют между собой ионно-ковалентные связи. В принципе, гетероцепные линейные неорганические полимеры не обязательно должны быть бинарными: регулярно повторяющийся участок цепи м. б. образован и более сложными комбинациями атомов. Включение в главную цепь атомов металлов дестабилизирует линейную структуру и резко снижает и.
КОМБИНАЦИИ ЭЛЕМЕНТОВ, ОБРАЗУЮЩИЕ БИНАРНЫЕ ГЕТЕРОЦЕПНЫЕ НЕОРГАНИЧЕСКИЕ ПОЛИМЕРЫ ТИПА [—М—L—]n (ОБОЗНАЧЕНЫ ЗНАКОМ +)
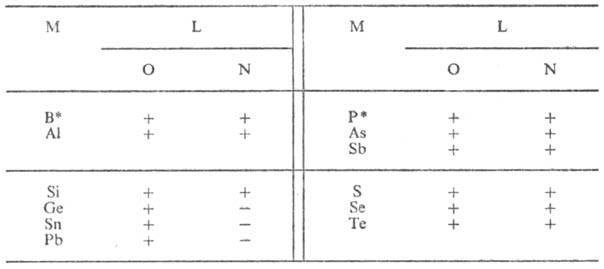
* Образует также неорг. полимеры состава [—В—Р—]n.
Особенности электронной структуры главных цепей гомо-цепных неорганических полимеров делают их весьма уязвимыми при атаке нуклеоф. или электроф. агентами. Уже по одной этой причине относительно стабильнее цепи, содержащие в качестве компонента L кислород или др. атом, соседний с ним по периодич. системе. Но и эти цепи нуждаются обычно в стабилизации, к-рая в прир. неорганических полимерах связана с образованием сетчатых структур и с очень сильным межмол. взаимод. боковых групп (включая образование солевых мостиков), в результате к-рого большинство даже линейных неорганических полимеров не-растворимы и по макроскопич. св-вам сходны с сетчатыми неорганическими полимерами.
Практич. интерес представляют линейные неорганические полимеры, к-рые в наиб. степени подобны органическим - могут существовать в тех же фазовых, агрегатных или релаксационных состояниях, образовывать аналогичные надмол. структуры и т.п. Такие неорганические полимеры могут быть термостойкими каучуками, стеклами, волокнообразующими и т.п., а также проявлять ряд св-в, уже не присущих орг. полимерам. К ним относятся полифосфазены, полимерные оксиды серы (с разными боковыми группами), фосфаты, силикаты. Нек-рые комбинации М и L образуют цепи, не имеющие аналогов среди орг. полимеров, напр. полупроводники с широкой зоной проводимости и сверхпроводники. Широкой зоной проводимости обладает графит, имеющий хорошо развитую плоскую или пространств. структуру. Обычным сверхпроводником при т-ре вблизи 0 К является полимер [—SN—]х; при повышенных т-рах он утрачивает сверхпроводимость, но сохраняет полупроводниковые св-ва. Высокотемпературные сверхпроводящие неорганические полимеры должны обладать структурой керамик, т. е. обязательно содержать в своем составе металлы (в боковых группах) и кислород.
Переработка неорганических полимеров в стекла, волокна, ситаллы, керамику и т. п. требует плавления, а оно, как правило, сопровождается обратимой деполимеризацией. Поэтому используют обычно модифицирующие добавки, позволяющие стабилизировать в расплавах умеренно разветвленные структуры.
Лит.: Энциклопедия полимеров, т. 2, М., 1974, с. 363-71; Бартенев Г. М., Сверхпрочные и высокопрочные неорганические стекла, М., 1974; Кор-шак В. В., Козырева Н. М., "Успехи химии", 1979, т. 48, в. 1, с. 5-29; Inorganic polymers, в кн.: Encyclopedia of polymer science and technology, v. 7, N. Y.-L.-Sydney, 1967, p. 664-91. С.Я. Френкель.
