Антимониды
АНТИМОНИДЫ (стибниды), соед. сурьмы с металлами. Кристаллич. в-ва с металлич. блеском, обычно серебристо-белого или серого цвета, с относительно высокими т-рами плавления. Обладают металлич. или полупроводниковой проводимостью; нек-рые антимониды при низких т-рах-сверхпроводники. Щелочные металлы образуют антимониды состава M3Sb, MSb и, начиная с К, MSb2 и др. Число образуемых антимонидов увеличивается от Li к Cs. Для соед. M3Sb характерна гексаген. Кристаллич. решетка типа Na3As, для MSb-моноклинная типа LiAs, для MSb2-моноклинная типа MgCu2. Антимониды щелочных металлов - полупроводники с шириной запрещенной зоны 1,0-1,5 эВ. Медь и серебро образуют по неск. бер-толлидных фаз; для Си известен также Cu2Sb. Получены только высшие антимониды Au-AuSb2 и AuSb3.
Для элементов II группы характерно образование M3Sb2. Для Be и Mg известны антимониды только такого состава; другие щел.-зем. металлы дают ряд антимонидов, в т.ч. MSb и MSb3, причем число соед. увеличивается от Са к Ва. Цинк и кадмий образуют антимониды составов M3Sb2, MSb и M3Sb4, ртуть-Hg3Sb2.
Металлы подгруппы Ilia образуют антимониды состава MSb, имеющие наиб. практич. значение. Все они, кроме металло-подобного TISb, кристаллизуются в кубич. решетке типа сфалерита и являются полупроводниками. С ростом атомного номера металла увеличиваются межатомные расстояния в молекулах, понижаются т-ры плавления, ширина запрещенной зоны и энергия диссоциации, уменьшается твердость и повышается плотность соединений. Элементы подгруппы III6, включая лантаноиды и актиноиды, образуют ряд антимонидов, из к-рых наиб. характерны: MSb (со структурой типа NaCl), M2Sb (с тетрагон, кристаллич. решеткой), M4Sb3, MSb2 (с моноклинной или тетрагон, решеткой), M5Sb3 (с гексагон. решеткой типа Mn5Si3).
Из элементов подгруппы IVa только для Sn известен SnSb (с кубич. кристаллич. решеткой). Переходные металлы IV-VIII групп образуют разнообразные антимониды, из к-рых чаще других встречаются MSb, MSb2, MSb3, M2Sb, M3Sb. Число соед. при переходе от IV группы к VI уменьшается, а далее, начиная с подгруппы Со, снова увеличивается. При переходе от четвертого к шестому периоду наблюдается тенденция к уменьшению числа антимонидов, наиб. число антимонидов у Ni (6), V и Rh (по 5). Для Сг, Mn, Fe, Ru известно по два антимонида, для Mo, W и Os - пo одному (Mo3Sb7, WSb и OsSb2). Большинство соед. состава MSb имеет гексагон. кристаллич. решетку типа NiAs или ромбическую типа МпР. Для MSb2 характерна структура типа пирита или марказита. Соед. M2Sb кристаллизуются обычно в тетрагон. решетке типа Cu2Sb. Элементы подгруппы Со образуют антимониды состава MSb3 с кубич. кристаллич. решеткой типа CoAs3, элементы подгруппы Ti и V - соед. M3Sb с кубич. решеткой типа или Cr3Si.
или Cr3Si.
Большинство антимонидов переходных элементов металлоподобны, нек-рые соед. MSb2 и особенно MSb3 - полупроводники, причем с увеличением атомной массы металла в пределах группы ширина запрещенной зоны возрастает. Нек-рые антимониды при низких т-рах становятся сверхпроводниками, наиб. высокие т-ры перехода у Nb5Sb4 (8,60 К), Ti3Sb (5,80 К). Нек-рые антимониды - антиферромагнетики с относительно высокими точками Нееля: 723 К для CrSb, 213 К для USb. Другие, напр. MnSb, MnSb2, - ферромагнетики, для к-рых характерны анизотропия магн. св-в и изменение с т-рой направления наиб. магн. восприимчивости.
Известен ряд двойных антимонидов, напр.: LiCdSb, K2CuSb2, BaZn2Sb2, TiSnSb, ZnSnSb2, NbSnSb. По св-вам близки к антимонидам антимонохалькогениды MSbX, где X = S, Se, Те. Эти соед. металлоподобны или полупроводники, при низких т-рах нек-рые из них становятся сверхпроводниками.
Антимониды щелочных и в неск. меньшей степени щел.-зем. металлов химически очень активны, легко окисляются, гидроли-зуются водой с выделением SbH3. Антимониды Mg и А1 менее активны, но легко разлагаются разб. к-тами. Все остальные антимониды взаимод. только с конц. к-тами или царской водкой. С увеличением содержания Sb в антимонидах их хим. устойчивость повышается. Нек-рые антимониды, в частности образуемые щелочными металлами, раств. в солевых расплавах, напр. в смесях LiCl-LiF или NaCl-Nal.
Известно ок. 15 сравнительно редких минералов, относящихся к антимонидам, напр. дискразит Ag3Sb, брейтгауптит NiSb, уль-манит NiSbS.
Антимониды синтезируют гл. обр. сплавлением компонентов в вакууме или в инертной атмосфере, иногда под слоем флюса (напр., из NaCl, KC1, СаС12, ВаС12). Мелкие кристаллы и пленки получают из газовой фазы - сублимацией компонентов или путем хим. транспортных р-ций. Монокристаллы выращивают методами направленной кристаллизации, вытягивания из расплава, горизонтальной зонной плавки. Эпитаксиальные пленки получают вакуумным напылением, осаждением из жидкой и газовой фаз. Нек-рые антимониды (напр., SnSb, Cu2Sb) образуются в сплавах (баббитах, сурьмяных бронзах и др.). Осн. область применения антимонидов - полупроводниковая техника.
СВОЙСТВА АНТИМОНИДОВ 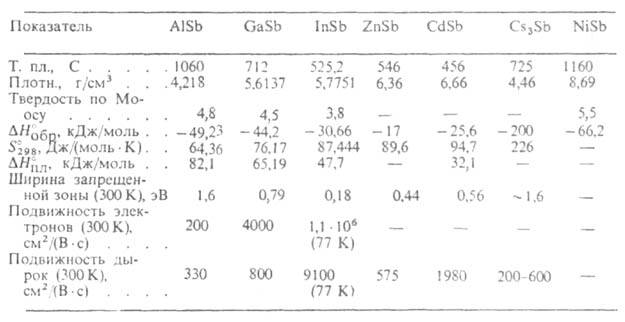
Св-ва важнейших антимонидов приведены в таблице. Антимонид алюминия AlSb-темно-серые с синеватым отливом кристаллы с металлич. блеском, решетка кубическая (а = = 0,61355 нм); перспективный материал для солнечных батарей и электронных приборов, работающих при т-рах до ~500°С. Антимонид цинка ZnSb - серые кристаллы с металлич. блеском, решетка ромбическая (а= 0,6128 нм, b = 0,7741 нм, с = 0,8115 нм, пространств. группа Рbса); материал для термоэлектрич. приборов. Антимонид цезия Cs2Sb - черные кристаллы с металлич. блеском, решетка кубическая (а = 0,9180 нм); используется для изготовления фотоэмиттеров с высоким квантовым выходом. Антимониды Cd и Mg, а также тройные соед. типа ZnSnSb2 - перспективные полупроводниковые материалы; Th3Sb4 может использоваться в кач-ве высокотемпературного термоэлектрич. материала; NiSb, как и др. Антимониды с металлич. проводимостью (CrSb, CoSb), предложено использовать как компоненты эвтектич. композиций с InSb и GaSb для магнитосопротивлений, детекторов ИК-излучения и др.
Осн. опасность при работе с антимонидами представляет SbH3, выделяющийся при действии воды или к-т на антимониды. См. также Галлия антимонид, Индия антимонид.
Литература
Самсонов Г.В., Абдусалямова М.Н., Антимониды, Душ.. 1977. П. И. Федоров, Р.Х. Акчурин.
