Сурьма
Сурьма (лат. Stibium), Sb, химический элемент V группы периодической системы Менделеева; атомный номер 51, атомная масса 121,75; металл серебристо-белого цвета с синеватым оттенком. В природе известны два стабильных изотопа 121Sb (57,25% ) и 123Sb (42,75% ). Из искусственно полученных радиоактивных изотопов важнейшие 122Sb (Т1/2 = 2,8 cym), 124Sb (T1/2 = 60,2 cym) и 125Sb (T1/2 = 2 года).
Историческая справка. Сурьма известна с глубокой древности. В странах Востока она употреблялась примерно за 3000 лет до н. э. для изготовления сосудов. В Древнем Египте уже в 19 в. до н. э. порошок сурьмяного блеска (природный Sb2S3) под названием mesten или stem применялся для чернения бровей. В Древней Греции он был известен как stími и stíbi, отсюда латинский stibium. Около 12—14 вв. н. э. появилось название antimonium. В 1789 А. Лавуазье включил сурьму в список химических элементов под названием antimoine (современный английский antimony, испанский и итальянский antimonio, немецкий Antimon). Русская «сурьма» произошло от турецкого sürme; им обозначался порошок свинцового блеска PbS, также служивший для чернения бровей (по другим данным, «сурьма» — от персидского сурме — металл). Подробное описание свойств и способов получения сурьмы и её соединений впервые дано алхимиком Василием Валентином (Германия) в 1604.
Распространение в природе. Среднее содержание сурьмы в земной коре (кларк) 5 ×10–5 % по массе. В магме и биосфере сурьма рассеяна. Из горячих подземных вод она концентрируется в гидротермальных месторождениях. Известны собственно сурьмяные месторождения, а также сурьмяно-ртутные, сурьмяно-свинцовые, золото-сурьмяные, сурьмяно-вольфрамовые. Из 27 минералов сурьмы главное промышленное значение имеет антимонит (Sb2S3) (см. также Сурьмяные руды). Благодаря сродству с серой сурьма в виде примеси часто встречается в сульфидах мышьяка, висмута, никеля, свинца, ртути, серебра и других элементов.
Физические и химические свойства. Сурьма известна в кристаллической и трёх аморфных формах (взрывчатая, чёрная и жёлтая). Взрывчатая сурьма (плотность 5,64—5,97 г/см3) взрывается при любом соприкосновении: образуется при электролизе раствора SbCl3; чёрная (плотность 5,3 г/см3) — при быстром охлаждении паров сурьмы; жёлтая — при пропускании кислорода в сжиженный SbH3. Жёлтая и чёрная сурьма неустойчивы, при пониженных температурах переходят в обыкновенную сурьму. Наиболее устойчивая кристаллическая сурьма (см. также Сурьма самородная), кристаллизуется в тригональной системе, а = 4,5064 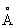 ; плотность 6,61—6,73 г/см3 (жидкой — 6,55 г/см3); tпл 630,5 °С; tкип 1635—1645 °С; удельная теплоёмкость при 20—100 °С 0,210 кдж/(кг × К) [0,0498 кал/(г ×°С)]; теплопроводность при 20 °С 17,6 вт/м × К [0,042 кал/(см × сек × °С)]. Температурный коэффициент линейного расширения для поликристаллической сурьмы 11,5 ×10–6 при 0—100 °С; для монокристалла a1 = 8,1×10–6 a2 = 19,5×10–6 при 0—400 °С, удельное электросопротивление (20 °С) (43,045×10–6 ом×см). Сурьма диамагнитна, удельная магнитная восприимчивость —0,66 ×10–6. В отличие от большинства металлов, сурьма хрупка, легко раскалывается по плоскостям спайности, истирается в порошок и не поддаётся ковке (иногда её относят к полуметаллам). Механические свойства зависят от чистоты металла. Твёрдость по Бринеллю для литого металла 325—340 Мн/м2 (32,5—34,0 кгс/мм2); модуль упругости 285—300; предел прочности 86,0 Мн/м2 (8,6 кгс/мм2). Конфигурация внешних электронов атома Sb5s25r3. В соединениях проявляет степени окисления главным образом +5, +3 и –3.
; плотность 6,61—6,73 г/см3 (жидкой — 6,55 г/см3); tпл 630,5 °С; tкип 1635—1645 °С; удельная теплоёмкость при 20—100 °С 0,210 кдж/(кг × К) [0,0498 кал/(г ×°С)]; теплопроводность при 20 °С 17,6 вт/м × К [0,042 кал/(см × сек × °С)]. Температурный коэффициент линейного расширения для поликристаллической сурьмы 11,5 ×10–6 при 0—100 °С; для монокристалла a1 = 8,1×10–6 a2 = 19,5×10–6 при 0—400 °С, удельное электросопротивление (20 °С) (43,045×10–6 ом×см). Сурьма диамагнитна, удельная магнитная восприимчивость —0,66 ×10–6. В отличие от большинства металлов, сурьма хрупка, легко раскалывается по плоскостям спайности, истирается в порошок и не поддаётся ковке (иногда её относят к полуметаллам). Механические свойства зависят от чистоты металла. Твёрдость по Бринеллю для литого металла 325—340 Мн/м2 (32,5—34,0 кгс/мм2); модуль упругости 285—300; предел прочности 86,0 Мн/м2 (8,6 кгс/мм2). Конфигурация внешних электронов атома Sb5s25r3. В соединениях проявляет степени окисления главным образом +5, +3 и –3.
В химическом отношении сурьма малоактивна. На воздухе не окисляется вплоть до температуры плавления. С азотом и водородом не реагирует. Углерод незначительно растворяется в расплавленной сурьме. Металл активно взаимодействует с хлором и др. галогенами, образуя сурьмы галогениды. С кислородом взаимодействует при температуре выше 630 °С с образованием Sb2O3(см. Сурьмы окислы). При сплавлении с серой получаются сурьмы сульфиды, так же взаимодействует с фосфором и мышьяком. Сурьма устойчива по отношению к воде и разбавленным кислотам. Концентрированные соляная и серная кислоты медленно растворяют сурьма с образованием хлорида SbCl3 и сульфата Sb2(SO4)3; концентрированная азотная кислота окисляет сурьму до высшего окисла, образующегося в виде гидратированного соединения xSb2O5 ×уН2О. Практический интерес представляют труднорастворимые соли сурьмяной кислоты — антимонаты(МеSbO3 ×3H2O, где Me — Na, К) и соли не выделенной метасурьмянистой кислоты — метаантимониты (MeSbO2 ×ЗН2О), обладающие восстановительными свойствами. Сурьма соединяется с металлами, образуя антимониды.
Получение. Сурьму получают пирометаллургической и гидрометаллургической переработкой концентратов или руды, содержащей 20—60% Sb. К пирометаллургическим методам относятся осадительная и восстановительная плавки. Сырьём для осадительной плавки служат сульфидные концентраты; процесс основан на вытеснении сурьмы из её сульфида железом: Sb2S3 + 3Fe Û 2Sb + 3FeS. Железо вводится в шихту в виде скрапа. Плавку ведут в отражательных или в коротких вращающихся барабанных печах при 1300—1400 °С. Извлечение сурьмы в черновой металл составляет более 90%. Восстановительная плавка сурьмы основана на восстановлении её окислов до металла древесным углем или каменноугольной пылью и ошлаковании пустой породы. Восстановительной плавке предшествует окислительный обжиг при 550 °С с избытком воздуха. Огарок содержит нелетучую четырёхокись сурьмы. Как для осадительной, так и для восстановительной плавок возможно применение электропечей. Гидрометаллургический способ получения сурьмы состоит из двух стадий: обработки сырья щелочным сульфидным раствором с переводом сурьмы в раствор в виде солей сурьмяных кислот и сульфосолей и выделения сурьмы электролизом. Черновая сурьма в зависимости от состава сырья и способа её получения содержит от 1,5 до 15% примесей: Fe, As, S и др. Для получения чистой сурьмы применяют пирометаллургическое или электролитическое рафинирование. При пирометаллургическом рафинировании примеси железа и меди удаляют в виде сернистых соединений, вводя в расплав сурьмы антимонит (крудум) — Sb2S3, после чего удаляют мышьяк (в виде арсената натрия) и серу при продувке воздуха под содовым шлаком. При электролитическом рафинировании с растворимым анодом черновую сурьму очищают от железа, меди и др. металлов, остающихся в электролите (Си, Ag, Аи остаются в шламе). Электролитом служит раствор, состоящий из SbF3, H2SO4 и HF. Содержание примесей в рафинированной сурьме не превышает 0,5—0,8%. Для получения сурьмы высокой чистоты применяют зонную плавку в атмосфере инертного газа или получают сурьму из предварительно очищенных соединений — трёхокиси или трихлорида.
Применение. Сурьма применяется в основном в виде сплавов на основе свинца и олова для аккумуляторных пластин, кабельных оболочек, подшипников (баббит), сплавов, применяемых в полиграфии (гарт), и т. д. Такие сплавы обладают повышенной твёрдостью, износоустойчивостью, коррозионной стойкостью. В люминесцентных лампах галофосфатом кальция активируют Sb. Сурьма входит в состав полупроводниковых материалов как легирующая добавка к германию и кремнию, а также в состав антимонидов (например, InSb). Радиоактивный изотоп 12Sb применяется в источниках g-излучения и нейтронов.
О. Е. Крейн.
Сурьма в организме. Содержание сурьмы (на 100 г сухого вещества) составляет в растениях 0,006 мг, в морских животных 0,02 мг, в наземных животных 0,0006 мг. В организм животных и человека сурьма поступает через органы дыхания или желудочно-кишечный тракт. Выделяется главным образом с фекалиями, в незначительном количестве — с мочой. Биологическая роль сурьмы неизвестна. Она избирательно концентрируется в щитовидной железе, печени, селезёнке. В эритроцитах накапливается преимущественно сурьма в степени окисления + 3, в плазме крови — в степени окисления + 5. Предельно допустимая концентрация сурьмы 10–5 — 10–7 г на 100 г сухой ткани. При более высокой концентрации этот элемент инактивирует ряд ферментов липидного, углеводного и белкового обмена (возможно в результате блокирования сульфгидрильных групп).
В медицинской практике препараты сурьмы (солюсурьмин и др.) используют в основном для лечения лейшманиоза и некоторых гельминтозов (например, шистосоматоза).
Сурьма и её соединения ядовиты. Отравления возможны при выплавке концентрата сурьмяных руд и в производстве сплавов сурьмы. При острых отравлениях — раздражение слизистых оболочек верхних дыхательных путей, глаз, а также кожи. Могут развиться дерматит, конъюнктивит и т. д. Лечение: антидоты (унитиол), мочегонные и потогонные средства и др. Профилактика: механизация производств. процессов, эффективная вентиляция и т. д.
Лит.: Шиянов А. Г., Производство сурьмы, М., 1961; Основы металлургии, т. 5, М., 1968; Исследование в области создания новой технологии производства сурьмы и ее соединений, в сборнике: Химия и технология сурьмы, Фр., 1965.
