Кетeны
КЕТEНЫ, орг. соед. общей ф-лы RR'C=C=O, содержащие систему кумулированных двойных связей С=С и С=О. Различают альдокетены (R=Н, R' - opг. радикал) и кетокетены (R и R' - opг. радикал). Физ. св-ва кетенов представлены в таблице.СВОЙСТВА КЕТЕНОВ
| Соединение | Т. пл., °С | Т. кип.. oС | ||
| Кетен СН2=C=О* | -151 | -56 | ||
| Метилкетен СН3СН= С= О | -80 | | ||
| Диметилкетен (СН3)2С= С=О | -97.5 | 34 | ||
| Диэтилкетен (C2H5)2C= С= О | | 92 | ||
| Дифенилкетен Ph2C= С=О | | 146 (11 мм рт. ст.) | ||
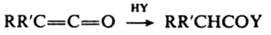
Y = ОН, ООН, OR:, SR:, NR2:, R:COO, PR2:, AsR2: Аналогично протекает р-ция с минер, к-тами, а также с металлоорг. соед.; в последнем случае при гидролизе продуктов р-ции образуются соответствующие кетоны; напр.:
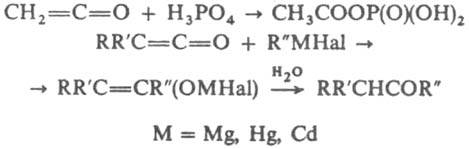
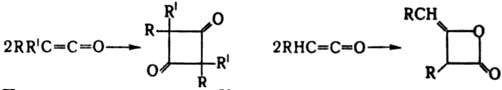
При циклодимеризации кетенов с соед., содержащими связи
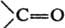
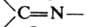 , -N=O,
, -N=O, 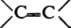 ,
,  , - N=N-, образуются соотв. b-лактоны (ф-ла I), b-лактамы (II), 1,2-оксазетидиноны (III), производные циклобутанона (IV), циклобутенона (V) и 1,2-диазетидинона (VI):
, - N=N-, образуются соотв. b-лактоны (ф-ла I), b-лактамы (II), 1,2-оксазетидиноны (III), производные циклобутанона (IV), циклобутенона (V) и 1,2-диазетидинона (VI): 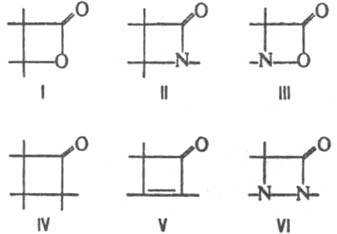
При р-ции кетена с диазометаном отщепляется азот и образуется циклопропанон (последний со второй молекулой диазометана превращ. в циклобутанон); при фотохим. разложении образуется карбен, к-рый димеризуется в этилен; при фотохим. р-ции с олефинами получаются циклопропаны:
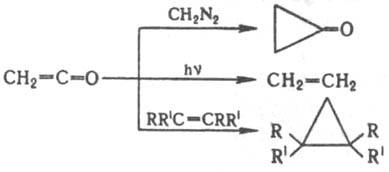
Наиб, распространенные способы синтеза кетенов-дегалогенирование галогенангидридов a-галогенкарбоновых к-т, дегидрогалогенирование галогенангидридов к-т, содержащих атом водорода в а-положении, разложение диазокетонов (Вольфа перегруппировка)., напр.:
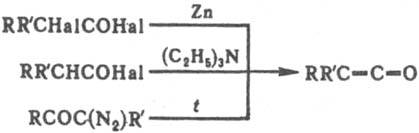
В пром-сти кетены получают пиролизом карбонильных соед., в частности кетен из СН3СООН (при 700 °С в присут. триэтилфосфата), (СН3СО)2О или ацетона. В лаб. условиях кетен получают пиролизом дикетена при 700-800 °С. Металлоорг. производные кетенов получают взаимод. ацетатов Ag или Си с (СН3СО)2О в присут. пиридина, напр.: СН3СООМ + (СН3СО)2О:М2С=С=О М = Ag, Cu(I) Эти производные - катализаторы окислительных процессов. Кетены широко применяют для синтеза орг. соед.; кетен в качестве ацетилирующего агента для спиртов, аминов, енолъных форм кетонов, напр. в произ-ве ацетатов целлюлозы, а также для получения нек-рых орг. реагентов, напр. изопропенилацетата, b-пропиолактона, уксусного ангидрида, дикетена. По токсичности кетен приближается к фосгену. Для определения содержания его в воздухе применяют р-цию с гидроксиламином и превращение образующейся ацетилгидроксамовой к-ты в комплекс с Fe(III). Лит.. Лейси Р. Н., в кн.. Успехи органической химии, т. 2, М., 1964, с. 204 254; Физер Л., Физер М.. Реагенты для органического синтеза, пер. с англ., т. 2, М., 1970. с. 125 29; Houben Weyl, Methoden der organischen Chemie, Bd 7, :П 4, Stuttg., 1968; The chemistry of functional groups. The chemistry of ketenes, allenes and related compounds, ed. by S. Patai, v. 1 2, Chichester, 1980. С. И. Завьялов.
Синонимы/примеры:*
Этенон; Карбометилен; Кетоэтилен
*подобраны ИИ, возможны неточности
Ещё по теме
Кетены — свойства и применение
Кетен — свойства и применение в промышленности
Кетен — характеристики и применение в химии
Ксантогенаты — свойства и применение
Кетоны — свойства, получение и применение
Этан — характеристики и применение
Этилен — свойства и применение
Тиенотиофены — строение и свойства
Тиетан и его производные — свойства и применение
